From Wikipedia, the free encyclopedia
Cistična fibroza jest genetički poremećaj koji najviše pogađa pluća, ali i gušteraču, jetru, bubrege i crijeva.[1][2] Dugoročni problemi uključuju otežano disanje i iskašljavanje sluzi, kao posljedica čestih infekcija pluća.[1] Ostali znakovi i simptomi mogu uključivati infekcije sinusa, slab rast, masnu stolicu, klabiranje prstiju na rukama i nogama i neplodnost kod većine muškaraca.[1] Mogu imati različite stepene simptoma.[1]
| Cistična fibroza (Mukoviscidoza) 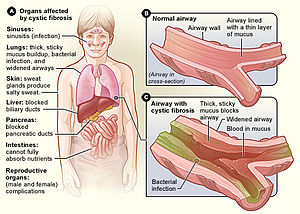 | |
|---|---|
| Klasifikacija i vanjski resursi | |
| ICD-10 | E84 |
| ICD-9 | 277.0 |
| OMIM | 219700 |
| DiseasesDB | 3347 |
| MedlinePlus | 000107 |
| eMedicine | article/1001602 |
| MeSH | D003550 |
| GeneReviews | CFTR-Related Disorders |
CF se nasljeđuje na autosomno recesivno svojstvo.[1] Uzrokovana je prisustvom mutacija u obje kopije gena za regulaciju proteinske transmembranske provodljivosti cistične fibroze (CFTR).[1] Oni koji imaju jednu aktivnu kopiju nositelji su i inače uglavnom zdravi.[3] Gen CFTR je uključen u proizvodnju znoja, probavne tečnosti i sluzi.[4] Kada CFTR nije funkcionalan, izlučevine koje su obično rijetke postaju guste.[5] Stanje se dijagnosticira pomoću testiranja znoja i genetičkog testiranja.[1] U nekim dijelovima svijeta, obavlja se skrining dojenčadi pri rođenju.[1]
Ne postoji poznati lijek za cističnu fibrozu.[3] Infekcije pluća liječe se antibioticima, koji se mogu davati intravenozno, udisati ili oralno.[1] Ponekad se dugoročno koristi antibiotik azitromicin.[1] Udisanje fiziološkog rastvora i salbutamol također može biti korisno.[1] Transplantacija pluća može biti opcija ako se funkcija pluća i dalje pogoršava.[1] Zamjena enzima pankreasa i vitamini topivi u mastima su važni, posebno kod mladih.[1] Tehnika uklanjanja sluzi, kao što je fizioterapija grudnog koša imaju neke kratkoročne koristi, ali dugoročni učinci su nejasni.[6] Prosječni životni vijek u razvijenim zemljama je između 42 i 50 godina.[7][8] 80% smrtnih slučajeva od cistične fibroze uzrokovano je plućnim komplikacijama.[1]
CF je najčešća među ljudima sjevernoevropskog porijekla i pogađa oko jedno od svakih 3.000 novorođenčadi.[1] Otprilike jedna od 25 osoba je nositelj.[3] Najmanje je uobičajena kod Afrikanaca i Azijata.[1] Bolest je 1938. godine otkrila Dorothy Andersen, sa simptomima koji su se poklapali s bolešću od 1595., ako ne i ranije.[2] Naziv "cistična fibroza" odnosi se na karakteristike fibroza i cista koje nastaju u pankreasu.[2][9]

Glavni znaci i simptomi su koža slanog okusa[10] slab rast i loše debljanje, uprkos normalnom unosu hrane,[11] nakupljanje guste, ljepljive sluzi,[12] česte infekcije grudnog koša i kašalj ili otežano disanje.[13] Muškarci mogu biti neplodni zbog urođebnog nesostatka vaas deferens.[14] Simptomi se često javljaju u beba i u djetinjstvu, kao što je opstrukcija crijeva zbog meconium ileus u novorođene djece.[15]
Kako djeca rastu, vježbaju kako bi oslobodili sluzi u alveolama.[16] Epitelne ćelije kod osoba koje imaju mutirani protein koji dovodi do abnormalno viskozne proizvodnje sluzi.[12] Loš rast kod djece obično predstavlja nemogućnost dobijanja na težini ili visini stope svojih vršnjaka i povremeno se ne dijagnosticira dok se ne pokrene istraga zbog slabog rasta. Uzroci zatajenja rasta su višestruki i uključuju hroničnu infekciju pluća, slabu apsorpciju hranjivih sastojaka kroz gastrointestinalni trakt i povećanu metaboličku potražnju zbog hroničnih bolesti.[11] U rijetkim slučajevima cistična fibroza može se manifestirati kao poremećaj koagulacije. Vitamin K se normalno apsorbuje iz majčinog mlijeka, adaptiranog mleka i kasnije čvrste hrane. Ova apsorpcija oslabljena je kod nekih pacijenata sa CF. Mala djeca posebno su osjetljiva na poremećaje malapsorpcije vitamina K, jer samo vrlo mala količina vitamina K prolazi kroz placentu, što djetetu ostavlja vrlo male rezerve i ograničenu sposobnost apsorpcije vitamina K iz prehrambenih izvora nakon rođenja. Budući da su faktori zgrušavanja II, VII, IX i X ovisni o vitaminu K, nizak nivo vitamina K može rezultirati problemima zgrušavanja. Slijedom toga, kada dijete ima neobjašnjive modrice, može se opravdati procjena zgrušavanja kako bi se utvrdilo je li prisutna osnovna.[17]

CF je uzrokovana mutacijom u genu regulacije transmembranske provodljivosti cistične fibroze (CFTR). Najčešća mutacija, ΔF508, jest delecija (Δ koja označava deleciju) tri nukleotida što rezultira gubitkom aminokiseline fenilalanin (F) na 508. poziciji na proteinu.[18][19] Ova mutacija čini dvije trećine (66–70%) slučajeva CF u cijelom svijetu i 90% slučajeva u Sjedinjenim Državama; međutim, čak preko 1.500 drugih mutacija može proizvesti CF.[20] Iako većina ljudi ima dvije aktivne kopije ('alela') gena CFTR , samo jedna je potrebna za prevenciju cistične fibroze. CF se razvija kada ni jedan alel ne može proizvesti funkcionalni protein CFTR. Dakle, CF se smatra autosomno recesivnom bolešču.
Gen CFTR , pronađen na lokusu q31.2 hromozoma 7, dugačak je 230.000 baznih parova i stvara protein koji je dug 1.480 aminokiselina. Preciznije, lokacija je između baznih parova 117,120,016 i 117,308.718, na dugom kraku hromosoma 7, regija 3, traka 1, potpojas 2, predstavljena kao 7q31.2. Strukturno, CFT je tip gena poznat kao ABC gen. Proizvod ovog gena (CFTR protein) je hloridni ionski kanal, važan u stvaranju znoja, probavnih sokova i sluzi. Ovaj protein posjeduje dva ATP-hidrolizna domena, što omogućava proteinu da koristi energiju u obliku ATP-a. Sadrži i dva domena koji se sastoje od po šest alfa-heliksa, koji omogućavaju proteinu da pređe ćelijsku membranu. Regulatorno mjesto vezanja na proteinu omogućava aktiviranje fosforilacijom, uglavnom cAMP-ovisne protein-kinaze. Karboksil terminal proteina je usidren na citoskelet, interakcijom domena PDZ.[21] Većinu CFTR u plućnim prolazima proizvode rijetke ćelije koje transportuju ione i reguliraju svojstva sluzi.[22]
Pored toga, povećavaju se dokazi da, osim CFTR, i genetički modifikatori moduliraju učestalost i težinu bolesti. Jedan od primjera je lektin koji veže manan, uključen u urođenu imunost, olakšavanjem fagocitoze mikroorganizama. Polimorfizmi u jednom ili oba alela koja vežu manan i koji rezultiraju nižim nivoima cirkulacije proteina povezani su s trostruko većim rizikom od završne faze pluća, kao i povećanim teretom hroničnih bakterijske infekcije.
Do 1/25 osoba sjevernoevropskih porijekla smatra se genetičkim nositeljem. Bolest se pojavljuje samo kada bračni parovu od njih imaju djecu, jer svaka trudnoća između njih ima 25% šanse da rodi dijete s tom bolešću. Iako samo jedno od svakih 3.000 kavkazoidne novorođenčadi ima CF, poznato je više od 900 mutacija gena koji uzrokuje CF. Dosadašnji testovi traže najčešće mutacije.[23]
Mutacije potvrđene testom razlikuju se u zavisnosti od etničke grupe osobe ili zbog pojave CF koja je već u porodici. Više od 10 miliona Amerikanaca, uključujući 1/25 kavkazosidnih, nositelji su jedne mutacije gena CF. CF je prisutan u drugim rasama, iako ne tako često kao kod ovakvih osoba. Otprilike 1/46 Latinoamerikanaca, 1/65 Afroamerikanaca i 1/90 Amerikanaca Azije nosi mutaciju gena CF.

Može se dogoditi nekoliko mutacija u genu CFTR, a različite mutacije uzrokuju različite nedostatke u CFTR proteinu, ponekad uzrokujući blažu ili težu bolest. Ovi proteinski nedostaci također su meta za lijekove koji ponekad mogu vratiti njihovu funkciju. ΔF508-CFTR, koji se javlja kod >90% pacijenata u SAD-u, stvara protein koji se presavijaju normalno i nisu na odgovarajući način transportirani do ćelijske membrane, što rezultira njihovim degradacijama.
Druge mutacije rezultiraju prekratkim proteinima (skraćenim) jer proizvodnja prerano završava. Druge mutacije proizvode proteine koji normalno ne koriste energiju (u obliku ATP), ne dopuštaju hloridu, jodidu i tiocijanatu da odgovarajuće prođu membranu,[24] i razgrađuju se većom brzinom od uobičajene. Mutacije mogu dovesti i do stvaranja manje kopija CFTR proteina.[25]
Protein stvoren ovim genom usidren je na vanjskoj membrani ćelija u znojnim žlijezdama, plućima, pankreasu i svim ostalim preostalim egzokrinim žlijezdama u tijelu.
Protein se proteže kroz ovu membranu i deluje kao kanal koji povezuje unutrašnji dio ćelije (citoplazma sa okolnom tečnosti). Ovaj kanal primarno je odgovoran za kontrolu kretanja halogenidnih aniona, iznutra prema vani ćelije; međutim, u znojnim kanalima olakšava kretanje hlorida iz znojnog kanala u citoplazmu. Kada CFTR protein ne resorbuje ione u znojnim kanalima, hlorid i tiocijanat[26] oslobođeni iz znojnih žlijezda zadržavaju se unutar kanala i ispumpavaju do kože.
Pored toga, ne može se proizvesti hipotiocijanit, OSCN, sistem imunske odbrane.[27][28] Budući da je hlorid negativno nabijen, to modificira električni potencijal unutar i izvan ćelije, zbog čega kationi prelazu u ćeliju. Natrij je najčešći kation u vanćelijskom prostoru. Višak hlorida u znojnim kanalima sprečava resorpciju natrija epitelnim natrijevim kanalima, a kombinacija natrija i k+hlorida stvara so, koja se u velikim količinama gubi u znoju osoba sa CF. Ova izgubljena so čini osnovu za test znoja.[25]
Većina oštećenja kod CF nastaje zbog začepljenja uskih prolaza zahvaćenih organa zgusnutim sekretom. Te blokade dovode do remodeliranja i infekcije u plućima, oštećenja nakupljenim probavnih enzimima u gušterači, začepljenja crijeva gustim izmetom itd. Postavljeno je nekoliko teorija o tome kako defekti u proteinima i ćelijskoj funkciji uzrokuju kliničke efekte. Najsuvremenija teorija sugerira da neispravan transport iona dovodi do dehidracije epitela dišnih puteva, zgušnjavanja sluzi. U epitelnim ćelijama disajnih puteva, treplje postoje između apikalne površine ćelije i sluzi u sloju poznatom kao površinska tečnost disajnih puteva (ASL). Protok iona iz ćelije i u ovaj sloj određen je ionskim kanalima, kao što je CFTR. CFTR ne samo da dopušta iznošenje hloridnih iona iz ćelije u ASL, već regulira i drugi kanal zvani ENac, koji omogućava natrijevim ionima da napuste ASL i uđu u respiratorni epitel. CFTR normalno inhibira ovaj kanal, ali ako je CFTR neispravan, natrij slobodno teče iz ASL-a i dolazi u ćeliju.
Kako voda prati natrij, dubina ASL će se iscrpljivati, a treplje će ostati u sluzničkom sloju.[29] Kako se treplje ne mogu efikasno kretati u gustom, viskoznom okruženju, nedostaje mukocilijskii klirens i dolazi do nakupljanja sluzi, što začepljuje male dišne puteve.[30] Nakupljanje viskozne sluzi bogate hranjivim sastojcima, u plućima omogućava bakterijama da se sakriju od imunskog sistema, što uzrokuje ponovljene respiratorne infekcije. Prisustvo istih CFTR proteina u kanalu gušterače i znojnim žlijezdama na koži također uzrokuju simptome u ovim sistemima.

Cistična fibroza može se dijagnosticirati različitim metodima, uključujući skrining novorođenčadi, testiranje znoja i genetičko testiranje.[31] Od 2006. godine u Sjedinjenim Državama, 10% slučajeva dijagnosticira se ubrzo nakon rođenja, kao dio programa skrininga novorođenčadi. Za novorođenče, u početku mjeri se povišena koncentracija imunoreaktivnog tripsinogena u krvi.[32] Da bi potvrdila dijagnoza CF, za dojenčad s abnormalnim skriningom za novorođenčad, potreban je test znoja,
U mnogim slučajevima, roditelj postavlja dijagnozu jer je dojenče slanog okusa.< Imunoreaktivni nivoi tripsina mogu se povećati kod osoba koje imaju jednu mutiranu kopiju gena CFTR (nositelji) ili rijetki slučajevi, kod osoba sa dvije normalne kopije gena CFTR . Zbog ovih lažno pozitivnih slučajeva, skrining kod novorođenčadi može biti kontroverzan.[33][34]
Osobe s CF mogu biti uvedene u registar bolesti, koji omogućava istraživačima i ljekarima da prate zdravstvene rezultate i identificiraju kandidate za klinička ispitivanja.[35]
Iako nisu poznati lijekovi za CF, koristi se nekoliko metoda liječenja. Upravljanje CF značajno se poboljšalo tokom proteklih 70 godina. Dok bi novorođenčad rođena s njim prije 70 godina bilo malo vjerojatno da će živjeti dalje od svoje prve godine, dojenčad će danas vjerojatno živjeti i do odrasle dobi. Nedavni napredak u liječenju cistične fibroze značio je da takve osobe sa mogu živjeti punijim životom manje opterećeni svojim stanjem. Temelji upravljanja su proaktivni tretman infekcija dišnih puteva i podsticanje dobre prehrane i aktivnog načina života. Plućna rehabilitacija kao upravljanje CF-om nastavlja se tokom čovjekova života i usmjerena je na maksimiziranje funkcije organa, a time i na kvalitet života. Radni terapeuti koriste tehnike uštede energije (ECT) u procesu rehabilitacije pacijenata sa cističnom fibrozom.[36] Examples of energy conservation techniques are ergonomic principles, pursued lip breathing, and diaphragmatic breathing.[37] Pacijenti sa CF imaju umor i dispneju zbog hroničnih plućnih infekcija, pa smanjenje količine energije potrošene tokom aktivnosti može im pomoći da se osjećaju bolje i steknu veću neovisnost. U najboljem slučaju, sadašnji tretmani odgađaju pad funkcije organa. Zbog širokih razlika u simptomima bolesti, liječenje se obično odvija u specijalističkim multidisciplinarnim centrima i prilagođeno je pojedincu. Ciljevi za terapiju su pluća, gastrointestinalni trakt (uključujući dodatke enzima gušterače), reproduktivni organi (uključujući pomoćnu reproduktivnu tehnologiju) i psihološka podrška.
Najdosljedniji aspekt terapije kod CF je ograničavanje i liječenje oštećenja pluća uzrokovanih gustom sluzi i infekcijama, s ciljem održavanja kvaliteta života. Intravenska, inhalacija i oralni antibiotici koriste se za liječenje hroničnih i akutnih infekcija. Mehanički uređaji i inhalacijski lijekovi koriste se za izmjenu i pročišćavanje zgusnute sluzi. Ove terapije, iako su učinkovite, mogu izuzetno dugo trajati. Terapija kisikom kod kuće preporučuje se onima sa značajnim niskim nivoom kiseika.[38] Mnogi ljudi sa CF koriste probiotike, za koje se smatra da mogu ispraviti crijevnu disbiozu i upale, ali dokazi iz kliničkih ispitivanja u vezi sa efikasnošću probiotika za smanjenje pogoršanja pluća kod osoba sa CF nisu sigurni.[39]
Transplantacija pluća može postati neophodna za osobe sa CF kako opadaju plućna funkcija i tolerancija vježbanja. Iako je pojedinačna transplantacija pluća moguća i kod drugih bolesti, osobama sa CF moraju se zamijeniti oba plućna krila, jer preostala pluća mogu sadržavati bakterije koje mogu inficirati presađeno pluće. Transplantacija gušterače ili jetre može se izvesti istovremeno za ublažavanje bolesti jetre i/ili dijabetesa.[40] Transplantacija pluća uzima se u obzir kada funkcija pluća opadne do te mjere da je potrebna pomoć mehaničkih uređaja ili je nečije preživljavanje ugroženo.[41] Prema Merckovom priručnik za dijagnozu i terapiju, "bilateralna transplantacija pluća za teške bolesti pluća postaje sve rutinskija i uspješnija sa iskustvom i poboljšanim tehnikama. Među odraslima s CF, medijana preživljavanja nakon transplantacije je oko 9 godina.[42]
Prognoza za cističnu fibrozu poboljšala se zbog ranije dijagnoze kroz skrining i bolji tretman i pristup zdravstvenoj zaštiti. Godine 1959. srednja dob preživljavanja djece sa CF u Sjedinjenim Državama bila je šest mjeseci.[43] U 2010. godini procjenjeno se da će preživljavanje za žene biti 37 godina, a za muškarce 40.[44]
U SAD-u, od onih s CF, koji imaju više od 18 godina od 2009. godine, 92% je završilo srednju školu, 67% je imalo barem neko fakultetsko obrazovanje, 15% je bilo invalidno, 9% je bilo nezaposleno, 56% bilo je samaca , a 39% je bilo u braku ili živi s partnerom.[45]
| Mutcija | Frekvencija (svjetska)[46] |
|---|---|
| ΔF508 | 66%–70% |
| G542X | 2,4% |
| G551D | 1,6% |
| N1303K | 1,3% |
| W1282X | 1,2% |
| Sve ostale | 27,5% |
Cistična fibroza je najčešća autosomno recesivna bolest, koja ograničava život među ljudima evropskog naslijeđa.[47] U Sjedinjenim Državama oko 30.000 osoba ima CF; većini se dijagnosticira sa šest mjeseci života. U Kanadi oko 4.000 ljudi ima CF.[48] Otprilike 1/25 ljudi evropskog porijekla i 1/30 evropeidnih Amerikanaca,[49] je nositelj CF mutacije. Iako je CF rjeđi u ovim skupinama, otprilike 1/46 Latinoamerikanaca, 1/65 Afroamerikanaca i 1/90 azijatskog porijekla nosi barem jednu abnormalnost gena CFTR.[50][51] Ireland has the world's highest prevalence of CF, at one in 1353.[52]
Iako je tehnički rijetka bolest, CF se svrstava među najrasprostranjenije genetičke bolesti koje skraćuju život. Najčešća je u zemljama zapadnog svijeta. Izuzetak je Finska, gdje samo svaka od 80 osoba nosi CF mutaciju.[53] Prema Svjetskoj zdravstvenoj organizaciji : "U Evropskoj uniji utvrđeno je da je jedno od 2000-3000 novorođenčadi pogođeno CF-om".[54] In the United States, one in 3,500 children is born with CF.[55] U 1997. otprilike 1/3.300 evropeidne djece u Sjedinjenim Državama rođeno je s CF. Suprotno tome, samo jedno od 15.000 afroameričke djece patilo je od toga, a kod azijskih Amerikanaca stopa je bila čak i niža na jedno od 32.000.[56]
Cistična fibroza pogađa podjednako i muškarce i žene. Iz razloga koji ostaju nejasni, podaci su pokazali da muškarci imaju duži životni vijek od žena,[57][58] iako nedavne studije sugeriraju da ova rodna razlika možda više i ne postoji, možda zbog poboljšanja u zdravstvenim ustanovama.[59][60] Nedavno istraživanje iz Irske utvrdilo je vezu između ženskog hormona estrogena i lošijih ishoda kod CF.[61]
Distribucija alela CF razlikuje se među populacijama. Učestalost nositelja ΔF508 procijenjena je na 1/200 u sjevernoj Švedskoj, 1/143 u Litvaniji i 1/38 u Danskoj. Nije pronađen nijedan nositelj ΔF508 među 171 Finaca i 151 pripadnika Saami naroda.[62] ΔF508 se javlja u Finskoj, ali tamo je manjinski alel. Poznato je da se u Finskoj CF javlja u samo 20 porodica (rodoslova).[63]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.