
Aromatičnost
From Wikipedia, the free encyclopedia
Aromatičnost – u hemiji – je svojstvo cikličnih (prstenastih), ravnih struktura sa pi-vezama u rezonanciji (one koje sadrže delokalizirane elektrone), što daje povećanu stabilnost u odnosu na druge geometrijske ili vezne aranžmane s istim skupom atoma. Aromatski prstenovi su vrlo stabilni i ne raspadaju se lahko. Organski spojevi koji nisu aromatski klasificirani su kao alifatski spojevi – oni mogu biti ciklični, ali samo aromatični prstenovi imaju poboljšanu stabilnost.
Budući da su najčešći aromatski spoj evi derivati benzena (aromatski ugljikovodik uobičajen u nafti i njegovim izvedenicama). Riječ aromatski povremeno se neformalno odnosi na derivate benzena, pa je tako prvo definirano. Ipak, postoje mnogi aromatski spojevi koji nisu benzenski. Naprimjer, u živim organizmima najčešći aromatski prstenovi su dvostruko prstenaste baze u RNK i DNK. Aromatskna funkcionalna grupa ili drugi supstituent naziva se aril grupa.
Najranija upotreba izraza "aromatski" bila je u članku Augusta Wilhelma Hofmanna, 1855.[1] Hofmann je izraz koristio za klasu benzenskih spojeva, od kojih mnogi imaju miris (arome), za razliku od čistih zasićenih ugljikovodika. Aromatičnost kao hemijsko svojstvo nema opću vezu sa mirisnim svojstvima takvih spojeva (kako mirišu), iako su 1855., prije nego što je shvaćena struktura benzena ili organskih spojeva, hemičari poput Hofmanna počeli shvatati da su mirisave molekule iz biljaka, poput terpena, imale hemijska svojstva za koja danas prepoznajemo da su slična nezasićenim naftnim ugljovodonicima poput benzena.
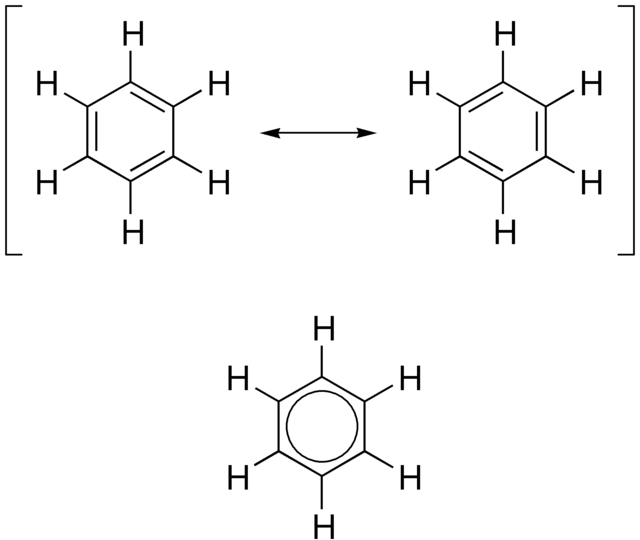
U pogledu elektronske prirode molekule, aromatičnost opisuje konjugirani sistem, često napravljen od naizmjeničnih jednostrukih i dvostrukih veza u prstenu. Ova konfiguracija omogućava da se elektroni u pi-sistemu molekule delokaliziraju oko prstena, povećavajući stabilnost molekule. Molekula ne može biti predstavljena jednom strukturom, već rezonancijskim hibridom različitih struktura, kao naprimjer sa dvije rezonantne strukture benzena. Ove molekule nije moguće pronaći ni u jednom od ovih prikaza, s dužim pojedinačnim vezama na jednom mjestu, a kraćim dvostrukim vezama na drugom. Umjesto toga, molekule imaju dužine veza između jednostruke i dvostruke veze. Ovaj često viđeni model aromatskih prstenova, naime ideju da je benzen nastao od šesteročlanog ugljeničkog prstena sa naizmeničnom jednostrukom i dvostrukom vezom (cikloheksatrien), razvio je August Kekulé. Model benzena sastoji se od dva rezonantna oblika, što odgovara dvostrukim i jednostrukim vezama koje se naslažu da bi nastalo šest jednoipolovinskih-veza. Benzen je stabilnija molekula nego što bi se očekivalo bez obračunavanja delokalizacije naboja.