
Estáu d'oxidación
From Wikipedia, the free encyclopedia
En química, l'estáu d'oxidación (EDO) ye un indicador del grau d'oxidación d'un átomu que forma parte d'un compuestu o otra especie química (por casu un ion). Formalmente, ye la carga llétrica hipotética que l'átomu tendría si tolos sos enllaces con elementos distintos fueren 100 % iónicos. El EO ye representáu por númberos, que pueden ser positivos, negativos o cero. En dellos casos, l'estáu d'oxidación permediu d'un elementu ye una fracción, tal como +8/3 pal fierro na magnetita (Fe3O4). El mayor EO conocíu ye +8 pa los tetraóxidos de ruteniu, xenón, osmiu, iridiu, hassio y dalgunos compuestos complexos de plutoniu, ente que'l menor EO conocíu ye -4 pa dellos elementos del grupu del carbonu (elementos del grupu 14).

La oxidación dase cuando un elementu o compuestu pierde unu o más electrones. Xeneralmente, cuando una sustancia aferrúñase (pierde electrones), otra sustancia recibe o capta dichos electrones amenorgándose. Este ye'l mecanismu básicu que promueve les reacciones d'óxido-reducción o redox.
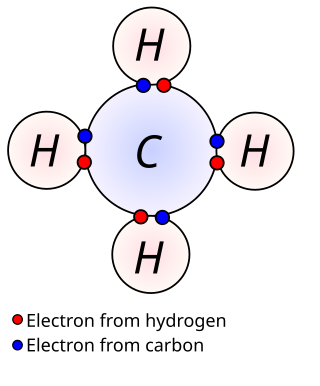
Un átomu tiende a obedecer la regla del octeto para asina tener una configuración electrónica igual a la de los gases nobles, que son bien estables químicamente (los sos átomos nun formen enllaces químicos cuasi con naide, nin siquier con ellos mesmos). Dicha regla sostién qu'un átomu tiende a tener ocho electrones nel so nivel d'enerxía más esternu. Nel casu del hidróxenu este tiende a tener 2 electrones, lo cual apurriría-y la mesma configuración electrónica que la del heliu.
Cuando un átomu A precisa, por casu, 3 electrones pa obedecer la regla del octeto, entós dichu átomu tiende a tener un númberu d'oxidación de -3, cuando adquiera esos 3 electrones. Per otru llau, cuando un átomu B tien los 3 electrones que tienen de ser vencíos por que el átomu A cumpla la llei del octeto, entós esti átomu tiende a tener un númberu d'oxidación de 3+, cuando dexe esos 3 electrones. Nesti exemplu podemos deducir que los átomos A y B pueden xunise pa formar un compuestu, y que esto depende de les interacciones ente ellos. La regla del octeto y del dueto pueden ser satisfeches compartiendo electrones (formando compuestos covalentes, por casu en molécules como l'agua) o venciendo y adquiriendo electrones (formando compuestos iónicos como por casu nos cristales de cloruru de sodiu).
Los elementos químicos estremar en 3 grandes grupos, clasificaos pol tipu de carga llétrica que pueden adquirir al participar nuna reacción química:
- Metales.
- Non metales.
- Gases nobles.
Esisten elementos metálicos que, dependiendo de les condiciones a que sían sometíos, pueden funcionar como metales o non metales indistintamente. A estos elementos denominar semimetales o metaloides.
Los elementos metálicos (los cualos tienden a dexar electrones) cuando formen compuestos tienen de normal estaos d'oxidación positivos. Los elementos non metálicos y semimetálicos, sicasí, pueden tener estaos d'oxidación positivos y negativos, dependiendo del compuestu que tean constituyendo.
