
Acid percloric
compus chimic / From Wikipedia, the free encyclopedia
Acidul percloric (HClO4) este cel mai stabil dintre oxoacizii clorului și, totodată, cel mai tare și mai acid dintre acizii oxigenați. El se poate obține în stare liberă din sărurile lui, prin tratare cu H2SO4, apoi distilare sub presiune redusă.
Mai multe informații Denumiri, Alte denumiri ...
| Acid percloric | |
 Model 3D | |
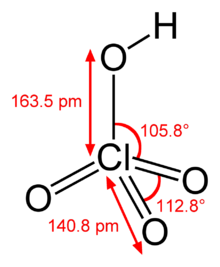 Structura moleculară | |
| Denumiri | |
|---|---|
| Alte denumiri | - |
| Identificare | |
| Număr CAS | 7601-90-3 |
| PubChem CID | 24247 |
| Informații generale | |
| Formulă chimică | HClO4 |
| Aspect | lichid colorat |
| Masă molară | 100.46 g/mol |
| Proprietăți | |
| Densitate | 1.67 g/cm3 |
| Starea de agregare | lichid |
| Punct de topire | -112 °C (anhidru) |
| Punct de fierbere | 203°C |
| Solubilitate | miscibil în apă |
| Anion | Hidrogen |
| Cation | Perclorat |
| Duritate (Scara Mohs) | - |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
| Modifică date / text | |
Închide
În stare anhidră se prepară prin distilarea în vid a acidului percloric concentrat, în prezența unui agent deshidratant, cum este percloratul de magneziu.