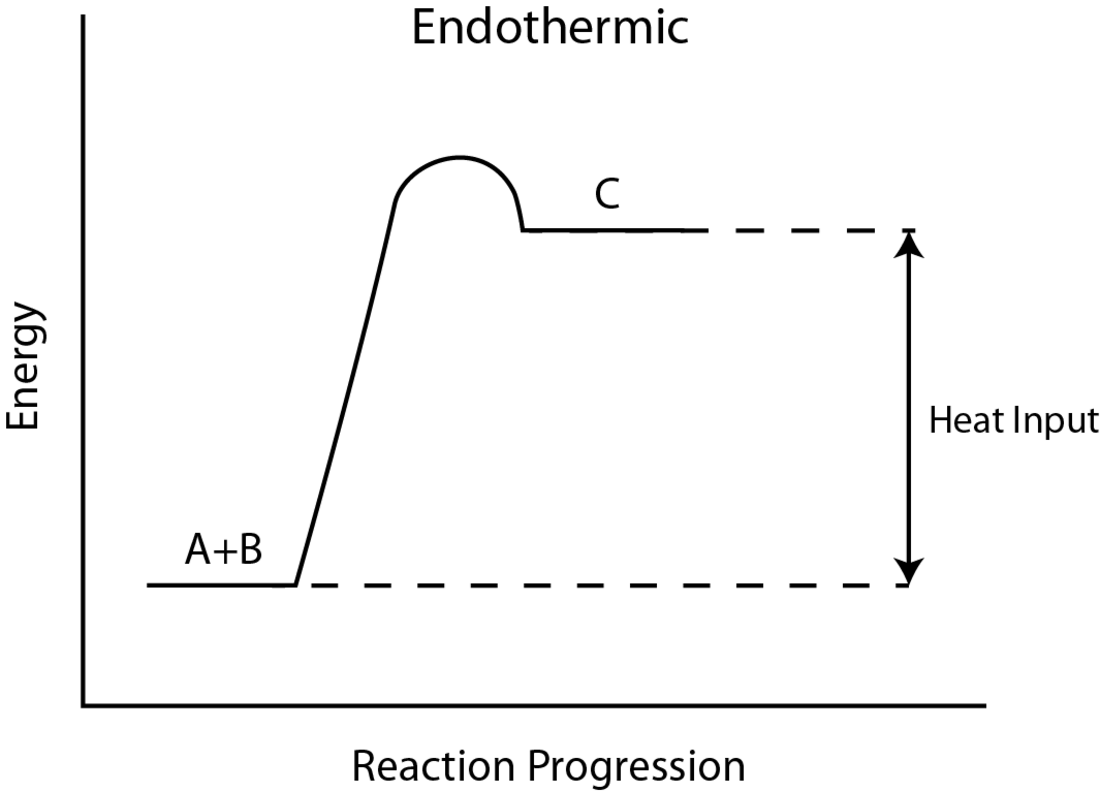
吸热过程
来自维基百科,自由的百科全书
在热化学中,吸热过程(來自希臘語 ἔνδον (endon),意即:“在……里”,和 θερμ- (therm),意即:“热” )是系统的焓H(或内能U)增加的任何热力学过程。 [1]在这样的过程中,封闭系统通常从其周围吸收热能,这就是热量传递到系统中。因此,吸热反应通常会导致系统温度升高和环境温度降低。它可能是一个化学过程,例如溶解硝酸铵(NH
4NO
3 )水溶液(H
2O) 或物理过程,例如冰块的融化。
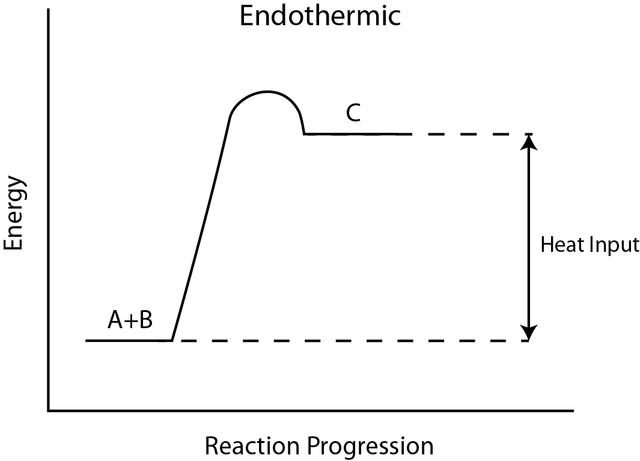
该术语由19世纪法国化学家马赛兰·贝特洛创造。与吸热过程相反的是放热过程,它释放或“释放”能量,通常以热的形式存在,有时以电能的形式存在。因此,在每个术语(吸热和放热)中,前缀指的是过程发生时热量(或电能)的去向。
化学中的应用
由于在各种过程(状态变化、化学反应)中键断裂和形成,通常会发生能量变化。如果形成键的能量大于断裂键的能量,则能量被释放。这被称为放热反应。但是,如果打破键所需的能量多于释放的能量,则能量会被吸收。因此,它是一个吸热反应。 [2]
细节
一个过程能否自发发生不仅取决于焓变,还取决于熵变( ∆S )和绝对温度T。如果某个过程在特定温度下是自发过程,则产物的吉布斯自由能G = H – TS低于反应物(放能过程),[1]即使产物的焓更高。因此,吸热过程通常需要系统中有利的熵增加( ∆S > 0 ),以克服不利的焓增加,以便仍然∆G < 0 。虽然吸热相变到更无序的更高熵状态(例如熔化和汽化)很常见,但在中等温度下的自发化学过程很少吸热。在假设的强吸热过程中,焓增加∆H ≫ 0通常导致∆G = ∆H – T∆S > 0 ,这意味着该过程不会发生(除非由电能或光子能驱动)。吸热和放能过程的一个例子是
例子
参考资料
Wikiwand - on
Seamless Wikipedia browsing. On steroids.