Hajos–Parrish–Eder–Sauer–Wiechert反应
維基百科,自由的 encyclopedia
Hajos–Parrish–Eder–Sauer–Wiechert反应(Hajos–Parrish[1][2]–Eder–Sauer–Wiechert[3] reaction)
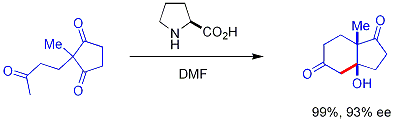
由脯胺酸催化的不对称羟醛反应。此反应以其在罗氏(Hajos、Parrish)和先灵公司(Eder、Sauer、Wiechert)的早期研究者的名字而命名。这是有机催化的早期例子,也是第一个实现的非金属催化的羟醛反应。 最早是在20世纪70年代由 Hajos 和 Parrish 发现,如下图所示:
他们以非手性的三酮作为原料,用天然存在的手性脯胺酸作为催化剂,用3mol%的(S)-(-)-脯氨酸,就可以100%产率和93%ee实现底物的分子内羟醛反应。反应是在二甲基甲酰胺中进行,温度适中。他们也因此分离出了羟醛加成产物——双环酮醇。该加成产物最近才有人利用该实验再次分离出来。[4]
先灵公司的研究组则将反应在非生理条件下进行,以47mol%的(S)-脯氨酸催化,80°C下,在 1N 高氯酸的乙腈溶液中进行反应。他们因此无法分离出酮醇产物,只得到了失水后产生的羟醛缩合产物((7aS)-7a-甲基-2,3,6,7-四氢吲哚-1,5-二酮)。[5]
Hajos 和 Parrish 接下来又用圆二色谱和单晶X射线衍射对上述酮醇产物的结构进行了分析,结果显示酮醇中的六元环为椅型构象,其中角甲基占据直键、羟基占平键,与洋地黄糖苷元(digitoxigenin)中CD环的构象类似(左下图)。[6]但是,酮醇产物的7a-乙基类似物则不然,该分子中乙基处于平键、羟基处于直键,以避免另一构象中乙基与 C-4 和 C-6 之间更为强烈的1,3-二轴交互作用(右下图)。
2000年[7][8],List 和 Barbas 等人尝试用简单的仲胺来模拟以烯胺活化机理催化羟醛反应的天然Ⅰ型醛缩酶[9],选用(S)-脯氨酸来做丙酮和对硝基苯甲醛的分子间直接羟醛反应,实现了68%产率、76%ee。[10]一般认为这标志着有机催化复兴的开始。 有机催化的分子间羟醛反应也被称为 List-Barbas 羟醛反应。[11]
上述反应的副反应有酮与脯氨酸生成噁唑啉酮,以及醛与脯氨酸生成亚甲胺叶立德。List 等以高浓度的丙酮作为底物以抑制副反应的发生。 他们还考察了一些脯氨酸的类似物,但是发现大多数催化能力不如脯氨酸,还是最便宜的脯氨酸几乎是最好的催化剂。 不过5,5-二甲基噻唑-4-羧酸的催化效果也十分良好。[12]
同年 Notz 和 List 又将此反应拓展至邻二醇的合成:[13]
1985年有人将该反应用于 Wieland-Miescher酮的不对称合成,利用丁烯酮与2-甲基-1,3-环己二酮先发生麦克尔加成,然后再在脯氨酸催化下,发生羟醛反应成环制得产物。[14]总过程是一种罗宾逊成环反应。产物 W-M 酮是许多固醇类和萜类化合物的合成前体。 2000年,Barbas 等实现了脯氨酸催化下利用串联麦克尔-羟醛反应制取 Wieland-Miescher 酮的不对称合成。[15]
2002年,美国的 MacMillan(大卫·麦克米兰)用脯氨酸作催化剂首次实现了不同的醛之间的羟醛反应。克服了做醛的交叉羟醛反应时醛的自身缩合问题。[16]