Loading AI tools
来自维基百科,自由的百科全书
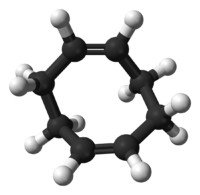
1,5-环辛二烯是一种有机化合物,化学式为C8H12,通常可以简写成COD。这种二烯烃是制备其他有机物的重要前体,并在金属有机化学用作配体。[2][3]
| 1,5-环辛二烯 | |
|---|---|

| |
| |
| IUPAC名 Cycloocta-1,5-diene[1] | |
| 识别 | |
| CAS号 | 111-78-4 |
| ChemSpider | 74815 |
| SMILES |
|
| InChI |
|
| InChIKey | VYXHVRARDIDEHS-QGTKBVGQBM |
| EC编号 | 203-907-1 |
| 性质 | |
| 化学式 | C8H12 |
| 摩尔质量 | 108.18 g·mol−1 |
| 外观 | 澄清无色液体 |
| 密度 | 0.882 g cm−3(液态) |
| 熔点 | -69.5 °C(204 K) |
| 沸点 | 151 °C(424 K) |
| 溶解性(水) | - |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
1,5-环辛二烯可由1,3-丁二烯在镍催化剂作用下二聚制得,同时得到的副产物还有乙烯基环己烯。2005年时全球大约生产了10,000吨1,5-环辛二烯。[4]
1,5-环辛二烯与乙硼烷二甲基硫醚加合物(相当于甲硼烷)反应产生9-硼二环[3.3.1]壬烷,[5] 后者简称9-BBN,是有机化学中用于硼氢化反应的试剂:
1,5-环辛二烯与二氯化硫或类似试剂加成得到2,6-二氯代-9-硫代双环[3.3.1]壬烷:[6]
1,5-环辛二烯可以与低价金属通过碳碳双键形成典型的不饱和烃配合物。配合物Ni(cod)2是制备多种Ni(0)和Ni(II)配合物的前体。金属环辛二烯配合物很具有吸引力,因为它们足够稳定可以被分离出来,稳定性通常超过类似的乙烯配合物。环辛二烯配合物的稳定性是螯合效应造成的。环辛二烯配体很容易被其他配体取代,例如膦。
Ni(COD)2可以在环辛二烯配体存在条件下,用三乙基铝还原无水二(乙酰丙酮)合镍制得[8]:
类似的Pt(COD)2需要用迂回的路线制备,反应中需使用环辛四烯基二锂[9]:
目前已有大量关于环辛二烯配合物的研究报道,其中许多发表在无机合成(Inorganic Syntheses)第25、26和28卷上。铂配合物已经使用在许多配合物的合成中:
环辛二烯配合物是有用的起始原料,以下反应是一个值得注意的例子:
生成物Ni(CO)4有剧毒,因此在反应容器中生成它比直接配制更安全。其他低价金属的环辛二烯配合物包括Mo(COD)(CO)4、[RuCl2(COD)]n和Fe(COD)(CO)3。环辛二烯在Rh(I)和Ir(I)的配位化学中特别重要,例如克拉布特里催化剂和环辛二烯氯化铑二聚体。平面四边形的配合物[M(COD)2]+也是已知的(M = Rh、Ir)。

1,5-环辛二烯张力很大的反-反异构体是一种已知的化合物。(E,E)-COD最早由乔治·怀特塞兹和阿瑟·科普在1969年通过顺式异构体的光异构化制得。[10]另一种合成路线(八元环的双消除反应)由罗尔夫·胡伊斯根于1987年报道。[11](E,E)-COD的构象是扭船式而不是椅式的。这种化合物已被研究用于点击化学的介质。[12]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.