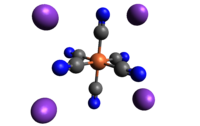
亚铁氰化钾,俗称黄血盐,化学式为K4[Fe(CN)6]·3H2O,它是配位化合物[Fe(CN)6]4−的钾盐。室温下为柠檬黄色单斜晶体。
| 亚铁氰化钾 | |
|---|---|

| |
| |

| |
| IUPAC名 Potassium hexacyanoferrate(II) 六氰合铁(II)酸钾 | |
| 别名 | 亚铁氰化钾 黄血盐 |
| 识别 | |
| CAS号 | 13943-58-3(无水) 14459-95-1(三水) |
| PubChem | 161067 |
| ChemSpider | 20162028 |
| SMILES |
|
| EINECS | 237-722-2 |
| 性质 | |
| 化学式 | K4[Fe(CN)6] |
| 摩尔质量 | 三水:422.388 g·mol⁻¹ |
| 外观 | 淡黄色结晶颗粒 |
| 密度 | 1.85 g/cm3(三水) |
| 熔点 | 70 °C(343 K) |
| 沸点 | 400 °C(673 K) |
| 溶解性(水) | 28.9 g/100 mL(三水,20°C) |
| 溶解性 | 不溶于乙醇、乙醚 |
| 磁化率 | −130.0·10−6 cm3/mol |
| 结构 | |
| 晶体结构 | 单斜 |
| 危险性 | |
GHS危险性符号
| |
| GHS提示词 | Warning |
| H-术语 | H411 |
| P-术语 | ? |
| NFPA 704 | |
| 闪点 | 不燃 |
| 致死量或浓度: | |
LD50(中位剂量)
|
6400 mg/kg(大鼠口服)[1] |
| 相关物质 | |
| 其他阴离子 | 铁氰化钾 |
| 其他阳离子 | 亚铁氰化钠 普鲁士蓝 |
| 附加数据页 | |
| 结构和属性 | 折射率、介電係數等 |
| 热力学数据 | 相變数据、固、液、气性质 |
| 光谱数据 | UV-Vis、IR、NMR、MS等 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
合成
1752年,法国化学家皮埃尔·约瑟夫·麦克尔首先报道了亚铁氰化钾的制备,他通过使普鲁士蓝与氢氧化钾反应来实现。[2][3]
亚铁氰化钾在工业上由氰化氢、氯化亚铁和氢氧化钙生产,它们组合生成亚铁氰化钙Ca2[Fe(CN)6]·11H2O。然后用钾盐处理该溶液以沉淀混合的钾-钙盐CaK2[Fe(CN)6],最后再用碳酸钾处理得到钾盐。[4]
从历史上看,该化合物是由含有氮、铁和碳酸钾的有机化合物制成的。[5]常见的氮源和碳源是焙烧后的角、皮革废料、内脏或干血。它也可以从煤气厂的废氧化物(含有氰化氢)中获得。
化学性质
用硝酸处理亚铁氰化钾可以得到H2[Fe(NO)(CN)5]。用碳酸钠中和后,可以选择性地结晶出硝普钠的红色晶体。[6]
- 2 K4[Fe(CN)6] + Cl2 → 2 K3[Fe(CN)6] + 2 KCl
该反应可用于从溶液中去除亚铁氰化钾。[來源請求]
应用
亚铁氰化钾在工业中有许多应用。它和其钠盐被广泛用作路盐和食盐的抗结剂。亚铁氰化钾和亚铁氰化钠也被用于锡的提纯和从钼矿石中分离铜。亚铁氰化钾可用于生产葡萄酒和柠檬酸。[4]
截至2017年,在欧盟,亚铁氰酸盐(E535–538)仅被授权在两个食品类别中作为盐替代品。肾是亚铁氰酸盐毒性的器官。[7]
亚铁氰化钾可用于动物饲料。[8]
在实验室中,亚铁氰化钾用于确定高锰酸钾的浓度,这种化合物通常用于氧化还原滴定。 亞铁氰化钾与铁氰化钾和磷酸盐缓冲溶液混合使用,为β-半乳糖苷酶提供缓冲液,该酶用于裂解X-gal,使与β-gal共轭的抗体(或其他分子)与目标结合的地方呈现出明亮的蓝色。 在与铁离子反应时,它会产生普鲁士蓝色。因此,它被用作实验室中铁的鉴定试剂。
亚铁氰化钾可用作植物的肥料。[來源請求]
公元1900年前,在卡斯纳法发明之前,亚铁氰化钾是碱金属氰化物的最重要来源。[4]在这个历史过程中,氰化钾是通过分解亚铁氰化钾产生的[5]:
- K4[Fe(CN)6] → 4 KCN + FeC2 + N2
其中,FeC2是计量比组成的混合物,包括α-Fe、C和Fe3C等。[9]若在空气中热分解,则会有KFeO2等氧化产物。[10]
结构
与其他金属氰化物一样,亚铁氰化钾不管是水合物还是无水盐,都具有复杂的聚合结构。该聚合物由八面体 [Fe(CN)6]4−中心与CN配体结合的K+离子交联。[11]当固体溶解在水中时,K-CN键会断裂。[來源請求]
亚铁氰化钾无毒,在体内不会分解为氰化物。对大鼠的毒性低,致死量 (LD50) 为6400mg/kg。[12]
参见
参考資料
外部链接
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.

