
硫的同素异形体
維基百科,自由的 encyclopedia
硫有著大量的同素異形體,其數量只是僅次於碳。[1]除了有很多同素异形体,每个同素异形体通常还有各种同质异形体(相同结构的硫分子的不同晶体结构),由希腊字母前缀(α、β 等)区分。[2]
| 此條目需要擴充。 (2012年11月30日) |

此外,由于硫元素几个世纪以来一直都是一件商品,它的各种同素异形体都被赋予了传统名称。早期的工人发现了一些后来被证明是硫的单一或混合的同素异形体。某些形式以其外观命名,例如 “珍珠硫之母”,或者以在鉴定它们的方面非常杰出的化学家命名,例如 “Muthmann硫I”或“Engel硫”。[2][3]
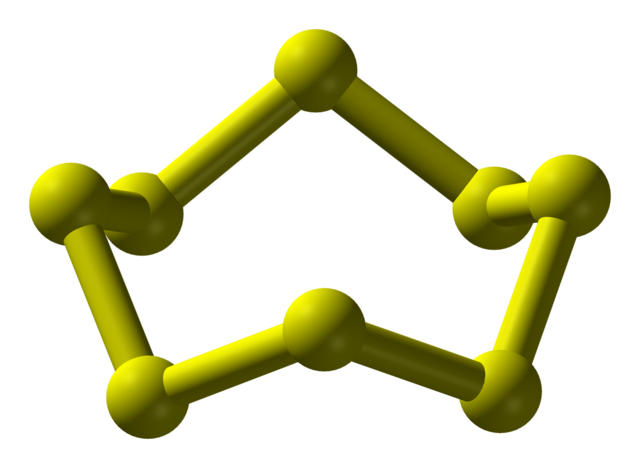
最常见的硫形式是 S
8 的正交晶系同质异形体,为褶皱环结构(见右图)。S8还有另外两种同质异形体,也具有几乎相同的分子结构。[4]除了 S8,以外,含有 6、7、9–15、18 和20个原子的硫环也是已知的。[5] 在五种高压同素异形体中,有两种有金属性。[6]
硫的同素异形体的数量反映了相对较强的S-S键,键能 265 kJ/mol。[7]此外,与大多数元素不同,硫的同素异形体可以在有机溶剂中进行处理,并且可以通过HPLC进行分析。[8]