2019冠狀病毒病疫苗
用來對抗SARS-CoV-2冠狀病毒的疫苗 来自维基百科,自由的百科全书
2019冠狀病毒病疫苗是旨在提供針對嚴重急性呼吸道症候群冠狀病毒2型(SARS-CoV-2)的獲得性免疫力的疫苗,該病毒是導致2019冠狀病毒病(COVID-19)的病毒。
在COVID-19大流行之前,關於引起嚴重急性呼吸系統症候群(SARS)和中東呼吸系統症候群(MERS)等疾病的冠狀病毒的結構和功能已經有了既定的知識體系。這些知識在2020年初加速了各種疫苗平台的開發。[1]SARS-CoV-2疫苗最初的重點是預防有症狀的、往往是嚴重的疾病。[2]2020年1月,SARS-CoV-2基因序列數據通過GISAID共享,到2020年3月,全球製藥業宣布了解決COVID-19的重大承諾。[3]2020年,第一批COVID-19疫苗被開發出來,並通過緊急授權[4]和有條件批准向公眾提供。[5][6]最初,大多數COVID-19疫苗是兩劑量的疫苗,唯一的例外是單劑量的嬌生2019冠狀病毒病疫苗。[4]然而,人們發現疫苗的免疫力會隨著時間的推移而減弱,需要人們接種加強劑量的疫苗以保持對COVID-19的免疫力。[4]
COVID-19疫苗在減少COVID-19的傳播和降低COVID-19造成的嚴重程度和死亡方面的作用被廣泛稱讚。[4][7]根據2022年6月的一項研究,從2020年12月8日至2021年12月8日,COVID-19疫苗在185個國家和地區額外防止了1440萬至1980萬例死亡。[8][9]許多國家實施了分階段分配計劃,優先考慮併發症風險最高的人群,如老年人,以及暴露和傳播風險高的人群,如醫護人員。[10][11]
疫苗概況

針對數種動物的冠狀病毒引發疾病的疫苗已經被研製,包括針對禽類傳染性支氣管炎病毒、犬冠狀病毒和貓冠狀病毒的疫苗[12]。
此前,針對可感染人類的冠狀病毒的疫苗的研製工作,主要是針對嚴重急性呼吸道症候群冠狀病毒(SARS)和中東呼吸症候群冠狀病毒(MERS)的疫苗,也有過一定進展。SARS和MERS的疫苗已經完成了動物試驗。[13][14]
截至2020年,還沒有針對SARS的對人類安全有效的治療性或保護性疫苗被研製出來[15][16]。根據2005年和2006年發表的論文,識別並研發治療SARS的新疫苗和藥物是當時世界各國政府和公共衛生機構的優先事項[17][18][19]。
同樣,目前暫時沒有針對MERS的經過試驗的疫苗[20]。當MERS正在流行時,人們認為當時已有的對SARS的研究可能為研發針對MERS的疫苗和藥物提供借鑑[15][21]。截至2020年3月,一種基於DNA的MERS疫苗已完成了人類的I期臨床試驗[22];另外三種基於病毒載體的MERS疫苗則正在進行臨床試驗,其中兩種是腺病毒載體疫苗(ChAdOx1-MERS、BVRS-GamVac),另一種則是改良牛痘病毒載體疫苗(MVA-MERS-S)[23]。
截至2021年2月,66種SARS-CoV-2候選疫苗正在進行臨床試驗,其中17種Ⅰ期臨床試驗,23種Ⅰ–Ⅱ期臨床試驗,6種Ⅱ期臨床試驗和20種Ⅲ期臨床試驗[24]。在Ⅲ期臨床試驗中,幾種COVID-19疫苗在預防症狀性COVID-19感染的效力高達95%[25]。目前有至少18種疫苗獲得至少一個政府醫藥監管機構的緊急批准:3種RNA疫苗(輝瑞-BioNTech疫苗、莫德納疫苗以及華森疫苗[26]),至少6種不活化疫苗(國藥北京生物眾愛可維、國藥武漢生物眾康可維、CoviVac、QazVac、巴拉特生物技術科瓦克辛(Covaxin)、科興疫苗以及深圳康泰疫苗[27]),4種病毒載體疫苗(「衛星V」、牛津-阿斯利康疫苗、康希諾疫苗、嬌生疫苗),以及5種蛋白質亞基疫苗(安徽智飛疫苗、EpiVacCorona、阿布達拉、高端疫苗[28]、諾瓦瓦克斯疫苗[29])。截至2022年5月19日,世界衛生組織把11款疫苗列入緊急使用清單[30]:輝瑞-BioNTech疫苗、牛津-阿斯利康疫苗及該疫苗的印度版(COVISHIELD)、嬌生疫苗、莫德納疫苗、眾愛可維(國藥北京生物)、科興生物(CoronaVac)、科瓦克辛(Covaxin)、諾瓦瓦克斯疫苗及該疫苗的印度版科沃瓦克斯(Covovax)、克威莎疫苗。[31][32][33][34] 接種COVID-19疫苗可以大大降低SARS-CoV-2傳播、感染和死亡風險。[35]
許多國家已經實施了分階段的分配計劃,優先考慮併發症風險最高的人群(例如老年人)和暴露、傳播風險較高的人群(例如醫護人員)[36]。根據國家衛生機構的官方報告,截至2021年1月8日,全球已施用1770萬劑COVID-19疫苗[37]。國藥集團估計在2021年將生產30億劑疫苗[38],阿斯利康製藥預測將生產30億劑,輝瑞公司將生產20億劑,而莫德納公司計劃將生產7-10億劑[39]。印度估計在2021年能生產35億劑新冠疫苗[40]。到2020年12月,各國已預訂購了超過100億劑疫苗[41];大約一半的疫苗由高收入國家購買,而這些國家人口僅占世界人口的14%[42]。目前,各國也在加速生產疫苗,推進群眾大力接種疫苗,疫苗接種人次在逐步上升。為使疫苗在全球普及應用,世衛牽頭的COVAX確保開發中國家及低收入國家都可獲取基本的疫苗供應[43]。
背景與時間線
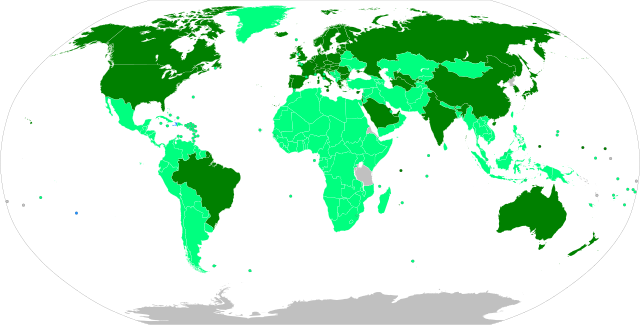
全面授權,正在進行大規模疫苗接種
緊急使用授權,正在進行大規模疫苗接種
緊急使用授權,有限的疫苗接種
全面授權,計劃大規模疫苗接種
緊急使用授權,計劃大規模疫苗接種
有待緊急使用授權
沒有數據
2019年12月1日,由SARS-CoV-2引起的一種疾病在中華人民共和國湖北省武漢市發現,早期當局隱瞞、拖延、掩蓋疫情一個月左右,並通過中國春運擴散到全中國,後於世界範圍內首次被發現,隨後通報國際社會,全球各國陸續檢測發現此病傳播已久,後來該疾病被命名為2019冠狀病毒病[44]。2020年,該疾病導致的2019冠狀病毒病疫情在世界各地蔓延,因應這場人類公共衛生史上百年一遇的大瘟疫,使得前所未有的大量資金和人力被用於研發針對該疾病的疫苗[45]。許多組織正在利用已經公開的基因序列研發SARS-CoV-2疫苗[46][47][48]。[何時?]大約有35家企業和學術機構參與到這一進程之中[49],其中3家,包括莫德納[50]、Inovio Pharmaceuticals及昆士蘭大學,得到了流行病防備創新聯盟(CEPI)的支持[51]。根據2020年3月10日的一份報告,當時全世界有約300項正在進行的前期研究[52]。
2020年3月,美國政府、醫療行業和大學向研究人員提供了訪問IBM的超級計算機以及亞馬遜、微軟和谷歌的雲計算資源的權限。這些計算資源的提供者成立了2019冠狀病毒病高性能計算聯盟,其正被用於預測疾病傳播、模擬可能的疫苗以及篩選數千種化合物以設計針對2019冠狀病毒病的疫苗或治療方案[53]。
2020年3月上旬,CEPI公布了20億美元的籌資目標,以建立一個涵蓋公共組織、私人組織、慈善組織和民間社會組織的全球合作夥伴關係,以加速2019冠狀病毒病疫苗的研發。丹麥、芬蘭、德國、挪威和英國政府承諾支持CEPI為研發2019冠狀病毒病疫苗所做的努力[54]。
2020年5月18日,中華人民共和國領導人習近平應世界衛生組織總幹事譚德塞邀請,在第73屆世界衛生大會視頻會議開幕式上發表《團結合作戰勝疫情 共同構建人類衛生健康共同體》的致辭,其中提到「中國新冠疫苗研發完成並投入使用後,將作為全球公共產品」[55]。
2020年6月4日,中華人民共和國國務院總理李克強在全球疫苗峰會視像會議致辭,表示中國將繼續支持世界衛生組織在統籌疫苗研發等方面發揮作用,亦願意為全球疫苗免疫聯盟提供捐助[56]。8月24日,李克強在湄公河合作第三次領導人會議上發言,稱中國的疫苗研製完成並投入使用後,將優先向湄公河國家提供[57]。
2020年8月11日,俄羅斯總統普丁宣布,俄羅斯完成全球第一款COVID-19疫苗[58]。但俄羅斯尚未公布候選疫苗的第Ⅰ期或第Ⅱ期臨床試驗結果,候選疫苗也尚未進入第Ⅲ期臨床試驗[59]。
2020年10月,世界衛生組織牽頭實施COVAX項目,旨在於2021年底前購入20億支COVID-19疫苗[60],並優先向開發中國家提供[61][62]。
2020年11月9日,澳洲開始生產由阿斯利康研發的2019冠狀病毒病疫苗[63]。同日,輝瑞公司及其合作夥伴BioNTech SE(BNTX)宣布所開發的疫苗有效性超過90%[64]。11月11日,俄羅斯宣布該國研發的Sputnik V疫苗有效性達到92%[65]。11月16日,莫德納宣布該公司研發的疫苗有效性達94.5%[66]。阿斯利康瓦爾牛津大學宣布兩家機構聯合研發的AZD1222疫苗有效性可達90%[67]。
2020年11月,世界衛生組織表示,全球有213種COVID-19疫苗正在被研發,其中49種疫苗進入臨床試驗階段[68]。
2020年12月2日,英國藥品及保健品管理局批准緊急使用輝瑞製藥與BioNTech合作研發的BNT162b2疫苗[69],並於12月9日展開全民接種計劃[70]。日本參議院全體會議於12月2日一致表決通過修改後的《預防接種法》,內容包括由國家承擔日本民眾接種COVID-19疫苗的費用[71]。
12月7日,中華人民共和國澳門特別行政區應變協調中心強調,特區政府預計於年底引進首批疫苗。[72]同月,中華人民共和國四川已經針對12類高風險人員開展了COVID-19疫苗緊急接種。[73]同月,莫斯科70多個站點啟動COVID-19疫苗接種工作,自願申請接種的醫護人員、教師等高風險感染人群將優先接種該疫苗,優先接種人群為醫護人員、教師等高風險感染人群。[74]4日,蕪湖開展冬春季COVID-19疫苗摸底,這次摸底是為統籌做好該市COVID-19疫苗、流感、肺炎鏈球菌肺炎等疫苗接種,建立落實多病共防機制的前期工作。[75]
2020年12月11日,美國食品藥物管理局宣布批准緊急使用輝瑞製藥與BioNTech合作研發的BNT162b2疫苗[76][77]。同月,世界衛生組織表示,雖然一些COVID-19疫苗已陸續推出並開始接種,但目前仍不清楚疫苗是否能防止人體感染SARS-CoV-2。[78]
2020年12月31日,世界衛生組織率先核准使用輝瑞製藥與BioNTech合作研發的輝瑞-BioNTech 2019冠狀病毒病疫苗[79]。同日,中華人民共和國國務院召開的疫情防控記者會上宣布,國藥集團生物新冠不活化疫苗已獲中華人民共和國國家藥監局批准附條件上市[80]。
2021年1月11日,世衛組織宣布,已有40多個國家開始接種COVID-19疫苗。[81]
2021年1月30日,嬌生公司宣佈研發的疫苗的單劑有效率為66%[82][83]。
2021年2月3日,中華人民共和國外交部發言人汪文斌宣布,中國正式加入COVAX計劃,將提供1000萬劑疫苗用於開發中國家急需[84]。
2021年2月5日,世界衛生組織總幹事譚德塞表示,全球新冠疫苗接種數量已經超過了報告的感染病例總數[85]。
2021年2月15日,世界衛生組織批准緊急使用阿斯特捷利康與牛津大學共同研發的牛津-阿斯利康2019冠狀病毒病疫苗[86][87]。
2021年2月24日,由印度血清研究所生產的60萬劑阿斯利康疫苗運抵加納首都阿克拉,加納因而成為世界衛生組織疫苗分配計劃(COVAX)的首個受益國[88]。
2021年3月8日,芬蘭研究人員研發出一款鼻噴式2019冠狀病毒病疫苗,計劃幾個月內開展臨床試驗[89]。
2021年3月12日,嬌生公司研發的嬌生2019冠狀病毒病疫苗獲得歐盟和世衛組織發出緊急使用許可[90]。這是世衛組織和歐盟首次批准使用單次接種的新冠疫苗[91]。
2021年3月31日,俄羅斯註冊了全球首個用於動物的新冠疫苗[92]。
2021年4月30日,美國莫德納公司研發的莫德納疫苗獲得世界衛生組織核准緊急使用授權,是世衛組織第五種列入緊急使用清單的新型冠狀病毒疫苗[93]。
2021年5月5日,美國政府宣布總統拜登同意臨時豁免新型冠狀病毒疫苗的專利保護,以促進疫苗的全球供應,世衛組織發言人讚揚是「里程碑時刻」,世衛組織總幹事譚德塞在推特稱美國的行動是「應對全球衛生挑戰的強有力的領導範例」[94]。
2021年5月7日,中國國藥集團研發生產的BBIBP-CorV獲得世界衛生組織核准緊急使用授權,是世界衛生組織第六種列入緊急使用清單的新型冠狀病毒疫苗。[95][96]
2021年5月14日,深圳康泰生物宣布公司研發的新型冠狀病毒不活化疫苗已獲批在中國緊急使用,已啟動開展疫苗III期臨床試驗相關工作。[97]
2021年6月1日,中國科興生物研發生產的克爾來福疫苗獲得世界衛生組織核准緊急使用授權,是世界衛生組織第七種列入緊急使用清單的新型冠狀病毒疫苗。[98][99]
2021年6月28日,輝瑞旗下動物藥廠碩騰捐贈第一批試驗性質動物用COVID-19疫苗給美國加州奧克蘭動物園,老虎、熊、美洲獅和雪貂為第一批接種對象,該園之後也會為靈長類、果蝠和豬等動物注射疫苗[100]。
2021年7月26日,由中國工程院院士、軍事科學院軍事醫學研究院研究員陳薇領銜團隊所研發的霧化吸入用重組新冠疫苗(腺病毒載體)在《刺胳針·傳染病》發表I期臨床研究數據。這是全球首個發表的新冠疫苗黏膜免疫臨床試驗結果[101]。
2021年10月11日,世衛組織疫苗顧問小組表示完成注射兩劑中國科興克爾來福或國藥眾愛可維疫苗的60歲或以上長者、中度至嚴重免疫力低下的族群,仍然有很高的受感染及演變為重症的風險,建議為這類族群在完成接種第二劑科興或國藥疫苗後的一至三個月,再追加多一劑世衛組織列入緊急使用的疫苗作為加強劑,這是世衛組織首次建議打第三針疫苗[102]。
截至2021年10月末,全球已接種了超過70億劑疫苗,其中阿聯及中國的接種率已超過八成,智利及柬埔寨的接種也接近八成水平。非洲國家均在20%以下,其中南非的接種率最高,為19%,坦尚尼亞、奈及利亞及衣索比亞只有1%的人口接種疫苗。[103]
2021年11月3日,印度研發的科瓦克辛疫苗獲世衛組織批核緊急使用授權,在完成兩劑接種兩個月後的有效率為78%[104]。
2021年11月12日,康希諾研發的全球首款吸入式腺病毒載體新冠疫苗克威莎亮相第五屆海南國際健康產業博覽會[105]。
2021年12月17日,由美國諾瓦瓦克斯醫藥開發後授權印度血清研究所生產的科沃瓦克斯獲世衛組織發出緊急使用授權[106]。
2021年12月21日,世衛組織向美國諾瓦瓦克斯醫藥原廠發出諾瓦瓦克斯2019冠狀病毒病疫苗的緊急使用授權[107]。
2022年1月25日,輝瑞和德國生物新技術公司宣布正式啟動針對變異新冠病毒奧密克戎毒株的疫苗臨床試驗。[108]
2022年4月3日,國藥集團中國生物二代重組蛋白新冠疫苗獲得國家藥品監督管理局頒發的臨床試驗批准文件。[109]
2022年5月20日,世界衛生組織對中國製造商康希諾生物研發的單劑型COVID-19疫苗克威莎核發緊急使用授權。
2022年6月30日,台灣高端生物製劑表示旗下高端新冠肺炎疫苗正參與世界衛生組織主導的團結實驗[110],並將在結果公布後向世衛組織申請核發緊急使用授權[111]。
2022年9月4日,康希諾發布公告,表示自己研發的全球首個吸入用新冠疫苗克威莎霧優在中國獲批緊急使用[112][113]。
2022年9月初,多國相繼批准針對奧密克戎BA.1或BA.4/5的新冠二價疫苗。[114]
2023年1月,康希諾開始試生產一款尚處於臨床試驗階段的疫苗,這款疫苗也是中國使用mRNA技術研發的首批疫苗之一[115]。
2023年1月19日,國藥集團中國生物復諾健生物科技針對奧密克戎變異株研發的新冠mRNA疫苗獲得國家藥品監督管理局臨床試驗批件。[116]
2024年1月10日,北京科興中維生物技術公司確認,科興生物「克爾來福」疫苗已經停產,病毒學家常榮山曾經建議不要打不活化疫苗,並說病毒流行株的抗原性變化較大,最好打mRNA疫苗、重組蛋白疫苗[117]。中國生物製藥在2024年1月15日透露,通過投資科興中維,從中收到接近60億元人民幣的分紅,當時疫苗存貨仍有大約4億支[118]。
疫苗列表
疫苗效力
接種計劃
疫苗安全、供應及相關議題
參考文獻
外部連結
參見
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
