氙(英語:Xenon;舊譯氠[10]、氥[11]、𣱧[12])是一種化學元素,化學符號為Xe,原子序數為54,原子量為7002131293000000000♠131.293 u。氙是一種無色、無味的惰性氣體。地球大氣層中含有痕量的氙。 [13]雖然氙的化學活性很低,但是它仍然能夠進行化學反應,例如形成六氟合鉑酸氙──首個被合成的惰性氣體化合物。[14][15][16]
Quick Facts 外觀, 概況 ...
氙 54Xe|
|
| 外觀 |
|---|
無色氣體,在高壓放電管中呈現紫藍色
 |
| 概況 |
|---|
| 名稱·符號·序數 | 氙(Xenon)·Xe·54 |
|---|
| 元素類別 | 惰性氣體 |
|---|
| 族·週期·區 | 18·5·p |
|---|
| 標準原子質量 | 131.293(6)[1] |
|---|
| 電子組態 | [Kr] 4d10 5s2 5p6
2, 8, 18, 18, 8
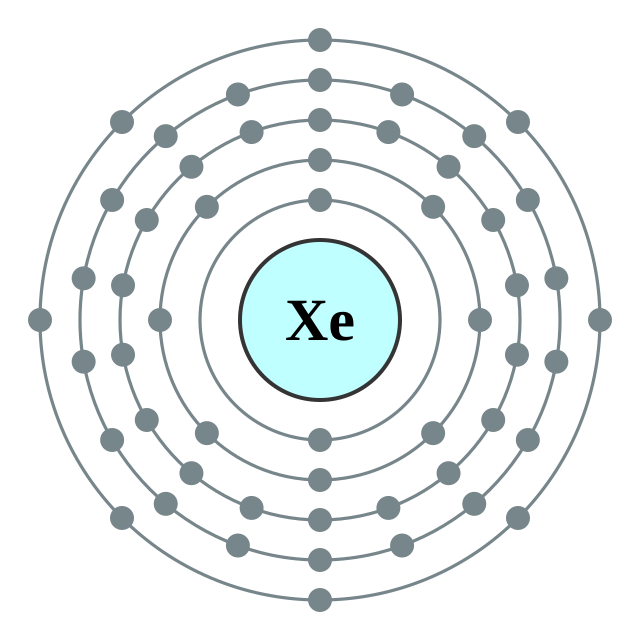 氙的電子層(2, 8, 18, 18, 8) 氙的電子層(2, 8, 18, 18, 8) |
|---|
| 歷史 |
|---|
| 發現 | 威廉·拉姆齊和莫里斯·特拉弗斯(1898年) |
|---|
| 分離 | 威廉·拉姆齊和莫里斯·特拉弗斯(1898年) |
|---|
| 物理性質 |
|---|
| 物態 | 氣態 |
|---|
| 密度 | (0 °C, 101.325 kPa)
5.894 g/L |
|---|
| 沸點時液體密度 | 3.057[2] g·cm−3 |
|---|
| 熔點 | (101.325 kPa)161.4 K,-111.7 °C,-169.1 °F |
|---|
| 沸點 | (101.325 kPa)165.03 K,-108.12 °C,-162.62 °F |
|---|
| 三相點 | 161.405 K(−112 °C),81.6[3] kPa |
|---|
| 臨界點 | 289.77 K,5.841 MPa |
|---|
| 熔化熱 | (101.325 kPa)2.27 kJ·mol−1 |
|---|
| 汽化熱 | (101.325 kPa)12.64 kJ·mol−1 |
|---|
| 比熱容 | 5R/2 = 20.786 J·mol−1·K−1 |
|---|
蒸氣壓
| 壓/Pa
|
1
|
10
|
100
|
1 k
|
10 k
|
100 k
|
| 溫/K
|
83
|
92
|
103
|
117
|
137
|
165
|
|
| 原子性質 |
|---|
| 氧化態 | 0, +1, +2, +4, +6, +8
(很少大於0)
(氧化物具弱酸性) |
|---|
| 電負度 | 2.6(鮑林標度) |
|---|
| 游離能 | 第一:1170.4 kJ·mol−1
第二:2046.4 kJ·mol−1
第三:3099.4 kJ·mol−1 |
|---|
| 共價半徑 | 140±9 pm |
|---|
| 范德華半徑 | 216 pm |
|---|
 氙的原子譜線 氙的原子譜線 |
| 雜項 |
|---|
| 晶體結構 | 面心立方 |
|---|
| 磁序 | 抗磁性[4] |
|---|
| 熱導率 | 5.65×10-3 W·m−1·K−1 |
|---|
| 聲速 | (液態)1090 m/s;(氣態)169 m·s−1 |
|---|
| CAS編號 | 7440-63-3 |
|---|
| 同位素 |
|---|
主條目:氙的同位素
|
Close
自然產生的氙由7種穩定同位素組成。氙還有40多種不穩定的放射性同位素。氙同位素的相對比例對研究太陽系早期歷史有重要的作用。[17]具放射性的氙-135是核反應爐中最重要的中子吸收劑,可通過碘-135發生負β衰變產生。[18]
氙可用在閃光燈[19]和弧燈中,[20]或作全身麻醉藥。[21]最早的準分子雷射設計以氙的二聚體分子(Xe2)作為雷射介質,[22]而早期雷射設計亦用氙閃光燈作雷射抽運。[23]氙還可以用來尋找大質量弱相互作用粒子[24],或作太空飛行器離子推力器的推進劑。[25]



