硫有著大量的同素異形體,其數量只是僅次於碳。[1]除了有很多同素異形體,每個同素異形體通常還有各種同質異形體(相同結構的硫分子的不同晶體結構),由希臘字母前綴(α、β 等)區分。[2]
此條目需要擴充。 (2012年11月30日) |

此外,由於硫元素幾個世紀以來一直都是一件商品,它的各種同素異形體都被賦予了傳統名稱。早期的工人發現了一些後來被證明是硫的單一或混合的同素異形體。某些形式以其外觀命名,例如 「珍珠硫之母」,或者以在鑑定它們的方面非常傑出的化學家命名,例如 「Muthmann硫I」或「Engel硫」。[2][3]
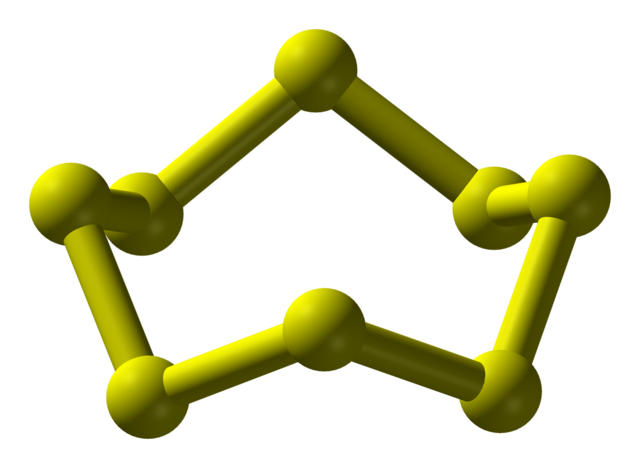
最常見的硫形式是 S
8 的正交晶系同質異形體,為褶皺環結構(見右圖)。S8還有另外兩種同質異形體,也具有幾乎相同的分子結構。[4]除了 S8,以外,含有 6、7、9–15、18 和20個原子的硫環也是已知的。[5] 在五種高壓同素異形體中,有兩種有金屬性。[6]
硫的同素異形體的數量反映了相對較強的S-S鍵,鍵能 265 kJ/mol。[7]此外,與大多數元素不同,硫的同素異形體可以在有機溶劑中進行處理,並且可以通過HPLC進行分析。[8]
氣態同素異形體
二硫為硫的雙原子分子。在720°C,硫主要以二硫存在。在530°C、低壓(1毫米水銀)的環境中,硫蒸氣佔99%是二硫。火焰中產生的S2分子使硫燃燒時呈藍色。[1]
在硫蒸汽存在。根據理論計算的最新觀點認為四硫有著環狀結構。[9]
尚未分離,只在硫蒸汽偵測到。[10]
固體環狀結構
S6的晶形為菱面體,為橙紅色固體,首次透過下列反應發現於1891年。
這是由含S6和S10的二硫化碳中之溶液製備所得。
為亮黃色固體,有α、β、γ、δ四種結構。環七硫的環有著不尋常幅度的鍵長(199.3–218.1 pm),因此被認為是最不穩定的同素異形體。

α-硫是硫自然界中最常見的形式,[1]其純淨時的顏色是黃綠色(市面上出售的硫因為有著微量的環七硫而呈現更黃的顏色)。α-硫實際上不溶於水,導熱性能差,為一良好的電絕緣體。此是硫由二硫化碳結晶而得之緊密的黃色晶體,融點112.8度。
融化硫於部分凝固後,倒出多餘液體,剩下無數之針形晶體即為單斜硫,融點119.2度。
為沸騰之硫注入冷水所得之軟黏體,有彈性。
發現於1890年,為融化硫由二硫化碳緩慢結晶而成。

這些同素異形體是由多種方法合成,例如 可以透過二氯化硫(Sn-mCl2)和H2Sm反應,即
Sn−mCl2 + H2Sm → cyclo-Sn+2 HCl[1]
製取。S12、S18、S20可以由S8製得,其中S12是繼S8後最穩定的環狀同素異形體。S9有4種形式,S18則有2種。
固體連鎖硫結構
生產純淨的連鎖硫已被證明是極其困難的。
亦稱「纖維硫」或ω1-硫[10],其密度為2.01 g·cm−3,會在其融點104°C附近分解。
亦稱ω2-硫。
連續硫形式
這是硫在160°C以上時融解的淬火產物。
此為融化後熔融的硫的名字,冷卻此主要給出β-硫。[10]
把硫加熱至170°C可形成S∞。
參考資料
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
