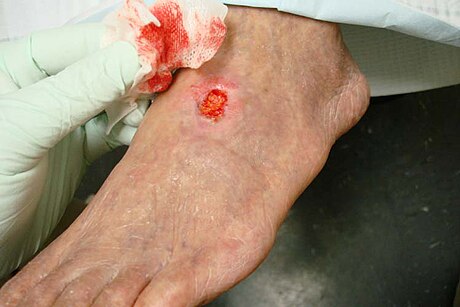
周边动脉疾病(Peripheral artery disease, PAD),可以称为周边血管疾病(Peripheral vascular disease, PVD)、周边动脉阻塞性疾病(Peripheral artery occlusive disease, PAOD),或是周边闭塞性动脉病变(Peripheral obliterative arteriopathy, POA),是一种供应大脑和心脏以外之动脉的窄化现象[1],多数情况会影响患者的双腿[2]。典型的症状是走路时脚痛,但这种症状在休息时便可改善[3]。其他症状包括:皮肤溃疡、皮肤偏蓝、冰冷,或是患肢的指甲和毛发生长较差[4]。并发症可能包括感染或坏疽,可能会导致截肢、冠状动脉疾病或中风[2],不过有将近一半的病患是没有症状的[3]。
周边动脉阻塞最主要的危险因子是吸烟[2]。其他危险因子包括糖尿病、高血压 和高胆固醇[5]。其潜在的致病机转通常是动脉粥样硬化,如果硬化的斑块脱落将会导致动脉的完全阻塞[6],其他原因包含动脉痉挛[1]。周边动脉阻塞通常借由发现踝肱指数(Ankle-brachial index, ABI)低于0.90而确诊,踝肱指数的公式是脚踝的收缩压除以手臂的收缩压[7],血管摄影是更准确的诊断方法,不过它具有一定的风险[7]。
目前筛检的效果仍待进一步研究[8][9],对于周边动脉阻塞的病患,戒烟和运动疗法能够改善[10][11]。药物治疗包括HMG-CoA还原酶抑制剂(Statin)、ACE抑制剂和西洛他唑 都会有帮助[11][12],阿司匹林对于轻症患者没有显著帮助,但通常会建议较严重的患者使用[13][14],华法林并没有特别效益[15]。一些用来治疗周边动脉阻塞的手术包括冠状动脉旁路移植、血管再成形术和旋切术[16]。
2010年全世界有将近2.02亿人有周边动脉阻塞的疾病[5]。在发达国家,周边动脉阻塞在45至50岁的民众中占了5.3%,85至90岁中占了18.6%[5];而在发展中国家,45至50岁的民众中占了4.6%,85至90岁中占了15%[5]。在发达国家,男女罹病的比例相当;但在发展中国家则是女性较容易罹病[5]。 在1990年,周边动脉阻塞造成近16,000的死亡;在2013年,周边动脉阻塞造成的死亡数更高达近41,000人[17]。
病理机制
周边动脉疾病泛指周边动脉血液循环系统的阻塞,导致与血液灌流不足有关的病理变化[18]。而周边动脉疾病好发于下肢周边的动脉循环系统,且最常影响骨骼肌的血液灌流,导致骨骼肌长期处于血氧供给不足的代谢环境,使骨骼肌慢性病变,因此周边动脉疾病的进展常是缓慢且渐进式的,而这也与其动脉粥状硬化疾病进展有关。
引起动脉粥状硬化的风险因子有很多,用以阐述其进展机制的理论也很多,引用目前最广为科学界所接受的损伤反应假说[19](response-to-injury hypothesis of atherosclerosis)。该假说认为动脉粥状硬化的起始点便是内皮细胞的长期损伤,引起的慢性发炎反应所导致的结果。而导致内皮细胞损伤的原因可能是物理性的。例如直接的创伤、血压长期升高导致的损伤、动脉分支处容易产生涡流引起的伤害;也有可能与血液环境物质对内皮细胞的暴露有关。例如血液中氧化物质的引起的损伤、慢性的高血糖或高血脂或是血液中容易对内皮细胞产生损伤的有害物质与代谢产物,像是同半胱胺酸等。皆有可能是引起血管内皮细胞长期处于损伤状态的可能性,而血管组织侦测到内皮细胞的损伤,便会释放发炎物质,例如Tumor Necrosis Factor alpha(TNF-α)会改变血管内皮的基因表现,增加其Vascular Cell Adhesion Molecule type 1(VCAM-1)的表现量,单核球与T淋巴球会辨识VCAM-1,与趋化因子的共同介导下,进入损伤的内皮细胞中,引发进一步的发炎反应。
长期处于发炎环境中的内皮细胞,其基因的表现与调节便会失灵,内皮细胞维持血液层流(laminar flow)与调节血管物质交换的功能也会受到影响,使得Low Density Lipoprotein(LDL)有较高的机会被氧化,例如被nitrogen oxide(NO)、巨噬细胞、脂氧合酶(lipoxygenase)等氧化,形成氧化态的LDL,氧化态的LDL会被巨噬细胞所吞噬,但是无法被巨噬细胞所分解,巨噬细胞进而凋亡形成泡沫细胞(foam cell)甚至胆固醇结晶(cholesterol crystal),堆积在血管内膜当中(tunica intima)。
此外,血管内皮细胞的损伤也会曝露组织凝血致活酶(tissue thromboplastin),提高外在路径的凝血反应机会,引起血栓的病理变化;而产生血栓过程中,血小板也会释放血小板衍生生长因子(platelet-derived growth factor)与发炎反应中巨噬细胞分泌的纤维母细胞生长因子(fibroblast growth factor)和TNF-α,皆会促进血管内膜的平滑肌增生与细胞外基质(extra-cellular matrix)的堆积,形成血管内膜增厚(intima thicken)的病理变化,在巨观结构上便能观察到动脉硬化斑(fatty streak)的解剖变化。
综上所述,从血管内皮细胞的损伤所引起的一连串慢性发炎的反应,与外在路径的凝血反应参与,到最后形成动脉硬化斑的病理变化,是周边动脉疾病因周边动脉血管阻塞,导致细胞组织灌流不足的最广为接受的病理机制,因此当今临床的药物治疗上,会运用抗血栓药物进行治疗,也是根基于干预这一连串的病理反应路径为立论基础。但在治疗之前,我们可以先针对周边动脉疾病的风险因子进行预防。
风险因子
如上病理机制中所提及,周边动脉疾病与动脉粥状硬化的发生息息相关,因此减少动脉粥状硬化的风险因子,相对也能减少周边动脉疾病的风险。而周边动脉疾病的风险因子在临床上主要分为不可缓和(nonmodifiable)与可缓和(modifiable)两大类。[20]
不可缓和的风险因子主要与先天的基因表现有关,像是常见于家族性的高胆固醇血脂症,提高LDL被氧化的几率,增加动脉粥状硬化发生的风险,另外先天性的血管异常疾病,因无法有效调节血液层流的理想生理状态,进而增加血管内皮受损的几率,也会提高动脉粥状硬化发生的风险;此外不可缓和的风险因子也与年纪有关,年纪越高发生周边动脉疾病的比率也提高,这也与血管随着年纪增加损伤的机制有关;最后,周边动脉血管疾病男性发生率较女性为高,虽机制仍待探索,但认为很可能就是性别因素背后的贺尔蒙差异引起的差别所致。
可缓和的风险因子像是高血脂与高血糖皆有药物可进行适当的控制,此外目前最常使用的药物便是抗凝血药物,进而阻断动脉粥状硬化有外在凝血路径参与的机制,此外减少氧化物质与容易引起发炎反应物质的暴露,也能有效减少周边动脉疾病的发生几率。
由上所知,我们可以在日常生活中,降低可缓和的风险因子,减少周边动脉疾病的发生率,面对不可缓和的风险因子,以公共卫生的角度来看,也应提高有较高发生率族群的警觉性,发展预防医学的策略;而当今治疗周边动脉疾病偏向以抗凝血药物为主,实与流行病学的大数据基础下,所论证得出的指导原则(guideline)有关。根据美国心脏协会与美国心脏学会在2016年的指导原则(American College of Cardiology/American Heart Association (ACC/AHA) [18]Guideline)所提及,确定患有周边动脉疾病,且有明显周边动脉疾病症状的族群,有显著性较高的几率发生重大不良心脏事件(Major Adverse Cardiac Event)与重大不良下肢事件(Major Adverse Limb Event)的几率提高很多[2],而周边动脉疾病与重大不良心脏事件或是重大不良下肢事件,在病理机制的共通点,便是血小板的凝集活性上升与凝血活性上升,且重大不良心脏事件与重大不良下肢事件的对人体的伤害也比较高,因此在周边动脉疾病的病人治疗分针上,偏向于避免重大不良心脏事件与重大不良下肢事件为主,而采取抗凝血或抗血小板的治疗药物为主。
治疗策略
周边动脉疾病的治疗策略上所述,最主要便是避免对人体有较大伤害的重大不良心脏事件与重大不良下肢事件的发生,而不同程度病理发展的病患,在治疗策略上也稍有不同,因此临床上将患有周边动脉疾病的病人分为有症状表现或无症状表现,与有心血管疾病史或无心血管疾病史两大分类指标,如下表四共分为四个群体[21],且根据生物统计学上的论证基础,各有不同的治疗策略。
表一:AHA/ACC guideline于周边动脉疾病的分类
| 无心血管疾病史 | 非急性心血管疾病史 | |
| 无症状表现的周边动脉疾病 | 群体一(group1)
降低心血管疾病的风险因子为主。 |
群体二(group2)
避免心血管疾病的复发,建议服用P2Y12抑制剂 |
| 有症状表现的周边动脉疾病 | 群体三(group3)
药物治疗预防主要不良心脏与下肢事件,建议服用P2Y12抑制剂。 |
群体四(group4)
避免心血管疾病的复发,建议服用P2Y12抑制剂,并适量使用其他抗凝血剂 |
群体一有周边动脉疾病却无症状表现,也无心血管病史的病患。该群体的病患属于较早期的周边动脉疾病,通常以降低动脉粥状硬化可缓和的风险因子为主要的治疗策略,以避免重大不良心脏与下肢事件发生为主。例如血糖与血脂的控制与降低引起内皮细胞损伤因子的暴露为主,且因为抗凝血药物的治疗在临床试验上并无显著性[22],因此在指导原则上并无建议进行抗凝血药物的治疗。
群体二为有周边动脉疾病且无明显症状,但有心血管疾病史,此群体病患主要以避免心血管疾病的复发,例如稳定型心绞痛的治疗为主。因此建议服用抗凝血药物,例如Clopidogrel[23],需要经过CYP450酵素代谢唯有活性的代谢物质,再有选择性且不可逆的结合在血小板的P2Y12受器上,抑制了adenosine diphosphate (ADP)结合在P2Y12受器上的位点,也抑制了glycoprotein GPIIb/IIIa complex的活化,进而抑制血小板的凝集,达到抗凝血的效果。
群体三为有周边动脉疾病且有明显症状,但无心血管疾病史。此类病人因为周边动脉疾病进展较为后期,且有明显症状,所以其发生主要不良心脏或下肢事件的几率也大幅提高,因此主要的治疗策略为降低主要不良心脏或下肢事件的发生,而建议抗凝血治疗,例如P2Y12受器的抑制剂—Clopidogrel、Ticagrelor。Ticagrelor与Clopidogrel在机转上不同之处为其是有选择性且可逆的结合在血小板的P2Y12受器上,与Clopidogrel为不可逆的结合在血小板的P2Y12受器上有些许不同,但在 Examining Use of Ticagrelor in Peripheral Artery Disease (EUCLID) trial中发现,Ticagrelor与Clopidogrel在周边动脉疾病的治疗上有类似的效果[24],因此认为Ticagrelor可做为Clopidogrel的替代用药。
群体四为有周边动脉疾病且有明显症状,且有非急性心血管疾病史。该群体的病患发生主要不良心脏或下肢事件的几率是所有群体中最高的,因此在治疗上也是偏向以避免主要不良心脏或下肢事件的复发为主要策略,而采用抗凝血药物的治疗,但在临床试验上[25],发现使用两种以上抗凝血药物效果并不比单用一种抗凝血药物来得好,而且还会增加出血副作用的发生率,因此建议单用Aspirin或P2Y12受器的抑制剂。
目前仍有两种在试验中的药物Rivaroxaban与Vorapaxar。Rivaroxaban有很高的选择性能竞争性抑制凝血因子Xa,根据Cardiovascular Outcomes for People Using Anticoagulation Strategies(COMPASS) trial[26],该试验将有症状的周边动脉疾病且有稳定型心绞痛的病患分为三组。第一组为每天服用两次2.5mg的Rivaroxaban和aspirin;第二组为每天服用两次5mg的Rivaroxaban;第三组为每天服用aspirin。结果发现第一组比第三组能显著降低主要不良心脏与下肢疾病,但是第一组却会增加消化道出血的机会,与小幅增加脑出血的机会,因此Rivaroxaban使用在周边动脉疾病的治疗上仍未受到美国FDA(Food and Drug Administration)的认可。
而Vorapaxar[27]能竞争性抑制血小板的Protease-Activated Receptor-1(PAR-1),而PAR-1与thrombin引起了血小板凝集有关,因此抑制PAR-1能降低血小板的凝集,而根据2013年Vorapaxar in patients with peripheral artery diseas的临床试验,发现Vorapaxar并不能显著性降低主要不良心脏事件,但是能显著性降低主要不良下肢事件,而且Vorapaxar能显著性提高周边血管的新生,因此Vorapaxar也许能成为未来治疗主要不良下肢事件的新药物。
而目前也有心脏细胞的研究[28],发现Vascular Endothelial Growth Factor(VEGF)能增加,间充质干细胞的存活率(mesenchymal stem cells),也许能用在未来心肌梗塞细胞治疗的应用基础上。而也期待未来在更加理解无论是动脉粥状硬化的机制,抑或是血液凝结的细节,或是更多有关血管新生的分子环境,都能成为未来在治疗上更加精准的标的,也更加精准且人性化的医疗。
参考资料
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.