Loading AI tools
锑化合物是化学元素锑(Sb)所形成的化合物。在锑化合物中,锑主要呈现+3和+5价,其+3价的阳离子在水中水解,一般以SbO+
的形式存在,而不是Sb3+
。[1]


锑可以形成+3价和+5价的卤化物。+3价的四种卤化物均是已知的,除三碘化锑为红色晶体外,其余均为无色晶体。[1]三氟化锑是一种氟化剂,其活性比三氟化砷强,可由三氧化二锑和氟化氢反应得到:[2]
- Sb2O3 + 6 HF → 2 SbF3 + 3 H2O
它可用于制备有机氟化物。其余三卤化锑可由金属锑和相应的卤素反应得到。
- 2 Sb + 3 X2 → 2 SbX3 (X=Cl、Br或I)
浓盐酸和硫化锑反应也能得到得到三氯化锑,它可以通过重结晶或蒸馏[3]来提纯。三氯化锑可以溶解很多氯化物,得到导电的溶液。[2]
三卤化锑在水溶液中可以强烈水解,生成难溶于水的卤氧化物:[1]
- SbX3 + H2O → SbOX↓ + 2HX (X=卤素)
除了SbOX外,还会生成Sb4O5X2等其它含氧物种。[4]
氯氧化锑由三氯化锑水解得到,白色的水解产物可以溶于酒石酸或硫代硫酸钠,形成[SbO(C4H4O6)]−和[Sb(S2O3)3]3−而溶解。将三氯化锑溶于较浓的盐酸,形成氯锑酸盐而抑制SbOCl沉淀的生成。它和强还原剂反应,放出剧毒的锑化氢:[2]
- 3 H+ + SbCl4− + 3 Zn → SbH3↑ + 3 Zn2+ + 4 Cl−
较弱的还原剂只会使反应产物停留在单质锑:
- 2 SbCl4− + 3 Fe → 2 Sb↓ + 3 Fe2+ + 8 Cl−
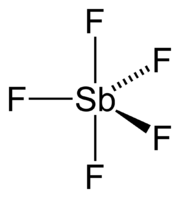
五卤化锑是低熔点的化合物。五氟化锑可由五氯化锑和氟化氢反应,或三氟化锑和氟气反应得到:[5]
- SbCl5 + 5 HF → SbF5 + 5 HCl
- SbF3 + F2 → SbF5
五氯化锑可由三氯化锑的进一步氯化得到。
- SbCl3 + Cl2 → SbCl5
这两种卤化物都能形成六卤配离子SbX−
6。三氯化锑在氯化铯的存在下被氯气部分氧化,生成深蓝色的Cs2SbCl6,其结构与黑色的(NH4)2SbBr6类似,由[SbX6]3−和[SbX6]−构成。[6]
锑和氧气反应得到三氧化二锑(Sb4O6),它以二聚体的形式存在。简单的分子Sb2O3只有在高温下存在。三氧化二锑溶于浓酸或有配位性的酸,形成相应的盐或配离子,如溶于硫酸生成硫酸锑(Sb2(SO4)3);它也能溶于碱形成亚锑酸盐。氢氧化锑(Sb(OH)3)是未知的,目前仅已知Sb2O3·xH2O这一水合物。[7]
五氧化二锑(Sb4O10)可由五氯化锑的水解得到。[8]其胶体可由三氧化二锑和过氧化氢反应得到:[9]
- Sb4O6 + 4H2O2 ⇌ Sb4O10 + 4 H2O
在硫酸介质中,过硫酸铵氧化三氧化二锑也能得到五氧化二锑。[10]五氧化二锑的酸性比三氧化二锑强,可溶于碱形成锑酸盐。在工业上以五氯化锑制备锑酸盐,为使碱的用量减少而节约成本,会先将氯化物水解,再用氢氧化钠进行反应。[11]将三氧化二锑溶于氢氧化钠得到的亚锑酸盐用过氧化氢氧化,也是工业上制备锑酸盐的方法之一。[12]六羟基合锑酸钾(K[Sb(OH)6])在强碱性的条件下可以将钠离子沉淀。[13]


锑的硫化物在自然界中以辉锑矿的形式存在。硫化锑可溶于碱金属硫化物溶液[14]或氢氧化物溶液[7]:
- Sb
2S
3 + 3 S2−
→ 2 SbS3−
3 - 2 Sb
2S
3 + 4 OH−
→ SbO−
2 + SbS−
2 + 2 H
2O - Sb
2S
3 + 6 OH−
→ SbO3−
3 + SbS3−
3 + 3 H
2O
形成的硫代亚锑酸盐在酸的存在下又会沉淀出硫化锑。硫代锑酸锑(SbSbS4)可用作润滑添加剂。[15]硒化锑可由锑和硒的单质直接反应得到[16],它可用作光学材料[17],如用于太阳能电池中。[18] 硫化锑和氯化亚铜、三氯化铝在离子液体中反应,可以得到橙红色的[Cu(Sb2S3)][AlCl4]晶体。[19]
- Sb2S3 + CuCl + AlCl3 → [Cu(Sb2S3)][AlCl4]

碲化锑也可由相似的元素化合反应制备[20],或以三氯化锑、亚碲酸钠为原料,由还原剂硼氢化钠还原制得。[21]混合硫属化物(如Sb2Te2Se)是已知的,[22]可由单质在高温下按化学计量比反应得到。[23]