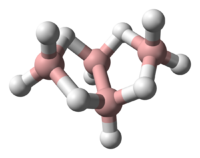
丁硼烷,更準確地說是丁硼烷(10)或網式丁硼烷,是第一種獲得分類(斯多克和馬塞內茨,1912年)及分離出來(阿爾弗雷德·霍克)的硼烷。它的沸點相對較低,只有18°C,在室溫下沸騰。丁硼烷有毒並有惡臭味。丁硼烷的熱穩定性較差。[2]
物理性質
丁硼烷又叫「四硼烷」,沸點在1.0133bar下(1bar=105Pa)為13℃,在0.516Pa下為0℃。密度為0.56g/cm3(-25℃,液態)和0.70g/cm3(固態)。[2]
丁硼烷在水中的溶解度很小,可飄浮在冷水中緩慢地水解,但不如乙硼烷那樣容易水解。丁硼烷可任意溶解在C6H6和CS2中。[2]
安全
因為它很容易被空氣氧化,所以必須儲存在真空中。丁硼烷與空氣、氧氣或硝酸接觸即會燃燒。包括丁硼烷在內的幾乎所有硼烷被認為有劇毒,並對生物體有強烈的損害。一項使用兔子和老鼠的毒性丁硼烷研究證實了這一點。[3]
製備
- 硼化錳的水解是最早獲得較高產率(14%)丁硼烷的反應之一。硼化錳酸解時最有效的酸是磷酸,而不是酸性更強的鹽酸和硫酸。鹵化硼在金屬氫化物存在下的高溫加氫還原也可獲得丁硼烷。[4]
- 丁硼烷可以通過熱解乙硼烷的方法製備[2] :
- 2 B2H6 → B4H10 + H2
- 也可以在大量氫氣中,與100℃和五硼烷-11(B5H11)反應10分鐘得到[2] :
- B5H11 + H2(大量) → B4H10 + 1/2 B2H6
- 還有一種方法,通過金屬鈉和碘代乙硼烷的反應製備:
- 2 B2H5I + 2 Na → B4H10 + 2 NaI [2]
參考資料
外部連結
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.