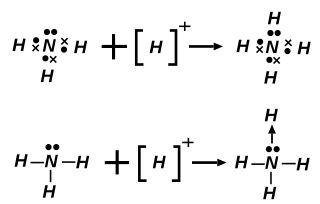配位鍵(英語:Coordinate Covalent Bond,又稱配位共價鍵,或簡稱配鍵),是一種特殊的共價鍵。當共價鍵中共用的電子對是由其中一原子獨自供應時,就稱配位鍵。配位鍵形成後,與一般共價鍵無異。
相關概念
形成條件
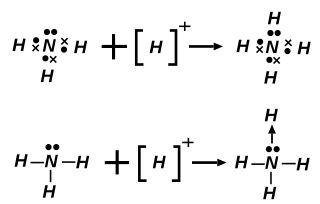 銨離子中的配位鍵
銨離子中的配位鍵
配位鍵的形成需要兩個條件:
- 一是中心原子或離子,它必須有能接受電子對的空軌域;
- 二是配位體,組成y配位體的原子必須能提供配對的孤對電子(L.P)。
當一個路易士鹼供應電子對給路易士酸而形成化合物時,配位鍵就形成。
例如:
氣態氨  和 氣體三氟化硼
和 氣體三氟化硼  形成固體
形成固體 



化合價
在配位化合物中,由電負性小的元素原子向電負性大的元素原子提供孤對電子形成配位鍵時,每個有一對孤對電子的前者(電負性小的原子)顯示+2價,後者顯示-2價。反之,由電負性大的元素原子提供孤對電子與電負性小的元素原子之間形成配位鍵時,兩種元素都無價態變化。
常見配位鍵化合物
- 一氧化碳
 ,其中碳氧間的三對共用電子對有一配位鍵,兩個正常共價鍵。
,其中碳氧間的三對共用電子對有一配位鍵,兩個正常共價鍵。
- 銨根
 ,其中N原子與左下右的
,其中N原子與左下右的 原子以極性鍵結合,並與上方的
原子以極性鍵結合,並與上方的 以配位鍵結合,由
以配位鍵結合,由 原子提供一對價電子。
原子提供一對價電子。
- 水合氫離子