甲酸鋰是鋰的甲酸鹽。它以化學計量組成LiCOOH·H2O的白色晶體形式以一水合物形式銷售。[3]
| 甲酸鋰 | |||
|---|---|---|---|
| |||
| 識別 | |||
| CAS號 | 556-63-8(無水物) 6108-23-2(一水合物) | ||
| PubChem | 23680280 | ||
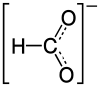
| SMILES |
| ||
| 性質 | |||
| 化學式 | CHLiO2 | ||
| 摩爾質量 | 51.97 g·mol−1 69.97 (一水合物) g·mol⁻¹ | ||
| 外觀 | 白色晶體[1] | ||
| 密度 | 1.46 g·cm−3 (20 °C)[1] (一水合物) | ||
| 熔點 | 93-95 °C(366-368 K)(一水合物[1]) 279~280 °C(無水,熔化略帶分解)[2]() | ||
| 溶解性(水) | 易溶於水 [1] | ||
| 相關物質 | |||
| 其他陰離子 | 乙酸鋰 | ||
| 其他陽離子 | 甲酸鈉 甲酸鉀 甲酸銣 甲酸銫 | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
製備
性質
甲酸鋰的晶體結構為正交晶系[5] ,空間群Pna21,晶格參數為a = 699 pm, b = 650 pm 和 c = 485 pm。[6]
甲酸鋰的一水合物會在 94 °C 時失水,形成無水合物。[7] 把無水甲酸鋰加熱到 230 °C[6] 時,會分解成碳酸鋰、一氧化碳和氫氣。[4]
危險性
參考資料
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.



![{\displaystyle {\ce {2HCOOLi ->[\Delta] Li2CO3 + CO ^ + H2 ^}}}](http://wikimedia.org/api/rest_v1/media/math/render/svg/dd2481d55ca822cfb281260e5b48ec4ef1fd436e)