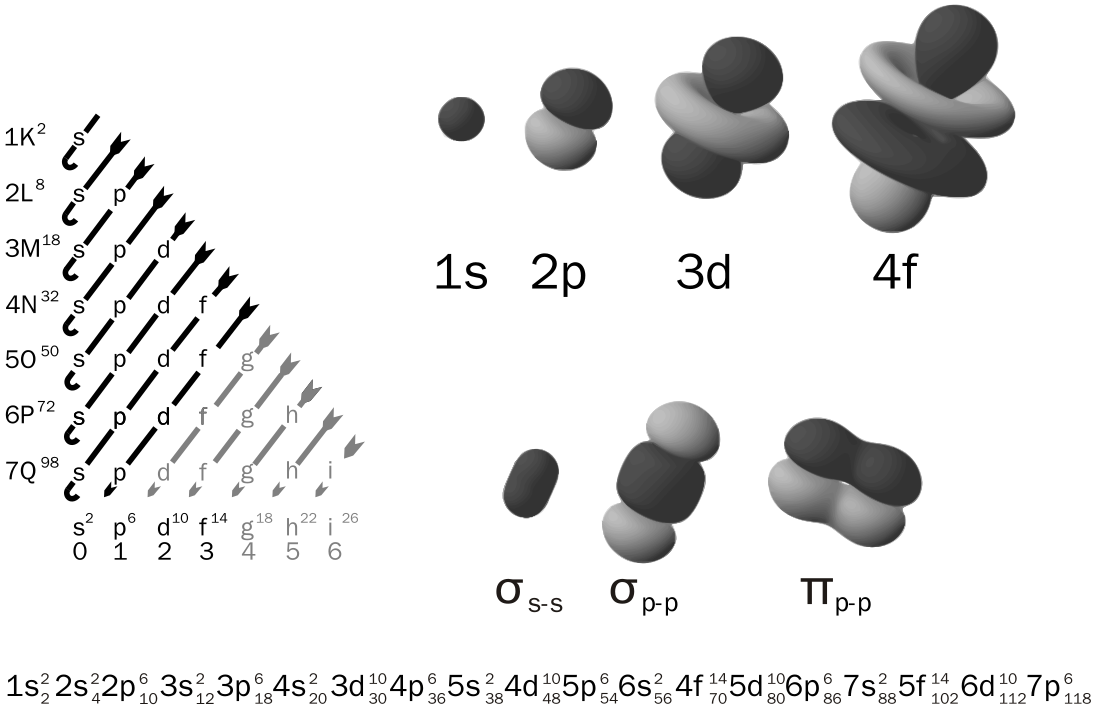
電子排佈(英語:electron configuration),或稱電子排序、電子構型,指電子在原子、分子或其他物理結構中的原子軌域或分子軌域上的排序及排列形態[2]。
此條目需要補充更多來源。 (2023年1月12日) |
| 「電子排佈」的各地常用名稱 | |
|---|---|
| 中國大陸 | 電子排布、電子構型 |
| 臺灣 | 電子組態[1] |
| 港澳 | 電子排佈 |


與其他基本粒子相同,電子遵從量子物理學而非經典物理學,因此具有波粒二象性。而且,根據量子物理學中的哥本哈根詮釋,任一特定電子在被偵測到前,它的確實位置是不確定的(軌域及軌跡放到一旁不計)。在空間中,該測量將會檢測的電子在某一特定點的概率,和在這一點上的波函數的絕對值的平方成正比。
電子能夠由發射或吸收一個量子的能量從一個能級躍遷到另一個能級,其能量傳輸的形式為吸收或釋放光子。由於包立不相容原理,沒有兩個以上的電子可以存在於某個原子軌域(軌域不等於電子層);因而一個電子只可跨越到另有空缺位置的軌域。
原子的電子構型可以反映出元素週期表中的元素的結構。這一概念有時用於也描述約束原子的多個化學鍵。在塊體材料的研究中這一理念可以說明激光器和半導體的奇特性能。
原子軌域的種類
根據薛定諤方程,原子軌域的種類取決於主量子數(n)、角量子數(l)和磁量子數(ml)。其中,主量子數就相當於電子層,角量子數相當於亞層,而磁量子數決定了原子軌域的伸展方向。另外,每個原子軌域里都可以填充兩個電子,所以對於電子,需要再加一個自旋磁量子數(ms),一共四個量子數。
n 可以取任意正整數。在 n 取一定值後,l 可以取小於 n 的自然數,ml 可以取 -l 到 +l。不論什麼軌域,ms 都只能取±1/2,兩個電子自旋相反。因此,s軌域(l=0)上只能填充2個電子,p軌域(l=1)上能填充6個,一個軌域填充的電子數為4l+2。
具有角量子數0、1、2、3的軌域分別叫做s軌域、p軌域、d軌域、f軌域。之後的軌域名稱,按字母順序排列(跳過j),如角量子數l=4時叫g軌域。
排佈規則
電子的排佈遵循以下規則:
- 構築原理:原子會選擇能量最低的構建方式。一般而言,新填入的電子都填在能量最低的空軌道上。
- 洪特規則:電子盡可能的佔據不同軌道,且自旋方向相同。整個原子的能量才處於最低。
- 包立不相容原理:在同一體系中,不存在四個量子數完全相同的電子。
- 能級交錯:電子層數較大的某些軌域的能量反低於電子層數較小的某些軌域能量的現象。
| 1s | ||||
| 2s | 2p | |||
| 3s | 3p | |||
| 4s | 3d | 4p | ||
| 5s | 4d | 5p | ||
| 6s | 4f | 5d | 6p | |
| 7s | 5f | 6d | 7p | |
| 8s | 5g | 6f | 7d | 8p |
有些原子的排佈不完全遵守上面的規則,如:
這是因為同一亞層中,全充滿、半充滿、全空的狀態是最穩定的。這種方式的整體能量比3d44s2要低,因為所有亞層均處於穩定狀態。
以鉻為例:
電子構型對性質的影響
電子的排佈情況,即「電子構型」,是元素性質的決定性因素。為了達到全充滿、半充滿、全空的穩定狀態,不同的原子選擇不同的方式。具有同樣價電子構型的原子,理論上得或失電子的趨勢是相同的,這就是同一族元素性質相近的原因;同一族元素中,由於週期越高,價電子的能量就越高,就越容易失去。
元素週期表中的區塊是根據價電子構型的顯著區別劃分的。不同區的元素性質差別同樣顯著:如s區元素只能形成簡單的離子,而d區的過渡金屬可以形成配合物。
參見
參考資料
外部連結
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.