淋巴絲蟲病
由絲蟲引起的疾病 来自维基百科,自由的百科全书
淋巴絲蟲病是由絲蟲等寄生蟲引起的疾病,[2]患者通常在兒童時期感染。大多數感染者無症狀,但部分感染者會出現象皮病,會讓其手臂、腿、乳房或生殖器嚴重腫脹並導致疼痛。[3][4]
世界各地超過1億人受淋巴絲蟲病感染,是導致永久性殘疾的主因。受此影響的人往往無法工作,且常因毀容和殘疾而被排斥。 [4]
淋巴絲蟲病是首個被發現由蚊子傳播的疾病,[5]絲蟲可以透過受到感染的蚊子叮咬他人而散播。目前已知班氏絲蟲、馬來絲蟲與帝汶絲蟲可感染人類,當中以班氏絲蟲最常見。絲蟲進入人體後會在淋巴管內築巢並破壞淋巴系統,它們可以在人體內存活8年,同時繁殖數百萬後代,幼蟲會以血液在人體內循環。[6]醫生會在晚上採集疑似受感染者的血液,血液經吉姆薩染液染色後再以血液抹片於顯微鏡下觀察是否受感染,也可以檢驗血清中是否含有抗體以診斷。[7]
該疾病可以透過大規模驅蟲防治,通常會給予阿苯達唑、伊維菌素和乙胺嗪等驅蟲藥之組合,持續6年直至再無人受感染。 [8]防止蚊蟲叮咬也是預防手段之一,包括減少蚊子數量和使用蚊帳。 [9]
截至2022年,全球47個國家共有約4000萬人感染,約8.63億人面臨患病風險。 它在熱帶非洲和亞洲最為常見。 淋巴絲蟲病被列為被忽視的熱帶疾病、也是四種主要蠕蟲病之一。 [7]該疾病每年造成數十億美元的經濟損失。 [9]
體徵和症狀

大多數感染淋巴絲蟲病患者不會出現症狀,[10]但部分患者的淋巴管會受損害,這可以透過醫學超聲波檢查出來。[9]在感染數月至數年後,蠕蟲會死亡,引發免疫反應,導致發燒和淋巴結腫大及疼痛(通常是腹股溝淋巴結)。[9][10]在淋巴絲蟲病流行地區,患者通常在兒童時期感染,並在青春期出現症狀。[9]
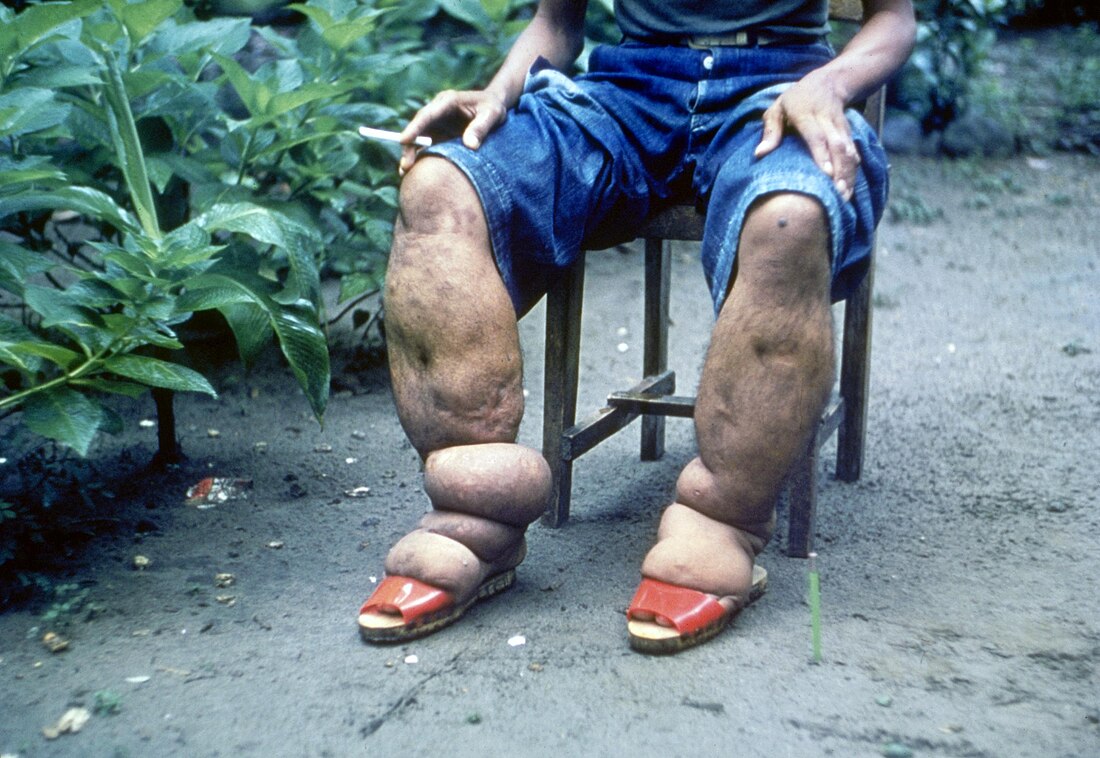
一部分患者的淋巴管會持續受到損害,讓血管無法讓淋巴液循環,導致淋巴液在手臂、腿、乳房或陰囊等地聚集並出現淋巴水腫;負責運輸免疫細胞的淋巴功能喪失,導致反覆遭受各種感染。[11]在感染、發炎與淋巴管受損下,患者的肢體會極度腫脹,周圍皮膚變厚、乾燥、變色,並佈滿疣狀腫塊,其中含有曲折的淋巴管環。 [11]
即使沒有淋巴損害,有些患者仍可能對毛細血管內的線蟲幼蟲產生過敏反應,稱為熱帶性肺部嗜酸性白血球增生。這些患者會出現夜間咳嗽、疲勞和體重下降。隨着時間推移,肺部可能受損,導致限制性肺病(肺活量下降)。[12]
病因

淋巴絲蟲病是由班氏絲蟲、馬來絲蟲、帝汶絲蟲三種不同的絲蟲感染導致,其中約90%患者是受班氏絲蟲感染。[13]絲蟲可以感染黑斑蚊、瘧蚊等蚊子,再透過其叮咬以傳播。
當蚊子叮咬時,絲蟲幼蟲落到皮膚上。它們爬進咬傷處,穿過皮下組織,並進入淋巴管。幼蟲在淋巴管中生長約1年直至成年,成年雌蟲體長約10公分、雄蟲約5公分。雌蟲和雄蟲交配後,雌蟲開始不斷產下幼絲蟲。在成蟲剩餘5至8年的壽命裏,成年雌蟲每天會產下超過1萬條幼絲蟲。[6][14]幼絲蟲通常在夜間在血液中循環。白天,它們會聚集在肺部的毛細血管中。 [14]
當蚊子叮咬受感染者時,會連同血液一起吸入微絲蟲。在蚊子體內,這些幼蟲穿透胃壁並移動至飛行肌肉,在那裏發育10至 20天後成具有感染人類能力的成熟形式。隨後,它們遷移至蚊子的口部,在蚊子下一次叮咬時被傳播到新宿主,從而延續其生命週期。[14]
淋巴絲蟲病本身是多種複雜因素相互作用的結果:絲蟲、絲蟲體內的內共生沃爾巴克氏體、宿主的免疫反應,以及各種機會性感染和併發症。成蟲寄生於人體淋巴系統中,阻礙全身淋巴液的流動,導致慢性淋巴水腫。[15]
診斷
診斷淋巴絲蟲病的首選方法是透過顯微鏡檢查血液樣本,尋找體內的微絲蟲。通常會採集厚血片,並使用吉姆薩染色分析。診斷者需能區分班氏絲蟲與其他可能存在的寄生蟲,若血樣在微絲蟲進入血液循環時採集,血片檢測是一種簡單且相當準確的診斷方法。然而,由於微絲蟲僅在夜間進入血液循環,因此血液樣本須在夜間採集。[16]
即使在病情晚期,也可能難以在外周血液中檢測到病原體。[17]在此情況下,可透過血清抗體檢測來診斷該疾病。[4] 另外,聚合酶鏈式反應(PCR)測試可檢測極微量(1皮克)的絲蟲 DNA。死亡並鈣化的線蟲可透過X光檢測發現,而超聲波檢查則可偵測成蟲移動時所產生的影像與聲音。[18]
淋巴絲蟲病可能與非絲蟲性象皮病(又稱土源性象皮病)混淆,後者是一種非傳染性疾病,由長期赤腳接觸含鹼性的刺激性黏土土壤引起。[19][20]然而,非絲蟲性象皮病通常是雙側影響雙腿,而淋巴絲蟲病則多為單側影響。此外,非絲蟲性象皮病極少影響腹股溝區域,與淋巴絲蟲病不同。此外,地理分佈也可作為區分依據:非絲蟲性象皮病多發於高海拔、季節性降雨量大的地區,而淋巴絲蟲病則較常見於低海拔、蚊蟲盛行的地區。[19]
預防
現今已證實驅蟲劑和蚊帳(尤其是經過溴氰菊酯或氯菊酯等殺蟲劑處理過的蚊帳)可在流行地區防止蚊蟲叮咬,進而減少淋巴絲蟲病傳播。[21][22][23]此外,室內滯留噴灑和個人防護設控制病媒的重要措施。[6]
由於淋巴絲蟲病尚無已知動物宿主,因此該疾病被認為可以完全消滅。[22]世界衛生組織正協調全球努力以根除此疾病,,其主要策略是對高風險人群進行大規模驅蟲治療(MDA,Mass Drug Administration)。具體治療方案取決於該地區是否與其他絲蟲病並存。WHO 的年度 MDA 指南如下
- 與羅阿羅阿絲蟲共流行的地區:施用400 mg阿苯達唑
- 與蟠尾絲蟲症共流行的國家:施用200 mcg/kg伊維菌素與400 mg阿苯達唑。
- 沒有蟠尾絲蟲症的國家:施用6 mg/kg乙胺嗪與400mg 阿苯達唑。
- 符合 IDA 指南、且無盤尾絲蟲病的國家[24]:施用200 mcg/kg伊維菌素、6 mg/kg乙胺嗪與400 mg阿苯達唑。[6][8]
由於該寄生蟲必須依賴人類宿主繁殖,對高風險人群進行連續治療4至6年就有可能打破傳播鏈,最終導致病原體滅絕。[22]
2011年,斯里蘭卡被WHO認證為已根除淋巴絲蟲病。2017 年7月,WHO 宣佈湯加已根除該病。此外,柬埔寨、中國、庫克群島、埃及、基里巴斯、馬爾代夫、馬紹爾群島、紐埃、帕勞、韓國、泰國、瓦努阿圖、越南及瓦利斯和富圖納群島等國家和地區亦已根除該病。[25]WHO於2020年設定目標,希望在 2030年前讓80%的流行國家消除淋巴絲蟲病。[26]
治療
淋巴絲蟲病的治療方式部分取決於感染該病的地理區域,通常涉及兩種或以上的驅蟲藥聯合使用,如阿苯達唑、伊維菌素和乙胺嗪。在漠南非洲,該病通常使用阿苯達唑與伊維菌素治療;在西太平洋地區,則使用三種藥物聯合治療。阿苯達唑與乙胺嗪的組合雖然常見,但不像其他組合那樣具有區域特異性。對於與羅阿羅阿絲蟲病共流行的地區,則採用阿苯達唑單藥治療,並結合病媒控制措施,2022年約1120萬人接受此治療方案。[8]
沃爾巴克氏體是寄生於絲蟲體內的共生細菌,為絲蟲提供生存所需的營養。四環素類抗生素多西環素可殺死這些細菌,進而阻止微絲蟲發育成成蟲,並縮短成蟲的壽命,使其在1至2年內死亡,而非原本10至14年的壽命。多西環素已被證明對治療淋巴絲蟲病有效,但其治療限制包括:
阿苯達唑考以阻止絲蟲吸收葡萄糖,使其因能量耗竭而死亡。[29]單獨使用阿苯達唑的療效不一,但與乙胺嗪聯合使用時效果更佳。[30]
伊維菌素常與阿苯達唑並用,其作用機制為與寄生蟲神經細胞結合,使其對氯離子通透性增加,最終導致寄生蟲癱瘓死亡。然而伊維菌素只能殺死幼蟲,無法殺死成蟲,因此通常需與 乙胺嗪合併使用,以同時消滅幼蟲和成蟲。[31]
對於陰囊象皮病(scrotal elephantiasis)和鞘膜積液,手術可能有幫助。然而,手術對於四肢象皮病的治療效果有限。[32]保持良好的衛生習慣、皮膚護理、運動和抬高受感染的肢體,可以減少或預防淋巴水腫和鞘膜積液引起的急性炎症反應。[6]
流行病學

無資料
小於10年
10–50
50–70
70–80
80–90
90–100
100–150
150–200
200–300
300–400
400–500
大於500年
淋巴絲蟲病發生在非洲、亞洲、中美洲、加勒比地區、南美洲以及某些位於熱帶和亞熱帶地區的太平洋島國。由淋巴絲蟲病引起的象皮病是世界上最常見的永久性殘疾之一。截至2018年,全球約有5100萬人感染淋巴絲蟲病,至少50個國家共8.63億人生活在需要預防性治療以阻止感染擴散的地區。到2022年,感染人數已降至約4000萬、在47個國家流行。這些改善主要歸功於世界衛生組織發起的全球消除淋巴絲蟲病計劃。自該計劃實施以來,已有7.4億人不再需要接受預防性治療。[6]
90%的淋巴絲蟲病是由班氏絲蟲引起,其餘病例大多是由馬來絲蟲引起的,而帝汶絲蟲較為罕見。班氏絲蟲主要影響赤道帶地區,包括非洲、尼羅河三角洲、土耳其、印度、東印度群島、東南亞、菲律賓、太平洋島嶼和南美部分地區。由於該病需要多次蚊蟲叮咬並持續數月至數年才能傳播,因此透過旅遊感染的風險較低。[33]班氏絲蟲之病媒蚊偏愛吸食人血,人類是唯一已知的天然宿主,無已知的動物宿主。[34]淋巴絲蟲病在美國極為罕見,僅在20世紀初在南卡羅來納州報告過一起病例。[4]
在南美洲,巴西、多米尼加共和國、圭亞那和海地四國致力於控制淋巴絲蟲病。[35]在拉丁美洲,該病主要由班氏絲蟲傳播,當地的主要媒介蚊為庫蚊屬。[36]為了應對該病的迅速發展,該地區推行了大規模藥物投放(MDA)計劃,該計劃已導致對藥物治療需求減少67%。[35]
巴西應對該病的方法包括以MDA計劃向受影響最嚴重的社區提供乙胺嗪藥物,並提供術後護理,例如教導家屬如何護理患者、幫助患者尋找工作以及提供社會支援網絡,以幫助患者重新融入社會。[37]
多米尼加共和國從2002年到2007年每年施行5輪DEC藥物治療,之後又進行了3輪MDA。[38]
圭亞那在2003至2007年期間使用DEC強化鹽來控制該病,並從2014年起改用MDA與DEC藥物相結合,以提高患者教育和治療的可及性。[38]
海地則在2002年開始使用DEC藥物,到2012年已達到全國範圍覆蓋,至2014年已有約20個社區不再需要MDA。
在淋巴絲蟲病流行的社區中,多達10%的女性會出現肢體腫脹,50%的男性會出現生殖器毀損。[39]
歷史


有證據顯示淋巴絲蟲病的病例可追溯至4000年前。[40]古印度的《梨俱吠陀》約在西元前1500年至1200年成書,當中可能提及了象皮病。《梨俱吠陀》第七卷的第五十首讚歌向神祇密多羅(Mitra)、伐樓那和阿耆尼祈求保護,避免受到「內部滋生並腫脹的事物」侵害。詩歌的作者懇求諸神不要讓「蟲」傷害他的腳,並描述該疾病會導致腳踝和膝蓋出現腫塊。[41]古埃及(西元前 2000 年)和西非諾克文化(西元前 500 年)的文物中,也顯示了可能的象皮病症狀。最早明確記載該疾病的文獻出現在古希臘,當時學者將淋巴絲蟲病與痲瘋病區分開,將痲瘋病稱為「希臘象皮病」(elephantiasis graecorum),而將淋巴絲蟲病稱為「阿拉伯象皮病」(elephantiasis arabum)。[40]
關於該病症狀的首次記錄出現在 16 世紀,當時荷蘭探險家揚·哈伊根·范林斯霍滕在探索果阿時紀錄到該病。隨後的探險家在亞洲和非洲地區也記錄了類似的症狀,但對該病的真正理解直到幾個世紀後才逐漸建立。[來源請求]
該病的致病原首次於19世紀晚期被識別。[42]1866 年,提摩西·路易斯在尚·尼古拉斯·德·馬爾奎和奧托·亨利·武歇雷的研究基礎上,確認微絲蟲與象皮病之間的關聯,為後續研究奠定基礎。1876年,約瑟夫·班克羅夫特發現了絲蟲成蟲[43]。隔年,萬巴德提出了該病與節肢動物傳播的關聯,並證實蚊子體內含有該病原體。然而,曼森當時誤認該病是透過接觸蚊蟲產卵的水體傳播的。[44]1900 年,喬治·卡邁克·洛確認了真正的傳播方式,發現蚊子口器內存在絲蟲,從而確定其透過蚊蟲叮咬傳播的機制。[40]
| “ | 馬拉巴爾地區許多人,包括奈爾和婆羅門及其妻子,甚至總人口的四分之一或五分之一,包括最底層的族群,都患有雙腿嚴重腫脹的疾病,這是一種可怕的景象。他們說這是因為他們經常涉水,而這片土地本身就十分潮濕。當地語言稱這種病為「pericaes」,這種腫脹從膝蓋以下蔓延,但患者不會感到疼痛,也不會特別在意這種疾病。 | ” |
| ——托梅·皮雷斯,東方志1512–1515.[45] | ||
研究方向
伊利諾伊大學芝加哥分校的研究人員開發出預防淋巴絲蟲病的新型疫苗。該疫苗已被證明能在淋巴絲蟲病感染的小鼠引發強烈的保護性免疫反應。這種疫苗引發的免疫反應已被證明可以在小鼠模型中預防班氏絲蟲和馬來絲蟲感染,並且可能對人類有用。[46]
2007年9月20日,遺傳學家發表了首篇馬來絲蟲的完整基因組草稿。[47]該計劃於1994年啟動,到2000年時已確定其80%基因組。確定其基因可能有助於藥物研發和疫苗。 [48]
獸類疾病
參考文獻
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.