碳化鉭是一類二元化合物,由鉭和碳組成,實驗式TaCx,x 一般在 0.4 到1 之間。它們的硬度極大,脆,是耐火材料,具有金屬的電導率。它是一種棕灰色粉末,通常通過燒結處理。
| 碳化鉭 | |
|---|---|
| |

| |
| IUPAC名 Tantalum carbide | |
| 別名 | 碳化鉭(IV) |
| 識別 | |
| CAS號 | 12070-06-3 12070-07-4((TaC0.5)) |
| SMILES |
|
| InChI |
|
| InChIKey | DUMHRFXBHXIRTD-UHFFFAOYSA-N |
| 性質 | |
| 化學式 | TaC |
| 摩爾質量 | 192.96 g/mol g·mol⁻¹ |
| 外觀 | 棕灰色粉末 |
| 氣味 | 無臭 |
| 密度 | 14.3–14.65 g/cm3 (TaC) 15.1 g/cm3 (TaC0.5)[1] |
| 熔點 | 3,850—3,880 °C(4,120—4,150 K)(TaC)[2] 3,327 °C(6,021 °F;3,600 K) (TaC0.5)[1] |
| 沸點 | 4,780—5,470 °C(5,050—5,740 K)(TaC)[1][2] |
| 溶解性(水) | 不溶 |
| 溶解性 | 可溶於HF-HNO3的混合物[1] |
| 熱導率 | 21 W/m·K |
| 熱力學 | |
| ΔfHm⦵298K | −144.1 kJ/mol |
| S⦵298K | 42.29 J/mol·K |
| 熱容 | 36.71 J/mol·K[3] |
| 相關物質 | |
| 相關化學品 | 一氮化鋯 碳化鈮 碳化鋯 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
作為重要的金屬陶瓷材料,碳化鉭在商業車刀中用於切削應用,有時會添加到碳化鎢合金中。[4]
取決於純度和測量條件,碳化鉭的熔點在約3880℃達到峰值。這個值是二元化合物里最高的。[5][6]只有碳化鉭鉿的熔點可能略高,大約為3942°C,[7]而碳化鉿的熔點與TaC相當。
製備
TaCx粉末是由鉭和石墨的粉末在真空或惰性氣體(氬)里使用爐子或電弧熔化裝置在約2000℃的溫度下進行加熱。[8][9]鉭和石墨的量決定了x的值。另一種技術是在真空或氫氣氣氛中,在1500–1700℃的溫度下通過碳進行五氧化二鉭的還原。該方法於1876年用於獲得碳化鉭,[10]但它無法控制產物的化學計量。[6]自蔓延高溫合成法也是已報道的直接從單質製備TaC的方法之一。[11]
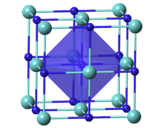
晶體結構

當 x = 0.7–1.0 時,TaCx有着立方結構 (岩鹽的結構) 。[12]碳化鉭的晶格常數會隨着x增長而增長。[13] TaC0.5有兩種結構。較穩定的具有反碘化鎘型三角結構,該結構在加熱至約2000℃時轉變為六方晶格,對碳原子來說已經沒有規律了。[8]
在這個表中,Z是每單位的配位數,ρ是由晶格常數計算而來的密度。
性質
碳化鉭中鉭和碳原子之間的鍵是離子鍵,金屬鍵和共價鍵混合,是很複雜的鍵,並且由於強共價成分,這些碳化物是非常堅硬且易碎的材料。舉個例子,TaC的顯微硬度為1600-2000 kg/mm2 [16](〜9 Mohs)和285 GPa的彈性模量,而鉭的相應值為110 kg/mm2和186 GPa。碳化鉭的硬度,屈服和剪切應力隨TaCx中碳含量的增加而增加。[17]
碳化鉭無論是什麼大小和溫度都具有金屬導電性。TaC 可以在10.35 K以下轉變為超導體。[13]
TaCx的磁性能從x≤0.9的反磁性變為「 x」≥0.9的順磁性。儘管HfCx具有與TaCx相同的晶體結構,但仍觀察到了相反的行為(磁性隨x的增加而減少)。[18]
應用
碳化鉭因其在熔點、硬度、彈性模量、導熱性、熱衝擊方面的優異物理性能而被廣泛用作超高溫陶瓷(UHTC)的燒結添加劑或高熵合金(HEA)的陶瓷增強材料抵抗力和化學穩定性,這使其成為航空航天工業中飛機和火箭的理想材料。
天然存在
鉭碳礦是碳化鉭的天然存在形式。它屬立方晶系,並且非常稀有。[19]
參見
參考資料
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
