Loading AI tools
固氧、固態氧形成於正常大氣壓的54.36K(-218.79°C)以下。固態的氧氣由於吸收紅色光,像液氧一樣,是淺藍色透明物質。 氧分子因它在分子磁化(molecular magnetization)上與晶體結構、電子排布、超導電性的關係而受到關注。氧分子是能承載磁矩的唯一的簡單雙原子分子(通常情況下縱使所有分子也只有少數能夠如此)[1]。它被認為是「受自旋控制(spin-controlled)」的晶體[1],並因此展現出不尋常的磁性規律[2]。在極高壓下,固氧從熱絕緣材料變成金屬的形態[3];而在極低溫下,它甚至能變成超導體[4]。對固氧的結構研究始於19世紀20年代,目前,已確定六種明確的晶體相[1]。
固氧的密度從α相的約21 cm3/mol,到γ相的約 23.5 cm3/mol 。固氧的摩爾質量 來自美國國家標準技術研究所

- α相:淺藍色,正常大氣壓下生成於23.8K以下,單斜晶系。
- β相:微弱的藍色至粉紅色,正常大氣壓下生成於43.8K以下,三方晶系。(室溫高壓下變為O
4) - γ相:微弱的藍色,正常大氣壓下生成於54.36K以下,等軸晶系。
- δ相:橙色,室溫下施加9GPa(9千兆帕斯卡)以上的壓強時生成。
- ε相:深紅色至黑色,室溫下施加10GPa以上壓強時生成。
- ζ相:金屬,在96GPa以上壓強生成。
已知室溫下給氧氣施加壓強時,它會凝固成叫做β相的物態。繼續加大壓強後,9GPa時,β相相變為δ相,10GPa時變為ε相。同時,隨着分子間斥力的增大,β相的顏色從粉紅到橙色,再到紅色(穩定的O
8形式),紅色隨壓強增大而逐漸變深直至黑色。96GPa下ε相出現後繼續壓縮,將出現金屬形式的ζ相。[5]
隨着室溫下氧氣的壓強超過10GPa,它將出人意料地相變為另一個同素異形體。它的體積驟減[6],顏色也從藍變成深紅[7]。這種ε相發現於1979年,但當時它的結構並不清楚。基於它的紅外線吸收光譜,1999年,研究人員推斷此相態是O
4分子的晶體[8]。但在2006年,X射線晶體學表明這個被稱作ε氧或紅氧的穩定相態實為O
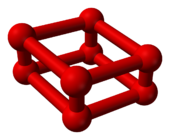
8[9][10]。此結構在理論上不曾被預測[5]:由四個O
2分子組成的菱形的O
8原子簇[11]。
 |
 |
8 的球棒模型 |
所有相態中,這個相態相當有趣。它顏色為深紅色,對紅外線吸收能力很強,並有磁場縮滅(magnetic collapse)[1]。它在很大的壓強範圍內(10GPa至96GPa)穩定,已成為許多X射線繞射、光譜學和理論學者的課題。
ε相的氧被繼續壓縮後,出現了ζ相[6]。這種相態在1990年,給氧氣施加132GPa壓強時也出現了[3]。已知金屬的、簇狀的ζ相[13]在低溫下表現出超導性[4][5]。
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.