热门问题
时间线
聊天
视角
價電子
原子中参与形成化学键的电子 来自维基百科,自由的百科全书
Remove ads
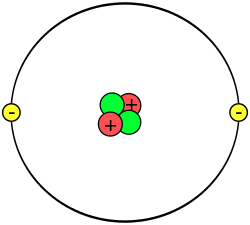
價電子(英語:valence electron)或價層電子(valence shell electron),是原子核外電子中能與其他原子相互作用形成化學鍵的電子。價層(valence shell)或價殼層[1]、價電子層,是一組在能量上可接受電子以形成化學鍵的軌域。
簡介
一般而言,主族元素的價電子就是「最外層電子」,即主族元素原子的主量子數最大的那層電子。過渡元素的價電子則可包括「次外層電子」,即過渡元素的價電子不僅是主量子數最大的那層電子,次外層電子也可以成為價電子。某些元素的倒數第三層電子也可以成為價電子。
價電子在決定一元素如何與其他元素進行化學反應時起了重要作用:原子的價電子愈少,原子就愈不穩定亦愈容易反應。
價電子通常處於最外層的電子軌道,且可以在原子間形成化學鍵的電子。價電子表示有形成化學鍵能力的電子,和已經形成化學鍵的電子是不同的。此外,價電子同時亦決定該元素的電導率。
各族價電子的數量
元素的價電子數是由元素週期表中的族所決定的,次元素就是這樣被分類。除週期表中的副族(又稱B族,第3-12族,即過渡金屬)外,個位數用以識別每直行下元素的價電子數。
* 價電子一般不對過渡金屬有用。
** 除氦以外,因為氦只有兩個價電子。
化學反應中的價電子
一原子最外層電子殼的價電子支配原子的化學鍵作用。因此,相同價電子數的原子在元素週期表被放置於同一列。一般來說,原子價的電子數與穩定原子(即同週期的惰性氣體原子)的原子價個數差距愈少,活性就愈高。所以第I族鹼金屬非常活潑,該族包括了鋰、鈉及鉀,它們是金屬中活性最高的一群。
每一個原子,如果有滿原子價的話都穩定得多,活性亦會低得多。而實現如此有兩個方式:一個原子跟鄰近原子分享電子,形成共價鍵;一個原子從其他原子中搶走電子,形成離子鍵。其中,若離子鍵需要一個原子把它的一些電子送給另一個原子,特稱為配位共價鍵。
* 共價鍵就是握手式的黏接及綁住。
** 離子鍵就是電容器形式的黏接及綁住。原始條件是高電壓原子與低電壓原子遠端存在以使電子從高電壓原子往低電壓原子流動。當這2個原子的電壓等值時,即完成了電容器的電壓平衡,於是離子鍵便形成了。而高電壓原子被稱為配合共價鍵是因為流動的電量主要由低電壓原子決定。
參考
外部連結
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads