Loading AI tools
来自维基百科,自由的百科全书
西方墨點法(英語:Western blot)或稱「蛋白質轉漬法」、「免疫墨點法」(immunoblot)或「西式吸印雜交」,是在分子生物學、生物化學和免疫遺傳學中常用的一種實驗方法,也是HIV檢測的方法之一。

利用特定抗體能夠專一結合其抗原蛋白質的原理來對樣品進行着色,通過分析着色的位置和着色深度獲得特定蛋白質在所分析的細胞或組織中的表達情況的信息,來分析檢測特定蛋白質的生物學檢測技術。
發明者一般認為是美國斯坦福大學的喬治·斯塔克(George Stark)。[1]在尼爾·伯奈特(Neal Burnette)於1981年所著的《分析生物化學》(Analytical Biochemistry)中首次被稱為「Western印跡法」。
Western Blot與Southern或Northern雜交方法類似,但Western Blot採用的是聚丙烯酰胺凝膠電泳,被檢測物是蛋白質,「探針」是抗體,「顯色」用標記的二抗。經過PAGE(根據分子大小)分離的蛋白質樣品,轉移到固相載體(例如硝酸纖維素薄膜)上,固相載體以非共價鍵形式吸附蛋白質,且能保持電泳分離的多肽類型及其生物學活性不變。以固相載體上的蛋白質或多肽作為抗原,與對應的抗體起免疫反應,再與酶或同位素標記的第二抗體起反應,經過底物顯色或放射自顯影以檢測電泳分離的特異性目的基因表達的蛋白成分。該技術也廣泛應用於檢測蛋白水平的表達。
實驗大致分為鑄膠、跑膠、轉漬、接一級抗體、接二級抗體以及壓片幾個部分。
樣本可以從整個組織或者細胞培養物中獲得。固體組織首先需要被機械性的破碎,可以使用攪拌器(對於較大體積的樣本),勻質機(對於小體積的樣本),或者利用超聲波粉碎。細胞也可以通過上述方式機械性的被破開。當然病毒及環境樣本也可以是蛋白的來源,因此Western Blotting並不僅限於細胞研究。
合適的清潔劑、鹽類和Buffer都可以被用於裂解細胞以及溶解蛋白。蛋白酶和磷酸酶抑制劑經常被添加進去,以防護樣品被其自身的酶消化掉。組織準備經常在低溫條件下進行,以避免蛋白變性和降解。
生物化學與機械技術(包括各種形式的過濾和離心)的結合,可用於分離不同的細胞室與細胞器。

樣本中的蛋白質通過凝膠電泳進行分離。蛋白質可以通過等電點(pl),分子量,電荷,以及上述因素的組合進行分離。分離的實際效果取決於樣本的處理和凝膠的性質。這是用來識別某種蛋白的一個非常有用的方法。
到目前為止,最常見的凝膠電泳方式是採用聚丙烯酰胺凝膠和十二烷基硫酸鈉(SDS)作為緩衝負載的組合。SDS-PAGE(SDS聚丙烯酰胺凝膠電泳)能夠保存處在變性狀態下的多肽,這些多肽由蛋白質被強還原劑還原而失去了二三級結構產生(例:從二硫鍵[S-S]到巰基[SH and SH]),通過他們不同的分子量,從而將蛋白質分離。採樣蛋白被帶負電荷的SDS包裹,並通過凝膠的丙烯酰胺網格移動到帶正電的電荷上。較小的蛋白質會更快的遷移通過這個網格,因此蛋白質是通過大小(通常用千道爾頓,kDa作為量度單位)進行分離的。丙烯酰胺濃度決定了凝膠的分辨率:丙烯酰胺濃度越大,較低分子量的蛋白質的分辨率越好。丙烯酰胺濃度越低,高分子量的蛋白質的分辨率越好。蛋白質通常在凝膠上只沿一維做線性運動形成印痕。
樣品被加載到凝膠的泉點。第一道通常是預留給標記物或者梯度物的,它們是一些市售的蛋白質混合物,具有標定的分子量,能形成典型可見的彩色染色條帶。當電壓被施加在凝膠上,蛋白質透過其以不同的速度進行遷移,取決於蛋白質的大小。這些不同的前進速率(不同的電泳遷移率)在每個道內單獨形成條帶。

它也可以使用兩維(2-D)的凝膠,蛋白質從一個單一樣品中沿兩個維度傳播。蛋白質按等電點(蛋白質解離成陰陽離子的趨勢或程度相同,使得淨電荷成中性,此時的pH值即為等電點)在第一個維度分離,並根據其分子量在第二個維度中分離。
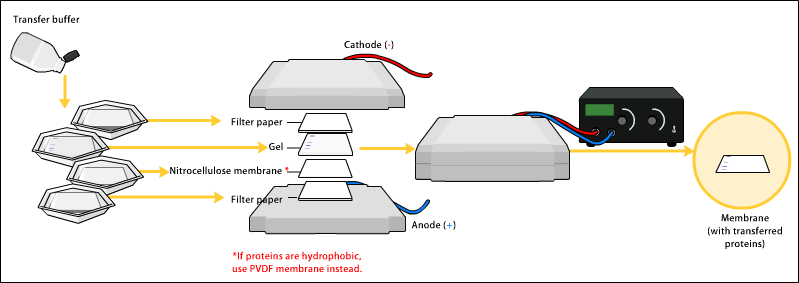
要讓抗體成功對蛋白質產生反應,就要將蛋白質從凝膠中轉移到用硝化纖維或聚偏二氟乙烯(PVDF)製成的膜。轉漬蛋白質時,最常用的方法稱爲"電印跡"(Electroblotting),即運用電流,從凝膠中牽引出帶負電荷的蛋白質,使其向帶正電荷的陽極方向移動,進入PVDF或硝化纖維膜內。蛋白質自凝膠移入膜內時,可維持其在凝膠內形成的結構。較舊的轉漬方法,則是在凝膠上先放一塊膜,再放一疊濾紙,然後,將其整疊移至緩衝溶液中,溶液在毛細管作用下會帶動蛋白質,一同由下而上進入濾紙。但實際上由於耗時長,該方法並不常用。 不論採用何種方法,轉漬完成後,蛋白質便會顯露於薄膜上,可供檢測。
由於膜能結合蛋白質,所以抗體以及目標蛋白都可以結合到膜上,也因此我們必須防止膜和抗體的反應發生。把膜放在稀釋的蛋白質溶液中(比如3-5%的牛血清蛋白、脫脂牛奶、TBS或者I-Block)可以阻擋非特定的結合。稀釋溶液中的蛋白會把膜上沒有與目標蛋白結合的地方全部結合,因此加了抗體之後,膜上就沒有空間去結合其他非目標蛋白。阻攔是實驗最後的鋪墊,可以使結果更清晰,排除錯誤可能性。
在檢測過程中,使用被修飾的抗體作「探針」來標記膜上的目標蛋白,這一抗體與報告酶相連接。當暴露於適當的底物時,報告酶驅動比色反應並產生顏色。由於各種原因,這傳統上發生在一個兩步法的過程中,雖然現在某些應用中可以用一步法的檢測方法。
當宿主或免疫細胞培養物暴露於目標蛋白(或其一部分)時,產生一抗。通常這是免疫反應的一部分,而在這裡一抗被採集,並在 Western blot 實驗中被用作直接結合蛋白質的敏感的和特異性的檢測工具。
在封閉後,將使用PBS或TBST緩衝液稀釋後的一抗溶液(通常0.5-5mg/mL)在溫和攪拌下與膜培育,通常室溫下培育1小時,或4℃下培育過夜。也可在不同溫度下培育,較低的溫度常帶來更高的結合性,包括特異性(與"目標蛋白")與非特異性(與"噪聲")結合。培育後,將膜在洗滌緩衝液中洗滌數次以除去未結合的一抗,使背景最小化。通常,洗滌緩衝液包括含少量洗滌劑的緩衝鹽液,有時加入奶粉或BSA。
沖洗膜以除去未結合的一抗,然後將膜暴露於另一種抗體,稱之為二抗。抗體來源於動物(或動物源的雜交瘤培養物)。二抗識別並結合一抗的物種特異性位點。因此,一個抗小鼠二抗可以與任何小鼠來源的一抗結合,並且可被稱為「抗物種」抗體(如抗小鼠,抗山羊等)。為了檢測靶蛋白,二抗通常與生物素或報告酶結合,如鹼性磷酸酶、辣根過氧化物酶。這意味着幾種二抗可與一種一抗結合併增強信號,從而可以檢測比單獨SDS-PAGE凝膠電泳所見濃度更低的蛋白質。
辣根過氧化物酶(Horseradish peroxidase, HRP)通常與二抗結合,以允許通過化學發光檢測靶蛋白。化學發光底物被HRP裂解,產生發光。因此,發光的量與HRP結合的二抗的量成正比,從而可以間接檢測靶蛋白的存在。將敏感的攝影膠片置於膜上,暴露於反應產生的光,可以產生與印跡結合的抗體的圖像。更便宜但不太敏感的方法是使用含1%過氧化氫的4-氯萘酚染色劑,過氧化物自由基與4-氯萘酚反應產生深紫色斑點,可以在不使用專門膠片的情況下拍攝。
另一種二抗檢測方法利用了近紅外(near-infrared, NIR)熒光團結合的抗體。由熒光染料激發產生的光是靜態的,使得熒光檢測更更清晰和精確地測量 Western blot 中與蛋白結合的標記抗體產生的信號。蛋白質可以被精確測量,是因為膜上由不同蛋白量產生的信號是靜態測量的,而化學發光檢測的光是動態測量的。
第三種選擇是使用放射性標記而不是與二抗結合的酶,例如使用碘的放射性同位素標記抗體結合蛋白,如葡萄球菌蛋白A或抗生蛋白鏈黴菌素。由於其他方法更安全、快捷、便宜,現已很少使用這種方法。然而,該方法的一個優點是基於自動射線的成像的靈敏度,在光學軟件的幫助下,可以實現高精度的蛋白定量檢測。

歷史上,由於在不同過程中獲得一抗和二抗相對容易,探測過程通常採用兩步法。這為研究人員和公司在靈活性、縮減成本方面提供了巨大優勢,也為檢測過程增加了擴增步驟。然而,由於高通量蛋白分析和低檢測限的出現,人們對發展一步法探測系統產生興趣,這一系統將加快檢測進程,並減少消耗。這需要一種探針抗體,既能識別靶蛋白,又含有可檢測的標記,探針通常可用於已知的蛋白標籤。與兩步法中的一抗類似,初級探針與膜一起培育,然後在一些列洗滌步驟後可以直接檢測。
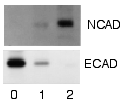
在未結合的探測劑被洗去之後,西方墨點法準備好檢測被標記和結合到目標蛋白質的探測劑。在實際應用中,並不是所有的西方墨點法揭示蛋白質僅在一種膜上的一個條帶。
雙向凝膠電泳也有用於上述的結果測定的前景。在2-D SDS-PAGE中,多肽鏈在二維平面上遷移。比如說,在第一個維度上,多肽根據其等電點被分離。而在第二個維度上,多肽鏈根據其分子質量分離。一個已知蛋白的等電點由其帶正電氨基酸(如賴氨酸、精氨酸)與帶負電氨基酸(穀氨酸、天冬氨酸)的相對數量決定。樣品可以先在非還原性條件下由SDS-PAGE分離,之後在還原性條件下做雙向電泳,後者會打破使蛋白質亞基連接的二硫鍵。
原則上,這個方法可以做到在一個凝膠中分離所有細胞蛋白。它主要的優勢即在於它往往能區分不同特定蛋白的多個亞種,比如區分一個蛋白是否被磷酸化。被分離的蛋白可以從凝膠中切除並後續使用質譜法確定分子質量。
Western Blot顯色的方法主要有以下幾種:
現常用的有底物化學發光ECL和底物DAB呈色,體同水平和實驗條件的是用第一種方法,目前發表文章通常是用底物化學發光ECL。只要買現成的試劑盒就行,操作也比較簡單,原理如下(二抗用HRP標記):反應底物為過氧化物+魯米諾,如遇到HRP,即發光,可使膠片曝光,就可洗出條帶。
Western印跡法在生物化學中定性檢測單個蛋白與蛋白修飾(比如翻譯後修飾PTM)中有着廣泛的應用。據估計,至少8-9%的與蛋白相關的出版物都應用了Western印跡法[2]。他被用作為一種可以鑑別在蛋白混合物中鑑別單種蛋白的泛用方法。並且通過蛋白與印跡膜上蛋白帶的大小與顏色可以得到一個半定量的估計。除此以外,應用在一組經過梯度稀釋已知濃度的純化蛋白可以獲得更加精確的蛋白濃度。Western印跡法被常規用作蛋白克隆後的鑑定實驗,也被廣泛用於藥物診斷,比如HIV診斷和牛海綿狀腦病(通常所說的瘋牛病)檢測。
在HIV檢測試驗種,應用Western印跡法檢驗在人體血清中的抗HIV抗體。已知被HIV感染的細胞被分散的點在向上面描述的膜上。隨後,血清在一級抗體中培育;洗去自由的未結合抗體,並加入與一個酶信號連接的二級抗體。顯色的板子就會表示出病人的血清中很有抗體[3]。Western印跡法也被用在診斷變異型克雅二氏病中,這是一種由於食用患有牛海綿狀腦病的牛肉所引起的朊毒體疾病。
另一個應用是用於的兔熱病診斷中。Western印跡法檢測針對土倫病法蘭西斯氏菌的敏感度幾乎達到100%,而專一性也達到了99.6%。[4]
Western印跡法進一步的應用也包括世界反興奮劑組織的賽後檢測等等。
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.