热门问题
时间线
聊天
视角
多囊卵巢綜合症
来自维基百科,自由的百科全书
Remove ads
多囊性卵巢綜合症(英語:Polycystic ovary syndrome,簡稱PCOS),又稱斯-李二氏症(Stein-Leventhal syndrome),是女性因為雄性激素上升所導致的症狀[4]。多囊性卵巢的症狀包含月經不規律或是無月經、月經量過多、多毛症、粉刺、盆腔疼痛、難以受孕與黑棘皮症[3]。相關的病症包含第二型糖尿病、肥胖症、阻塞性睡眠呼吸暫停、心血管疾病、情感障礙與子宮內膜癌[4]。
多囊性卵巢會受基因遺傳與環境因素影響[6][7]。其危險因子包含肥胖症、運動量不足或是有家族病史[8]。如果有以下三種症狀中的兩種便可診斷患者有多囊性卵巢:無排卵、雄性激素過高與卵巢囊腫[4]。囊腫可以由超音波影像檢測。其他造成類似症狀的疾病包含先天性腎上腺增生症,甲狀腺機能低下症與高泌乳素血症[9]。
多囊性卵巢綜合症目前並無特效藥可以治療[5]。現行治療方式包括減重和運動等生活型態調整[10][11],避孕藥物對於調整經期、抑制多餘的毛髮生長與改善青春痘有所幫助。二甲雙胍和抗雄性激素可能能夠改善多囊性卵巢綜合症,且針對青春痘和多毛等症狀有一定治療效果[12]。減重或是使用可洛米分、降血糖藥物每福敏則有助於改善不孕的狀況。若以上治療對於病人都沒有效果且病人有生育考量,則可考慮體外人工授精這個選項[14]。
多囊性卵巢綜合症是18歲到44歲女性間最常見的內分泌疾病[15]。一般認為,多囊卵巢綜合症的發生率在女性生育年齡期間佔約20%(根據鹿特丹診斷指引,英國為26%、澳洲為17.8%、土耳其為19.9%、伊朗為15.2%[16]。)多囊卵巢綜合症是現今導致不孕的主要原因之一[4]。目前已知最早的多囊卵巢綜合症病例於1721年紀錄於意大利[17]。
Remove ads
體徵及症狀
常見的體徵和症狀如下:
- 月經失調: 多囊卵巢綜合症主要導致月經次數過少(一年月經次數少於九次)或閉經(沒有月經連續三到數個月以上),也可能造成其他類型的月經失調[15][18]。
- 不孕[18]: 這是一個由慢性無排卵導致的常見症狀 (缺乏排卵)[15]。
- 雄性激素分泌過多: 即為雄性素過多症。最常見的症狀為痤瘡和多毛症,也可能導致月經過多 (週期長且量多的月經週期), 雄激素過多型脫髮症 (增加毛髮脫落程度及瀰漫性脫髮), 或其他症狀[15][19]。 約有四分之三的多囊卵巢綜合症女性患者 (根據 NIH/NICHD 1990的診斷標準))有出現高雄性素血症的症狀[20]。
- 代謝症候群:[18]有肚腩贅肉且出現與胰島素抗性有關的症狀[15]。 罹患多囊卵巢綜合症的女性的血清中胰島素與升半胱胺酸濃度較正常女性來的高且有胰島素抗性[21]。
Remove ads
原因
多囊卵巢綜合症為一種成因不明的異質性失調。[18][22][23]有一些證據如: 家族病例、同卵雙胞胎相比異卵雙胞胎在多囊卵巢綜合症的內分泌和代謝之遺傳性特徵上有較高的一致性等,點出多囊性卵巢綜合症可能為遺傳性疾病[7][22][23]。亦有證據表明若胎兒於子宮中暴露於高濃度的雄性激素與抗穆氏管荷爾蒙中,隨著年紀增長會提升其患多囊卵巢綜合症的風險。[24]
致病性的基因為體染色體顯性遺傳,在女性身上具有高度的基因外顯性且多變的表現度;這代表小孩有50%的機率從雙親其中一方獲得可能致病的基因片段,如果獲得此基因片段的為女兒,則會出現一定程度上的病徵[23][25][26][27]。 異變基因可能從父母雙方遺傳而來,也可能遺傳給兒女(可能成為帶原者或是早期脫髮或毛髮過多症狀者) [25][27]。
表現型:有一部分患者個疾病表現為卵泡膜分泌過多的雄性素 [26]。確切的基因影響方式尚未被確認[7][23][28]。在少數的案例,單個基因的突變有可能造成綜合性的突變症狀[29]。目前對該綜合症的發病病理機致的研究指出,多囊卵巢綜合症為複雜的多基因疾病[30]。
多囊卵巢綜合症症狀的嚴重程度似乎主要取決於肥胖症[7][15][31]。
多囊卵巢綜合症可視為一種代謝疾病,其的部分症狀為「可逆的」。 即便多囊卵巢綜合症由28個症狀組成,但其仍被視為一種婦科疾病。
即使多囊卵巢綜合症的病名表明卵巢為該疾病的病理核心,但是囊腫為一種症況而非病因。就算兩個卵巢被摘除,部分多囊卵巢綜合症的症狀仍會持續下去,其症狀在不存在囊種的狀況下仍有可能出現。自從1935年Stein和Leventhal首次描述以來,診斷、症狀和致病因素的標準仍為爭議的主題之一。因為卵巢為首要受影響的器官,婦科學者們通常視其為一種婦科疾病。然而,近年來許多觀察顯示多囊性卵巢為一種多重系統性失調疾病,主要問題源自於下視丘賀爾蒙調節失調 ,許多器官也與此調節有關。多囊性卵巢這個名稱源自於超聲波診斷之影像。多囊性卵巢綜合症的症狀非常多變,且只有約百分之15的患者可由超音波影像看出其卵巢中有囊腫。[32]
多囊卵巢綜合症可能與產前經期、表觀遺傳學因子、環境影響(尤其是工業中產生的內分泌干擾素[33]如雙酚A與特定藥物)及肥胖比例增加有關,上述任何原因之一都有可能是使病症惡化的緣由。[33][34][35][36][37][38][39]
發病機制
多囊性卵巢的發展會刺激卵巢持續製造分泌過量的雄性激素,尤其是睪固酮,通常會伴隨著以下的其中一個症狀或是兩者皆有(幾乎肯定其具有遺傳易受性[26]):
多囊性卵巢綜合症因其在超音波診斷中普遍可見的大量卵巢囊腫聞名。這些「囊腫」其實是未成熟的濾泡而非囊腫。這些濾泡由初級濾泡發育而成, 但在空腔濾泡期早期因為卵巢功能停止發育,這些濾泡會出現在卵巢周邊,在超音波檢驗的影像中看起來像成串的珍珠[來源請求]。
患有多囊性卵巢症候群的婦女因為下視丘釋放促性腺激素釋放激素的頻率增加,導致黃體成長激素與濾泡刺激素的比值升高[40]。
大多數具有PCOS的婦女具有胰島素抵抗或肥胖的症狀。 他們的胰島素濃度異常的提高導致「下丘腦-垂體-卵巢軸」區域中的異常並引起PCOS的症狀。高胰島素血症提高GnRH的釋放頻率、黃體成長激素量多過濾泡刺激素,因而佔了主導地位、增加卵巢雄激素的產生、減少濾泡的成熟並減少SHBG的作用[18]。此外,過多的胰島素會透過PI3K調高17α羥化酶的活性,而17α羥化酶的活性也和雄激素前體的合成有關[41],因此過多胰島素的幾個效果都會提高PCOS的風險[42]。胰島素抵抗是女性常見的情形,在正常體重的女性及體重過重的女性都可能會出現[10][15][21]。
Remove ads
診斷
並不是每一個多囊卵巢綜合症的病人都有出現多囊卵巢的症狀,也並非所有卵巢曩腫的病患都有多囊卵巢綜合症的症狀;雖然骨盆超聲波是主要的診斷工具,但也並不是唯一個診斷工具[43]。雖然該綜合徵與廣泛的症狀相關,最直接的診斷方法是使用鹿特丹診斷標準。
2023 年 8 月,Human Reproduction[44]、Fertility and Sterility[45]、The Journal of Clinical Endocrinology & Metabolism[46]和 European Journal of Endocrinology[47]同步發表的《2023 年國際基於循證醫學證據多囊卵巢綜合徵指南》 是目前的診斷指南。
-
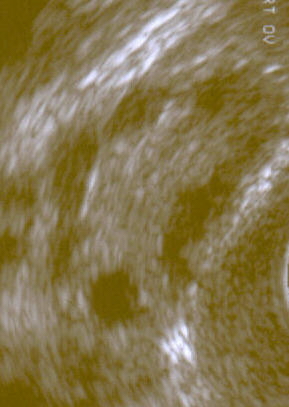
多囊卵巢在超聲波檢查上顯示的圖樣
-
多囊卵巢在陰道超聲波檢查上顯示的圖樣
-
多囊卵巢在超聲波檢查上顯示的圖樣
Remove ads
以下是兩種常見的定義:
- 在1990年,由國立衛生研究院 (美國)/ 美國國家兒童健康與人類發展中心贊助的協商研討會提出,如果一個人具有以下所有症狀,表示該人罹患多囊卵巢綜合症[48]:
- 出現排卵不規則的症狀
- 出現雄性素過剩的症狀 (臨床上或生化上)
- 排除可能導致月經不規則和雄激素過多的其他疾病導致上述症狀的產生
鹿特丹診斷標準涵蓋更廣泛的有症狀婦女,最顯著的部分是在於並未有雄性素過剩的婦女也被列入在其中。 評論家認為,從研究雄激素過多的婦女獲得的結果不一定可以推廣到給沒有雄激素過剩的婦女身上[51][52]。
- Androgen Excess PCOS Society
- 2006年,Androgen Excess PCOS Society提出了一套嚴謹診斷標準[15]:
- 具有雄性激素過剩症狀
- 出現排卵不規則、無排卵或多囊卵巢症狀,亦或同時出現上述症狀
- 排除會引起過量雄激素活性的其他因素*
應該調查其他原因,例如甲狀腺機能低下症、先天性腎上腺增生症(21-羥化酶缺乏症)、庫興氏症候群、高乳促素血症、雄激素分泌性腫瘤以及其他垂體或腎上腺疾病。[15][50]<[53]
處置
多囊卵巢綜合症的主要治療方法包括:調整生活方式及藥物治療[54]。
主要治療目標大致可分為下列四點:
目前現行療法中何為最佳治療方式仍是相當大的爭議,其中一個主要原因是因為缺乏比較不同療程療效的大規模臨床試驗。樣本往往是不太可靠因此可能產生矛盾不可靠的結果。
有助於減輕體重或降低胰島素抗性的一般干預措施對於改善多囊卵巢綜合症的症狀有益,體重增加與胰島素抗性被視為是潛在的病因。由於多囊卵巢綜合症有可能會引起嚴重的情緒障礙,因此適當的精神支持對於病情可能是有益的。[55]
當多囊卵巢綜合癥與超重或肥胖有關時,減肥是恢復規律月經的最有效方法,但是很多女性很難達到並維持顯著的體重減輕。2013年的科學評估發現,減肥,與飲食組成無關,可改善重量和體重組成、懷孕率、月經規律、排卵、雄激素過高、胰島素抗性、脂質以及生活質量。[56]即使如此,從水果、蔬菜和全穀物中獲得大部分碳水化合物的低GI飲食,相對於營養素均衡的健康飲食,仍能更好的改善月經規律。[56]
維生素D缺乏症可能在代謝症候群的發展中發揮一定的作用,故遵照醫囑補充缺乏的營養素是極為重要的[57][58]。然而,2015年的系統評估並沒有發現維生素D具有減輕多囊卵巢綜合症中代謝和激素失調情況的證據。[59]截至2012年,使用營養補充品預防多囊卵巢綜合症患者代謝缺陷的干預措施已經在小型、不受控制的和非隨機的臨床試驗中進行了測試;而所得數據不足以推薦使用。[60]
用於治療多囊卵巢綜合症的藥物有避孕藥及二甲雙胍。口服避孕藥能增加體內性激素結合球蛋白生產,促進游離睾酮的結合。這減少了由高睾丸激素引起的多毛症狀,並調節恢復正常月經週期。二甲雙胍是在2型糖尿病中常用的一種降低胰島素排斥的藥物,並在英國,美國,澳大利亞和歐盟仿單標示外使用用來治療多囊卵巢綜合症中的胰島素排斥。在許多情況下,二甲雙胍也能協助卵巢功能並恢復正常排卵[18][57][61]。螺內酯可用於其抗雄激素作用,而二氟甲基鳥氨酸則可用於減少面部毛髮。較新的胰島素抵抗藥物噻唑烷二酮(格列酮)顯示出與二甲雙胍相當的功效,但二甲雙胍具有更輕微的副作用[62][63]。 英國國家健康與照顧卓越研究院在2004年提出建議,當其他治療未能產生效果時,將給予給予BMI高於25的病患服用二甲雙胍[64][65]。二甲雙胍在每種類型的多囊卵巢綜合症中可能並非有效的,因此對於是否應該用作一般一線治療存在一些分歧[66]。羥甲基戊二酸單酰輔酶A還原酶抑制劑在治療潛在代謝綜合徵方面的應用尚不清楚[67]。
多囊卵巢綜合症可能導致難以受孕,因為它會導致不規律排卵。試圖懷孕時,會使用誘導生育的藥物包括排卵誘導劑克羅米酚或 脈衝亮丙瑞林 。 二甲雙胍與克羅米酚組合使用時,可提高生殖治療的療效。[68]二甲雙胍被認為在懷孕期間使用是安全的,於美國的懷孕分級為B[69]。2014年的評論得出結論,在三個月內使用二甲雙胍治療的女性並不會增加產下先天性障礙嬰兒的風險[70]。
如果病患目前沒有懷孕需求,可以藉由服用複合口服避孕藥來調節月經紊亂[18][57]。 調理生理週期的主要目的是讓女性生活上比較方便,改善女性對於生理週期與自己的感受;若能自然規律行經,便不需藉由服藥使生理週期變得規律。
如果不期望定期的月經週期,則不一定需要不規則循環的治療。大多數專家說,如果至少每三個月發生一次月經,那麼子宮內膜就會經常流下來,以防止增加子宮內膜異常或癌症的風險。[71]如果月經頻率極低或根本沒來,推薦使用某些形式的助孕素。[72]其中一種替代方案即是定期服用一次口服助孕素(例如,每三個月)以誘發可預測的月經出血。[18]
一篇2017年發表的科學論文指出肌醇與D-手性肌醇可能具有調節生理週期與改善排卵的功效,然而目前仍然缺乏其是否能影響懷孕機率的證據,一篇於2011年發表的綜述文章亦指出目前缺乏足夠的證據去證明D-手性肌醇具有任何功效。 [73][74][75]兩篇分別發表於2012年與2017年的綜述文章點出補充肌醇似乎能夠有效改善多囊性卵巢綜合症的幾種激素紊亂,且能降低採取體外受精之女性的促性腺激素釋放激素濃度與改善其卵巢過度刺激症的發作時間。[76][77][78]對於針灸是否能改善多囊性卵巢綜合症方面,目前仍然缺乏足夠的科學證據來證實其效用。[79][80]
預測
多囊性卵巢綜合症的高風險伴隨症狀:
- 可能發生子宮內膜增生症和子宮內膜癌,因為子宮內膜過度積累,且也缺乏黃體素導致雌激素對子宮細胞的刺激延遲[18][48][81]。這種風險是否直接歸因於綜合徵或相關的肥胖(高胰島素血症和雄激素過多症)還不清楚。[82][83][84]
- 胰島素抗性或第二型糖尿病[18]:2010年發表的一項論文得出,即使在控制身高體重指數(BMI)時,多囊性卵巢綜合症患者的胰島素抗性和II型糖尿病患病率也會升高。[48][85]多囊性卵巢綜合症也使一個女人,容易患有妊娠糖尿病,特別是肥胖症患者[18]。
- 高血壓,特別是肥胖或懷孕期間[18]。
- 憂鬱和焦慮[15][86]
- 血脂異常[18] (脂質代謝障礙 ) 膽固醇和三酸甘油酯。具有多囊卵巢綜合症的婦女顯示動脈粥樣硬化去除機制會減弱,導致殘餘物,似乎與胰島素抗性或II型糖尿病無關。[87]
- 心血管疾病[18][48]研究分析估計有多囊性卵巢綜合症患者的動脈疾病風險相對於沒有女性的2倍,與BMI無關[88]。
- 中風[48][48]
- 體重增加[18]
- 流產[89][90]
- 睡眠呼吸中止症,特別是肥胖症患者[18]
- 非酒精性脂肪肝,特別是肥胖症患者[18]
- 黑棘皮症(腋下,鼠蹊部與後頸出現暗色皮膚斑紋)[48]
- 自體免疫甲狀腺炎[91]
早期診斷和治療可能會降低其中一些風險,如II型糖尿病和心臟病。
卵巢癌和乳腺癌的風險總體上沒有顯著增加。[81]
流行病學
多囊性卵巢綜合症的盛行率受到診斷標準的影響。 世界衛生組織在2010年時估計全世界約有一億一千六百萬名女性(約3.4%的女性)受多囊性卵巢綜合症影響。[92]一份以鹿特丹診斷診斷指引為準的多囊性卵巢綜合症流行率社區研究發現,大約有百分之18的女性患有多囊性卵巢,而這些患者約有百分之70先前並未被確診出患有多囊性卵巢綜合症。[15]
約有百分之8到25的一般女性在超音波診斷中會看到有多囊性卵巢。[93][94][95][96]服用口服避孕藥的女性中,有14%發現有多囊性卵巢[94]。卵巢囊腫也是使用釋放黃體素的子宮環後常見的副作用。[97]
歷史
這種症狀最早在1935年由美國婦科醫生Irving F. Stein, Sr.與Michael L. Leventhal首次描述,其原始名稱為斯-李二氏症[43][48] 。
目前已知最早的多囊卵巢綜合症記錄,是1721年間源自義大利的記錄[17]。關於卵巢囊腫的相關變化描述最早出現在1844年[17]。
社會及文化
2005年在美國有約四百萬起多囊卵巢綜合症的病例,其醫療費用有43.6億美元[98]。2016年國立衛生研究院的研究預算有323億美元,其中有0.1%用在多囊卵巢綜合症的研究上[99]。
這種綜合徵的其他名稱包括多囊卵巢疾病、功能性卵巢雄激素過多症、卵巢濾泡膜細胞增殖、硬皮囊性卵巢綜合徵和斯-李二氏症。斯-李二氏症為其原始名稱,現在使用這個名稱都僅限於具有不孕症、多毛症、卵巢有多發囊狀腫大的閉經女性[43]。
這種疾病的名稱「多囊卵巢綜合症」是因為在醫學影像中可見多囊性卵巢而得此稱[18]。多囊性卵巢在靠近卵巢表面處有極大量正在發育的卵子,其在超音波中可用肉眼鑑別[43],看起來像許多小囊腫[100]。
參見
- 雄性素依賴症候群
- 《多囊卵巢綜合症挑戰》(真實改編電視劇)
參考文獻
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
Remove ads