實驗氣體定律 来自维基百科,自由的百科全书
波意耳-马略特定律(英语:Boyle's law,也称作Boyle–Mariotte law或Mariotte's law),在定量定温下,理想气体的体积与压力成反比。是由爱尔兰化学家罗伯特·波以耳,在1662年根据实验结果提出:“在密闭容器中的定量气体,在恒温下,气体的压强和体积成反比关系。”称之为波以耳定律:此定律实验结果首先由Henry Power[1] (页面存档备份,存于互联网档案馆)所发现。这是人类历史上第一个被发现的“定律”。马略特在1676年发表在《气体的本性》论文中:一定质量的气体在温度不变时其体积和压强成反比。波以耳和马略特这两人是各自分别独立确立定律的,因此在英语国家,这一定律被称为波义耳定律,而在欧洲大陆则被称为马略特定律。
这里
这个公式又可以继续推导,理想气体的体积与压强的乘积成为一定的常数。
如果在温度相同的状态下,A、B两种状态下的气体关系式可表示成。
习惯上,这个公式会写成
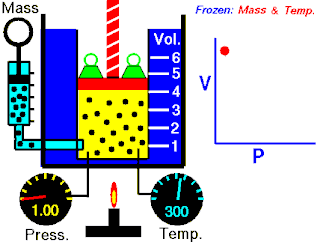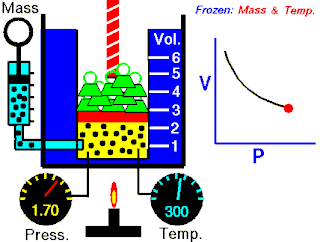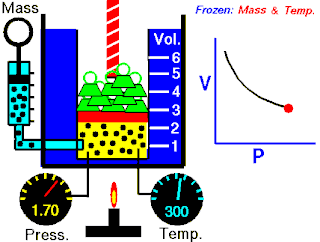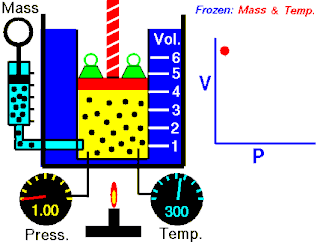
定律本身可以陈述如下:指出在恒定温度下的固定质量,绝对压力和气体的体积成反比。
当温度恒定时若体积增大,压力会减小,反之亦然。例如当体积减半,压力会加倍或是体积加倍,压力减半。
波意耳定律指出在恒定温度下的固定质量,绝对压力和气体的体积成反比。该法也可在稍微不同的方式表示,即绝对压力和体积总为常数。大多数气体于中等压力和温度下的表现如同理想气体。17世纪的技术不足无法产生高压或低温状况,所以波义耳定律于发表时并无偏差。而随科技进步,技术改良允许产生高压及低温的实验状况,理想气体于极度实验状况下的偏差可被显著的观察到,所以压力和容积之间的关系只能准确地描述实际气体理论。此偏差也可表示为压缩因子。
波意耳(和马略特)衍生的定律来自实验依据。该定律也可以由基于原子和分子存在理论、运动假设、完全弹性碰撞的假定存在的理论推导。这些假设是在实证主义科学界在当时遇到了巨大阻力,因为他们被视为纯粹的理论构建且毫无观测证据。
丹尼尔·伯努利在1737年至1738年用分子层面之牛顿运动定律得出波义耳定律 。而此结果被忽略直到1845年约翰·沃特斯顿发表的一篇动力学理论论文,然而此论文却被英国皇家学会拒绝。直到詹姆斯·普雷斯科特·焦耳,鲁道夫·克劳修斯以及路德维希·玻尔兹曼的作品才牢固建立了气体动力学理论并促使人们关注伯努利和沃特斯顿两者的理论。
能量学和原子论的支持者之间的争论引起波兹曼于1898年写一本书来厘清,而这本书经严厉批评导致波兹曼于1906年自杀。爱因斯坦在1905年发表理论动能适用于流体悬浮颗粒的布朗运动,此理论于1908年由让·佩蓝证实。
Seamless Wikipedia browsing. On steroids.