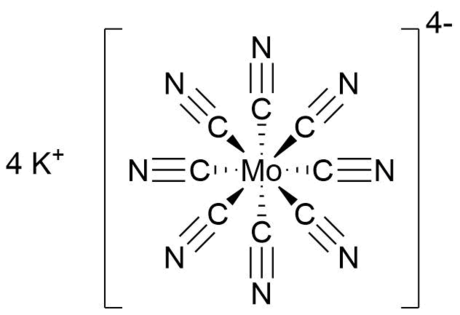
八氰合钼(IV)酸钾是一种无机化合物,化学式为K4[Mo(CN)8]。它是黄色固体,是一种氰均配物的钾盐,配位数为8。它常以二水合物K4[Mo(CN)8]·2H2O的形式存在。
| 八氰合钼(IV)酸钾 | |
|---|---|

| |

| |
| IUPAC名 Potassium octacyanidomolybdate(IV) | |
| 英文名 | Potassium octacyanomolybdate(IV) |
| 识别 | |
| CAS号 | 17456-18-7(无水) 17457-89-5(二水) |
| SMILES |
|
| 性质 | |
| 化学式 | K4[Mo(CN)8] |
| 摩尔质量 | 460.47 g·mol⁻¹ |
| 外观 | 黄色粉末 |
| 熔点 | >300 °C |
| 危险性 | |
GHS危险性符号
| |
| GHS提示词 | 警告 |
| H-术语 | H302, H315, H319, H335 |
| P-术语 | P261, P305+351+338 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备
八氰合钼(IV)酸钾可由硼氢化钾在乙酸和氰化钾的存在下还原钼酸盐制得。[1]这是最初的制备方法之一,钼酸盐在还原的同时,氰合钼(IV)酸盐原位生成,其产率在70%左右。由于反应原料较为便宜,它适用于较大剂量的制备。
- 4 MoO42- + 32 CN- + BH4- + 31 H+ → 4 [Mo(CN)8]4- + 16 H2O + H3BO3
另一种制备方法是以MoCl4(Et2O)2为原料和氰化钾反应,这一过程没有还原反应发生。[2]由于MoCl4(Et2O)2不如钼酸盐常见,这一方法只适用于少量制取八氰合钼(IV)酸钾。
- MoCl4(Et2O)2 + 8 KCN → K4[Mo(CN)8] + 4 KCl + 2 Et2O
化学性质
八氰合钼(IV)酸钾中的[Mo(CN)8]4−配离子会在强酸中会转化为黄色的潮湿敏感的异氢氰酸配合物[Mo(CNH)8]4+。[3]
- K4[Mo(CN)8] + 8 HSbF6 → [Mo(CNH)8][SbF6]4 + 4 KSbF6
它在光照下可以水解,并被空气中的氧气氧化为蓝色的K6[MoIV2MoVI(CN)8O6]·2H2O。[4]
它被电化学还原,可以得到K5[Mo(CN)8][5];用氢气在390 °C还原,则得到二价钼的配合物K4[Mo(CN)6][6]。
它和三甲基氯化锡在1:1水/四氢呋喃的混合溶液中反应,可以得到黄色的[(CH3)3Sn]4[Mo(CN)8]。[7]
- K4[Mo(CN)8] + 4 (CH3)3SnCl → [(CH3)3Sn]4[Mo(CN)8] + 4 KCl
参考文献
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.