Loading AI tools
来自维基百科,自由的百科全书
在有机化学中,环张力是当分子内的键结形成不正常角度时存在的不稳定类型。张力大多在小的环上,像是环丙烷和环丁烷这种其碳-碳-碳角度与近乎109°的理想值大大偏离的类型。.[1][2] 由于它们的高张力,使得这些小环的燃烧热升高了。
环张力是从角张力、皮策张力或构形张力,和外环张力或凡得瓦张力结合而来。角张力最简单的例子是小的环烷类像环丙烷和环丁烷,如下面所讨论的。此外,在无法被缓解的环系统中经常有重叠的情况。
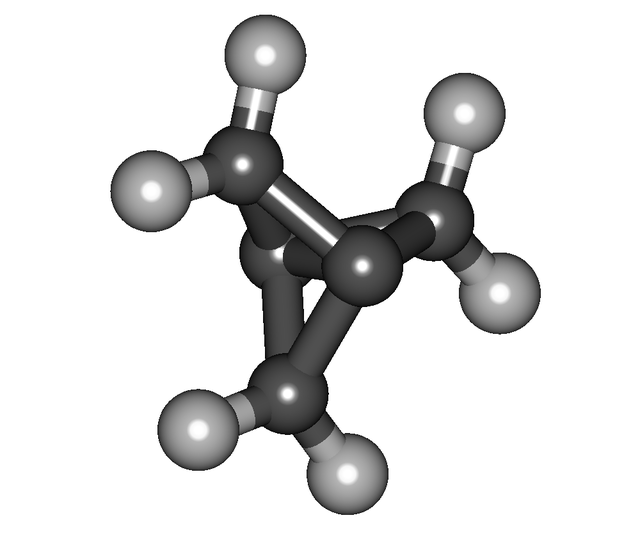
烷类
在烷类里,原子轨域的最理想重叠趋近于109.5°。最常见的环状化合物在它们的环上有五或六个碳。[3]阿道夫·冯·拜尔在1905年以拜耳张力学说获得诺贝尔奖,其解释了环状分子的相对稳定性。[3]
角张力发生在特定的化学结构中键角需要从理想的键结角度中改变以达到最大的键强度。因为环状分子缺乏非环状分子的弹性,所以角张力会对环状分子造成影响。角张力使分子变得不稳定,尤其是在高反应性和上升的燃烧热中更为明显。在化学键中原子轨域有效的重叠程度越大键的强度也会越大。角张力的定量测量方法为应变能。影响环状分子的环张力是由角张力和扭张力结合产生。[3]
让环张力之间做比较的常态能可从测量在环烷中一分子燃烧热的亚甲基而得知。[3]
每莫耳658.6 KJ的值是从一个不受张力影响的长链烷类获得的。.[3]
环烯类是sp2-混成的碳中心其扭曲所造成之张力的物质。图像是C60,其碳中心是金字塔形状。这个扭曲增强了此分子的反应性。角张力也是布莱特规则的基础,布莱特规则规定桥头碳中心在烯类里是不会合并在一起的,因为最终的烯类会是有极端角张力的物质。

在环烷类中,每一个碳是以非极性共价的方式和另外两个碳和两个氢作键结。碳上有sp3混成以及理想的角度109.5°。然而由于环状结构的限制,理想的角度只能以六碳环的方式达成—椅形的环己烷。对其他的环烷类来说,键角偏离了理想的状态。在环丙烷(3碳)和环丁烷(4碳)中的碳-碳键结各别是60°和~90°。
由三、四、和一些五元环所组成的有高度张力的分子,包括:环丙烷,环丙烯,环丁烷,环丁烯,[1,1,1]螺桨烷,[2,2,2]螺桨烷,环氧化合物,氮丙环,环戊烯,和降冰片烯。这些分子在环原子之间的键角比理想的四面体(109.5°)和三角平面(120°)里它们相对的sp3和sp2键结所形成的键角更加的尖锐。因为相对小的键角的关系,键结有比较高的能量,也可以接受含有更多的p-性质来减少键结的能量。此外,环丙烷/烯和环丁烷/烯的环型结构提供了非常少的构型弹性。因此,环原子的替代物存在于重叠构像的环丙烷中以及在环丁烷的间扭和重叠之间,并以凡得瓦力的形式提供高度的环张力能。
其他没有三和四元环的环烷烃可以受到张力的影响。这些包括了环芳,柏拉图烃,锥形的烯类,和环状炔烃。
有环张力的分子其键结中包含的位能和独特的键结构造可被用来驱动在有机合成中的反应。像这类的例子就有开环置换聚合反应,环丁烯的光诱导开环和环氧化合物与氮丙环的亲核开环反应。
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.