Kali sunfat (K2SO4) hay sunfat kali ở điều kiện thông thường là một muối ở dạng rắn kết tinh màu trắng không cháy và hòa tan trong nước. Nó được sử dụng khá phổ biến làm phân bón, cung cấp cả kali lẫn lưu huỳnh.
| Kali sunfat | |
|---|---|
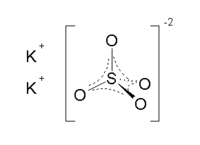 Công thức cấu tạo của kali sulfat | |
 | |
| Danh pháp IUPAC | Kali sulfat |
| Tên khác | Kali sunfat, sunphat kali |
| Nhận dạng | |
| Số CAS | |
| Thuộc tính | |
| Công thức phân tử | K2SO4 |
| Khối lượng mol | 174,2602 g/mol (khan) |
| Bề ngoài | Chất rắn kết tinh màu trắng |
| Khối lượng riêng | 2,66 g/cm³, khan |
| Điểm nóng chảy | 1.069 °C (1.342 K; 1.956 °F) |
| Điểm sôi | 1.689 °C (1.962 K; 3.072 °F) |
| Độ hòa tan trong nước | 11,1 g/100 ml (20 °C) |
| Cấu trúc | |
| Cấu trúc tinh thể | trực thoi |
| Các nguy hiểm | |
| MSDS | MSDS ngoài |
| Nguy hiểm chính | Kích ứng |
| Chỉ dẫn R | Không |
| Chỉ dẫn S | Không |
| Các hợp chất liên quan | |
| Anion khác | Kali bisunfat Kali sunfit Kali bisunfit Kali pesunfat |
| Cation khác | Lithi sunfat Natri sunfat Magie sunfat |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Lịch sử
Kali sunfat (K2SO4) được biết tới kể từ đầu thế kỷ 14, và nó được Glauber, Boyle và Tachenius nghiên cứu. Trong thế kỷ 17, nó được người phương Tây gọi là arcanuni hay sal duplicatum, do nó là tổ hợp của muối axit với muối kiềm.
Nguồn tự nhiên
Dạng khoáng vật của kali sunfat, gọi là arcanit, là tương đối hiếm. Các nguồn tự nhiên của kali sunfat là các khoáng vật phổ biến trong muối Stassfurt. Chúng là đồng kết tinh của kali sunfat với các sunfat của magie, calci và natri. Các khoáng vật đó là:
- Kainit MgSO4• KCl• H2O
- Schönit K2SO4•MgSO4•6H2O
- Leonit K2SO4•MgSO4•4H2O
- Langbeinit K2SO4•2MgSO4
- Glaserit K3Na(SO4)2
- Polyhalit K2SO4•MgSO4•2CaSO4•2H2O
Từ một số trong các khoáng vật nói trên, như kainit, kali sunfat có thể được tách ra, do muối tương ứng là ít hòa tan trong nước.
Với kali chloride, kieserit (MgSO4•2H2O) có thể bị chuyển hóa và sau đó kali sunfat có thể được hòa tan trong nước.
Sản xuất
- Phương pháp Hargreaves về cơ bản là quy trình tương tự nhưng với vật liệu khởi đầu khác biệt. Lưu huỳnh dioxide, oxy và nước (các vật liệu khởi đầu cho axit sunfuric) cho phản ứng với kali chloride. Hydro chloride tạo ra sẽ bay hơi đi.
- Kali sunfat được sản xuất bằng phản ứng của kali chloride và axit sunfuric.
Tính chất
Các tinh thể khan tạo thành một hình chóp sáu mặt kép, nhưng trên thực tế được phân loại là thoi. Chúng là các tinh thể trong suốt, rất cứng và có vị mặn đắng. Muối này hòa tan trong nước, nhưng không hòa tan trong các dung dịch kali hydroxide (tỷ trọng riêng 1,35), hoặc trong cồn khan. Nó nóng chảy ở 1.078 °C.
Sử dụng
Ứng dụng chính của kali sunfat là làm phân bón. Muối thô đôi khi cũng được dùng trong sản xuất thủy tinh.
Xem thêm
- Arcanum duplicatum, thuật ngữ để chỉ kali sunfat trong giả kim thuật
Tham khảo
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
