Хлорати
аніон З Вікіпедії, вільної енциклопедії
Хлора́ти — група хімічних сполук, солі хлоратної кислоти HClO3. Дані сполуки є білими, легкорозчинними кристалами. При спіканні проявляють сильні окисні властивості і дещо менші у розчинах. Хлорати мають здатність до детонації і є токсичними речовинами.
| Хлорати | |
 | |
 | |
| Маса | 1,4E−25 кг[1] |
|---|---|
| Спряжена кислота | Хлоратна кислота |
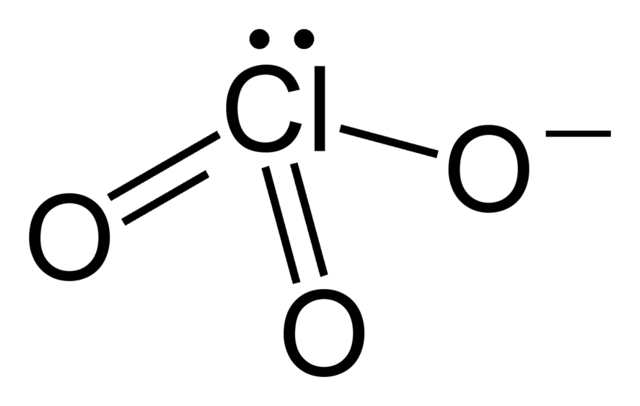
| Хімічна формула | ClO₃⁻ |
| Канонічна формула SMILES | [O-]Cl(=O)=O[1] |
| Хлорати у Вікісховищі | |

Застосовуються як окисники в піротехніці, у синтезі ClO2 та як гербіциди.
Хлорат-аніон має структуру тригональної піраміди (d(Cl-О) = 0,1452-0,1507 нм, кут O-Cl-O = 106°). Аніон ClO–
3 не утворює ковалентних зв'язків через атом О і не схильний утворювати координаційні зв'язки.
Будова та фізичні властивості

Хлорати є, як правило, кристалічними речовинами, розчинними у воді та деяких полярних органічних розчинниках. В твердому стані при кімнатній температурі досить стабільні. При нагріванні в присутності каталізатору розкладаються з виділенням кисню.
З горючими речовинами можуть утворювати вибухові суміші. Хлорати є сильними окисниками як у розчині, так і в твердому стані: суміші безводних хлоратів із сіркою, вугіллям та іншими відновниками, вибухають при швидкому нагріванні і ударі. Хлорати металів змінної валентності зазвичай нестійкі і схильні до вибухового розпаду. Всі хлорати лужних металів розкладаються з виділенням великої кількості тепла на хлориди і кисень, з проміжним утворенням перхлоратів.
Хлорати більшості металів отримані у вигляді гідратів, в безводному стані виділені хлорати лужних та лужноземельних металів, Ag, Tl(I), Pb(II), а також NH4ClO3, N(CH3)4ClO3.
Одержання
Узагальнити
Перспектива
У промислових масштабах хлорати (в першу чергу, натрію та меншою мірою калію) добувають шляхом електролізу водних розчинів відповідних хлоридів:
Менш поширені хлорати, наприклад, хлорати важких металів, добувають реакцією обміну:
Практично втратив своє значення давній спосіб отримання хлоратів, який полягає у пропусканні хлору крізь розчини гідроксидів металів. Реакцію проводять із гарячими розчинами, в іншому випадку замість хлоратів утворюватимуться гіпохлорити.
Хімічні властивості
Узагальнити
Перспектива
При нагріванні хлорати розкладаються; продукти реакції залежать від умов: просте нагрівання спричинює диспропорціонують з утворенням хлоридів та перхлоратів, а в присутності каталізатору (MnO2) утворюються хлорид металу та виділяється кисень:
При взаємодії солей з концентрованою хлоридною кислотою виділяється хлор:
Реакція хлоратів із відновниками (на кшталт метанолу або діоксиду сірки) є основою для синтезу оксиду хлору(IV):
Застосування
Основним застосуванням хлоратів є синтез оксиду хлору(IV) для відбілювання тканин і паперу. Деякі хлорати, наприклад, хлорат амонію NH4ClO3, використовуються як окисники у виробництві твердих пропелентів та очистці урану.
Хлорат калію широко використовується у виготовленні піротехніки, сірників, косметики тощо. Над більш поширеним хлоратом натрію він має перевагу у значно меншій гігроскопічності. Хлорат кальцію застосовується як гербіцид.
Також із хлоратів добувають невеликі кількості кисню для потреб лабораторій.
Див. також
Посилання
Вікісховище має мультимедійні дані за темою: Хлорати
Джерела
Wikiwand - on
Seamless Wikipedia browsing. On steroids.








