
Фосген
хімічна сполука / З Вікіпедії, безкоштовно encyclopedia
Шановний Wikiwand AI, Давайте зробимо це простіше, відповівши на ключові запитання:
Чи можете ви надати найпопулярніші факти та статистику про Фосген?
Підсумуйте цю статтю для 10-річної дитини
Фосге́н — хімічна сполука ряду оксогалогенідів складу COCl2. За звичайних умов є безбарвною газоподібною речовиною із запахом прілих фруктів або сіна. Як сильний електрофіл бере участь у реакції Фріделя — Крафтса. Проявляє сильні хлорувальні властивості.
| Фосген | |
|---|---|
 |
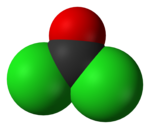 |
| Назва за IUPAC | Карбоніл дихлорид |
| Інші назви | оксохлорид вуглецю, хлорангідрид карбонатної кислоти |
| Ідентифікатори | |
| Номер CAS | 75-44-5 |
| Номер EINECS | 200-870-3 |
| Назва MeSH | D02.522.741 |
| ChEBI | 29365 |
| RTECS | SY5600000 |
| SMILES | C(=O)(Cl)Cl[1] |
| InChI | InChI=1S/CCl2O/c2-1(3)4 |
| Номер Бельштейна | 1098367 |
| Властивості | |
| Молекулярна формула | COCl2 |
| Молярна маса | 98,915 г/моль |
| Зовнішній вигляд | безбарвний газ безбарвна рідина білі кристали |
| Густина | 4,043 г/л (газ, 25 °C)[2] 1,4203 г/мл (рідина, 0 °C) 1,373 г/мл (рідина, 20 °C) |
| Тпл | -127,78 °C[2] |
| Ткип | 7,56 °C (760 мм рт. ст.) -30 °C (137 мм рт. ст.) |
| Розчинність (вода) | 0,9% (у холодній воді) |
| Структура | |
| Координаційна геометрія |
планарна |
| Геометрія | тригональна |
| Термохімія | |
| Ст. ентальпія утворення ΔfH 298 |
-220 кДж/моль |
| Небезпеки | |
| Температура спалаху | не займистий |
| Пов'язані речовини | |
| Пов'язані речовини | дифосген, тіофосген |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |

Сполука була відкрита у 1811 році британським хіміком Джоном Деві. З 1915 року фосген у суміші з хлором почав застосовуватися у військових протистояннях Німеччиною. У подальшому сполука застосовувалася у чистому вигляді. Були зафіксовані акти хімічної атаки італійською армією у 1935 році та японською — у 1937—1945 роках.
У 1993 році, в результаті підписання Конвенції про хімічну зброю, використання фосгену як хімічної зброї було заборонено. Його включили до списку 3, котрий регламентує виробництво та обіг небезпечних речовин.[3]
Фосген застосовується у виробництві пестицидів, пластмас, барвників, безводних оксидів металів.