Loading AI tools
З Вікіпедії, вільної енциклопедії
Механі́зм Гро́ттгусса — механізм переносу протонів чи протонних дефектів в середовищі, де наявний водневий зв'язок. Цей механізм відіграє важливу роль при описанні переносу протону в біологічних реакціях.
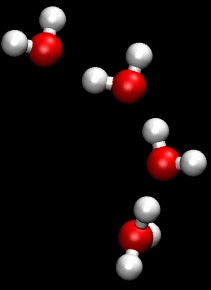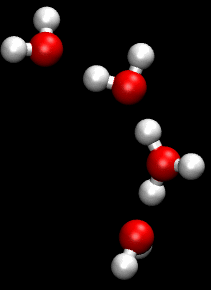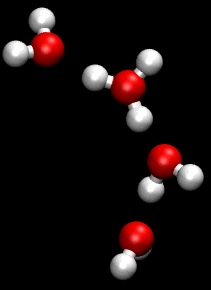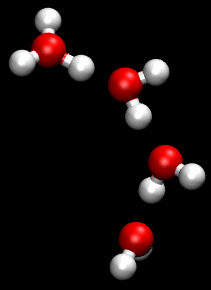
Модель була запропонована в 1805 році литовським вченим Теодором фон Гроттгуссом, який вперше застосував її до процесу електрохімічного розкладу води на водень і кисень. Гроттгусс уявляв молекули води у вигляді диполів, які розташовані ланцюжком між катодом і анодом електролізеру. Далі він припускав, що при електролізі позитивний кінець диполю води, який направлено до катоду, відщеплюється і з нього утворюється водень. Аналогічно відбувається відщіплення негативного кінця диполю з утворенням кисню. Після цього відбувається перегрупування позитивних і негативних кінцівок диполю в ланцюгу. Новий ланцюг диполів виявляється орієнтованим проти зовнішнього поля і диполі переорієнтовуються. Після поповнення числа диполів за рахунок молекул води з об'єму розчину, що не знаходиться між електродами, попередній ланцюг відновлюється та процес повторюється. Коли Гроттгусс вперше опублікував свою теорію в роботі «Theory of decomposition of liquids by electrical currents» (1806)[1] атомістика ще тільки завойовувала своє право на існування; закони електролізу залишались невідомими. Тому теорія Гротгуса була дуже сміливою та передовою для свого часу. Вона протрималась в науці більше сімдесяти років, коли її змінило уявлення про йони, яке краще відображало реальність.
Цей «естафетний механізм» електропровідності має багато спільного з механізмом переносу струму йонами Н3О+ та ОН-, але для більшості електролітів він виявився непридатним.

На сьогоднішній день поняття механізм Гротгуса застосовують як загальну назву для механізмів стрибку протонів. Вільні протони, завдяки своєму дуже малому радіусу в розчині моментально зв'язуються з молекулами води та утворюють йони гідроксонію (H3O+). Якщо співвідношення концентрацій дозволяють, може спостерігатися зв'язок іонів гідроксонію з декількома молекулами води. Окрім йону гідроксонію в розчині присутні катіон Цунделя (H5O2 +) та катіон Ейгена (H9O4 +). Перенос протону обумовлений взаємодією між цими двома катіонами, але механізм переносу досі не встановлено. Найбільш вірогідними є два механізми:
Молекули води здатні до іонізації з утворенням іону водню (протону) і гідроксильних іонів:
Хоча Н+ в реакції є продуктом дисоціації, однак, в реальності вільних протонів в розчині не існує. Утворені іони водню одразу ж гідратуються в іони гідроксонію Н3О+, це відбувається миттєво за рахунок водневих зв'язків між молекулами води.
Рух протону на далеку відстань сам по собі є неможливим. Але через наявність великого числа протонів між молекулами води, пов'язаних водневими містками, може спостерігатися картина, коли в доволі короткий час відбувається "стрибок протону" на великі відстані.
У результаті високої мобільності Н+, кислотно-основні реакції у водному розчині, як правило, виключно швидкі. Стрибок протону пояснюється високою іонною рухливістю іонів Н+ в порівнянні з іншими одновалентними катіонами, такими як Na+ або K+.
Механізм Гротгуса заснований на припущенні, що це не один конкретний перехід протону від однієї молекули до іншої, а що стрибок протону до однієї молекули призводить до стрибка іншого протону з цієї молекули.
Механізм Гротгуса' пояснює аномально великі значення коефіцієнтів дифузії протонів в порівнянні з коефіцієнтами дифузії різноманітних йонів.
В таблиці наведено коефіцієнти дифузії катіонів, пов'язані з тепловими коливаннями (Броунівський рух).
| Катіон | Рухомість, см2·В−1·с−1 |
|---|---|
| NH4+ | 0,763·10−3 |
| Na+ | 0,519·10−3 |
| K+ | 0,762·10−3 |
| H+ | 3,62·10−3 |
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.