Loading AI tools
Vikipedi'den, özgür ansiklopediden
Fosforil klorür (genellikle fosfor oksiklorür olarak adlandırılır), POCl
3 formülüne sahip bir sıvıdır. Nemli havada hidrolize olup fosforik asit ve hidrojen klorür dumanı açığa çıkarır. Endüstriyel olarak büyük ölçekte fosfor triklorür ve oksijen veya fosfor pentoksitten üretilir.[4] Esas olarak fosfat esterleri yapmak için kullanılır.
 | |||
| |||
 | |||
| Adlandırmalar | |||
|---|---|---|---|
Tercih edilen IUPAC adı Fosforil triklorür[1] | |||
Diğer adlar
| |||
| Tanımlayıcılar | |||
3D model (JSmol) |
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.030 | ||
| EC Numarası |
| ||
| 2272 | |||
PubChem CID |
|||
| RTECS numarası |
| ||
| UNII | |||
| UN numarası | 1810 | ||
CompTox Bilgi Panosu (EPA) |
|||
| |||
| |||
| Özellikler | |||
| Kimyasal formül | Cl3OP | ||
| Molekül kütlesi | 153,33 g mol−1 | ||
| Görünüm | dumanlı, renksiz sıvı | ||
| Koku | keskin, rutubet benzeri | ||
| Yoğunluk | 1,645 g/cm3, sıvı | ||
| Erime noktası | 125 °C (257 °F; 398 K) | ||
| Kaynama noktası | 1.058 °C (1.936 °F; 1.331 K) | ||
| Çözünürlük (su içinde) | tepkir | ||
| Çözünürlük | benzen, kloroform, karbon disülfür ve karbon tetraklorürde çözünür | ||
| Buhar basıncı | 40 mmHg (27 °C)[2] | ||
| Kırınım dizimi (nD) | 1.460 | ||
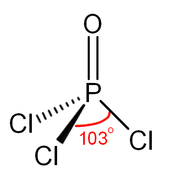
| Yapı | |||
| Fosfor atomundan Tetrahedral | |||
| Dipol momenti | 2.54 D | ||
| Termokimya[3] | |||
Isı sığası (C) |
138.8 J·mol−1·K−1 (sıvı), 84.9 J·mol−1·K−1 (gaz) | ||
Standart molar entropi (S⦵298) |
222.5 J·mol−1·K−1 (sıvı), 325.5 J·mol−1·K−1 (gaz) | ||
Standart formasyon entalpisi (ΔfH⦵298) |
−597.1 kJ·mol−1 (sıvı), −558.5 kJ·mol−1 (gaz) | ||
Gibbs serbest enerjisi (ΔfG⦵) |
−520.8 kJ·mol−1 (sıvı), −512.9 kJ·mol−1(gaz) | ||
Füzyon entalpisi (ΔfH⦵fus) |
13.1 kJ·mol−1 | ||
Buharlaşma entalpisi (ΔfHvap) |
38.6 kJ·mol−1 | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | Zehirli ve aşındırıcı[2] | ||
| GHS etiketleme sistemi: | |||
| Piktogramlar |     | ||
| İşaret sözcüğü | Danger | ||
| Tehlike ifadeleri | H302, H314, H330, H372 | ||
| Önlem ifadeleri | P260, P264, P270, P271, P280, P284, P301+P312, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P310, P314, P320, P321, P330, P363, P403+P233, P405, P501 | ||
| NFPA 704 (yangın karosu) |
|||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz) |
380 mg/kg (rat, oral) | ||
| NIOSH ABD maruz kalma limitleri: | |||
| PEL (izin verilen) | none[2] | ||
| REL (tavsiye edilen) | TWA 0.1 ppm (0.6 mg/m3) ST 0.5 ppm (3 mg/m3)[2] | ||
| IDLH (anında tehlike) | N.D.[2] | ||
| Güvenlik bilgi formu (SDS) | ICSC 0190 | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
| Bilgi kutusu kaynakları | |||

Fosfat gibi, POCl
3 tetrahedral şeklindedir.[6] Tahminî bağ ayrışma enerjisi 533,5 kJ/mol olan üç P−Cl bağı ve bir güçlü P–O bağı içerir. POF
3 durumundan farklı olarak, Schomaker-Stevenson kuralı, P–O bağı için uygun bağ uzunluğunu yalnızca P–O bağının çift bağ olarak ele alınması durumunda (P=O) öngörür.

Kristal yapısındaki ortalama bağ uzunlukları P–Cl arası 1,98 Å ve P=O için ise 1,46 Å'dür.[5]
3,4 atm kritik basınca sahiptir.[7] Donma noktası 1 °C ve kaynama noktası 106 °C olan POCl
3'ün sıvı aralığı suya oldukça benzer. Ayrıca su gibi POCl
3 de tersinir oluşumu nedeniyle [POCl
2]+
(diklorooksofosfonyum) katyonu ve Cl−
anyonlarınaotoiyonize olur.
POCl
3 suyla tepkimeye girerek hidrojen klorür ve fosforik asit verir:
Pirofosforil klorür O(−P(=O)Cl
2)
2 de dâhil olmak üzere dönüşümdeki ara maddeler izole edilmiştir.[8]
Fazla alkol ve fenollerle muamele üzerine, POCl
3 onların fosfat esterlerini verir:
Bu tür reaksiyonlar sıklıkla piridin veya bir amin gibi bir HCl alıcısının varlığında gerçekleştirilir.
Alüminyum klorür kompleksi (POCl
3·AlCl
3 ) oldukça kararlıdır ve bu nedenle (örneğin bir Friedel-Crafts reaksiyonunun sonunda) reaksiyon karışımlarından POCl
3 çıkarmak için kullanılabilir.
Fosforil klorür birçok yöntemle hazırlanabilir. Fosforil klorür ilk olarak 1847'de Fransız kimyager Adolphe Wurtz tarafından fosfor pentaklorürün suyla reaksiyona sokulmasıyla elde edildi.[9]
Ticari yöntem, fosfor triklorürün oksijenle oksidasyonunu içerir:
Alternatif bir yöntem, fosfor triklorürün potasyum klorat ile oksidasyonunu içerir:[10]
Fosfor pentaklorürün fosfor pentoksit ile reaksiyonu:
Klor gazı varlığında trikalsiyum fosfatın karbonla indirgenmesi:[11]
Fosfor pentoksidin sodyum klorür ile reaksiyonu da fosforil klorür verebilir:[11]
Fosforil klorür, fosfat esterlerinin (organofosfatlar) üretimi için endüstriyel ölçekte kullanılır. Bunlar, alev geciktiriciler (bisfenol A difenil fosfat, TCPP ve trikresil fosfat), PVC ve ilgili polimerler için plastikleştiriciler (2-etilheksil difenil fosfat) ve hidrolik sıvılar dahil olmak üzere geniş bir kullanım alanına sahiptir. POCl3 ayrıca organofosfat insektisitlerin üretiminde de kullanılır.
Yarı iletken endüstrisinde POCl
3 difüzyon proseslerinde güvenli bir sıvı fosfor kaynağı olarak kullanılır. Fosfor, silikon levha üzerinde katmanlar oluşturmak için kullanılan bir katkı maddesi görevi görür.
Laboratuvarda, POCl
3 dehidrasyonlarda bir reaktif görevi görür. Bir örnek, formamidlerin izonitrillere (izosiyanürler) dönüştürülmesini içerir;[12] birincil amidlerden nitrillere:[13]
İlgili bir reaksiyonda, bazı aril ikameli amidler Bischler-Napieralski reaksiyonu kullanılarak halkaya dönüştürülebilir.
Bu tür reaksiyonların bir imidoil klorür yoluyla ilerlediğine inanılmaktadır. Bazı durumlarda imidoil klorür nihai üründür. Örneğin piridonlar ve pirimidonlar, ilaç endüstrisinde ara ürünler olan 2-kloropiridinler ve 2-kloropirimidinler gibi kloro-türevlerine dönüştürülebilir.[14]
Vilsmeier-Haack reaksiyonunda POCl
3 amidlerle reaksiyona girerek bir "Vilsmeier reaktifi", bir kloro-iminyum tuzu üretir ve bu daha sonra sulu işlem sonrasında aromatik aldehitler üretmek üzere elektron açısından zengin aromatik bileşiklerle reaksiyona girer.[15]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.