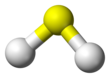
ไฮโดรเจนซัลไฟด์
จากวิกิพีเดีย สารานุกรมเสรี
ไฮโดรเจนซัลไฟด์ (อังกฤษ: hydrogen sulfide หรือ hydrogen sulphide) หรือ แก๊สไข่เน่า เป็นสารประกอบที่มีสูตรเคมีเป็น H2S ไม่มีสี, เป็นพิษ และเป็นแก๊สไวไฟ มีกลิ่นเน่าเหม็นคล้ายไข่เน่า[11] บ่อยครั้งเป็นผลจากแบคทีเรียย่อยสลายซัลไฟต์ในสารอนินทรีย์ในสภาวะขาดออกซิเจน เช่นใน หนองน้ำและท่อระบายน้ำ (การย่อยสลายแบบไม่ใช้ออกซิเจน) นอกจากนั้นยังพบในแก๊สจากภูเขาไฟ ก๊าซธรรมชาติ และบ่อน้ำบางบ่อ กลิ่นของ H2S ไม่ใช่คุณสมบัติโดยทั่วไปของกำมะถัน ซึ่งในความจริงแล้วไม่มีกลิ่น
 | |||
| |||
| ชื่อ | |||
|---|---|---|---|
| Systematic IUPAC name
Hydrogen sulfide[1] | |||
ชื่ออื่น
| |||
| เลขทะเบียน | |||
3D model (JSmol) |
|||
| 3DMet | |||
Beilstein Reference |
3535004 | ||
| ChEBI | |||
| ChEMBL | |||
| เคมสไปเดอร์ | |||
| ECHA InfoCard | 100.029.070 | ||
| EC Number |
| ||
Gmelin Reference |
303 | ||
| KEGG | |||
| MeSH | Hydrogen+sulfide | ||
ผับเคม CID |
|||
| RTECS number |
| ||
| UNII | |||
| UN number | 1053 | ||
CompTox Dashboard (EPA) |
|||
InChI
| |||
SMILES
| |||
| คุณสมบัติ | |||
| H2S | |||
| มวลโมเลกุล | 34.08 g·mol−1 | ||
| ลักษณะทางกายภาพ | แก๊สไร้สี | ||
| กลิ่น | เหม็นฉุนเหมือนไข่เน่า | ||
| ความหนาแน่น | 1.539 g.L−1 (0°C)[2] | ||
| จุดหลอมเหลว | −85.5[3] องศาเซลเซียส (−121.9 องศาฟาเรนไฮต์; 187.7 เคลวิน) | ||
| จุดเดือด | −59.55[3] องศาเซลเซียส (−75.19 องศาฟาเรนไฮต์; 213.60 เคลวิน) | ||
| 3.980 g dm−3 (ที่ 20 °C) [4] | |||
| ความดันไอ | 1740 kPa (at 21 °C) | ||
| pKa | 7.0[5][6] | ||
| กรด | Sulfonium | ||
| เบส | Bisulfide | ||
Magnetic susceptibility (χ) |
−25.5·10−6 cm3/mol | ||
ดัชนีหักเหแสง (nD) |
1.000644 (0 °C)[2] | ||
| โครงสร้าง | |||
กลุ่มจุด |
C2v | ||
รูปร่างโมเลกุล |
โค้ง | ||
Dipole moment |
0.97 D | ||
| อุณหเคมี | |||
ความจุความร้อน (C) |
1.003 J K−1 g−1 | ||
Std molar entropy (S⦵298) |
206 J mol−1 K−1[7] | ||
Std enthalpy of formation (ΔfH⦵298) |
−21 kJ mol−1[7] | ||
| ความอันตราย | |||
| อาชีวอนามัยและความปลอดภัย (OHS/OSH): | |||
อันตรายหลัก |
ติดไฟและเป็นพิษสูง | ||
| GHS labelling: | |||
Pictograms |
   | ||
Signal word |
อันตราย | ||
Hazard statements |
H220, H330, H400 | ||
Precautionary statements |
P210, P260, P271, P273, P284, P304+P340, P310, P320, P377, P381, P391, P403, P403+P233, P405, P501 | ||
| NFPA 704 (fire diamond) | |||
| จุดวาบไฟ | −82.4 องศาเซลเซียส (−116.3 องศาฟาเรนไฮต์; 190.8 เคลวิน)[8] | ||
อุณหภูมิที่ ติดไฟได้เอง |
232 องศาเซลเซียส (450 องศาฟาเรนไฮต์; 505 เคลวิน) | ||
| ขีดจำกัดการระเบิด | 4.3–46% | ||
| ปริมาณหรือความเข้มข้น (LD, LC): | |||
LC50 (median concentration) |
| ||
LCLo (lowest published) |
| ||
| NIOSH (US health exposure limits): | |||
PEL (Permissible) |
C 20 ppm; 50 ppm [สูงสุด 10 นาที][10] | ||
REL (Recommended) |
C 10 ppm (15 mg/m3) [10 นาที][10] | ||
IDLH (Immediate danger) |
100 ppm[10] | ||
| สารประกอบอื่นที่เกี่ยวข้องกัน | |||
hydrogen chalcogenidesที่เกี่ยวข้อง |
| ||
สารประกอบที่เกี่ยวข้อง |
ฟอสฟีน | ||
หากมิได้ระบุเป็นอื่น ข้อมูลข้างต้นนี้คือข้อมูลสาร ณ ภาวะมาตรฐานที่ 25 °C, 100 kPa
| |||
คาร์ล วิลเฮ็ล์ม เชเลอ นักเคมีชาวสวีเดนเป็นผู้ค้นพบไฮโดรเจนซัลไฟด์ในปี 1777
คุณสมบัติ
ไฮโดรเจนซัลไฟด์หนาแน่นกว่าอากาศเล็กน้อย ส่วนผสมระหว่าง H2S กับอากาศ สามารถระเบิดได้ เมื่อไฮโดรเจนซัลไฟด์เผาไหม้ในออกซิเจนจะให้เปลวไฟสีน้ำเงินและเกิดซัลเฟอร์ไดออกไซด์กับน้ำเป็นผลิตภัณฑ์ดังสมการ
2H2S + 3O2 → 2SO2 + 2H2O
โดยทั่วไปแล้วไฮโดรเจนซัลไฟด์มีฤทธิ์เป็นตัวรีดิวซ์ โดยเฉพาะเมื่ออยู่ในสภาวะเบส ซึ่งจะอยู่ในรูป SH-
ในอุณหภูมิสูง หรือเมื่อมีตัวเร่งปฏิกิริยาไฮโดรเจนซัลไฟด์สามารถทำปฏิกิริยากับซัลเฟอร์ไดออกไซด์เกิดเป็นกำมะถันและน้ำดังสมการ
2H2S + SO2 → 3S + 2H2O
ปฏิกิริยาดังกล่าว ใช้ในกระบวนการเคลาส์ ซึ่งเป็นกระบวนการสำคัญสำหรับกำจัดไฮโดรเจนซัลไฟด์ในภาคอุตสากรรม
ไฮโดรเจนซัลไฟด์ละลายน้ำได้เล็กน้อย และสามารถแสดงฤทธิ์เป็นกรดได้ (pKa = 6.9 ในสารละลาย 0.01-0.1M ที่ 18 °C) สารละลายของไฮโดรเจนซัลไฟด์ไม่มีสี แต่เมื่อถูกอากาศ จะถูกออกซิไดส์อย่างช้า ๆ เกิดความขุ่นจากกำมะถันซึ่งไม่ละลายน้ำ
ไฮโดรเจนซัลไฟด์ทำปฏิกิริยากับโลหะหลายชนิดเกิดเป็นเกลือซัลไฟด์ ซึ่งมักเป็นสีดำและไม่ละลายน้ำ ดังนั้นจึงมักใช้กระดาษชุบเลด(II)แอซิเตตในการทดสอบไฮโดรเจนซัลไฟด์ การนำโลหะซัลไฟด์ไปใส่กรดมักเกิดแก๊สไฮโดรเจนซัลไฟด์
การผลิต
ไฮโดรเจนซัลไฟด์ โดยทั่วไปแล้วผลิตโดยการแยกจากแก๊สธรรมชาติที่มี H2S ปน นอกจากนี้ยังอาจผลิตโดยปฏิกิริยาระหว่างไฮโดรเจนกับกำมะถันเหลวที่อุณหภูมิที่ 450 °C ซึ่งอาจใช้ไฮโดรคาร์บอนเป็นแหล่งคาร์บอนได้[12]
แบคทีเรียที่รีดิวซ์ซัลเฟตหรือซัลเฟอร์ สามารถสร้างพลังงานในสภาวะออกซิเจนต่ำโดยใช้ซัลเฟตหรือซัลเฟอร์เพื่อออกซิไดส์สารประกอบอินทรีย์ของไฮโดรเจน และเกิด H2S เป็นผลพลอยได้
วิธีการสังเคราะห์ปกติในห้องปฏิบัติการ ใช้ไอเอิร์น(II)ซัลไฟด์กับกรดแก่ ดังสมการ
FeS + 2 HCl → FeCl2 + H2S
ในการวิเคราะห์สารอนินทรีย์เชิงคุณภาพ สามารถใช้ไทโออะเซตาไมด์ในการผลิต H2S:
CH3C(S)NH2 + H2O → CH3C(O)NH2 + H2S
ซัลไฟด์ของธาตุโลหะและอโลหะหลายชนิด เช่น อะลูมิเนียมซัลไฟด์ ฟอสฟอรัสเพนตะซัลไฟด์ และซิลิคอนไดซัลไฟด์ เมื่อโดนน้ำแล้วจะให้ไฮโดรเจนซัลไฟด์:
Al2S3 + 6 H2O → 3 H2S + 2 Al(OH)3
P4S10 + 16 H2O → 10 H2S + 4 H3PO4
SiS2 + 2 H2O → 2 H2S + SiO2
นอกจากนี้ไฮโดรเจนซัลไฟด์ยังผลิตได้จากการให้ความร้อนกับกำมะถันกับสารอินทรีย์ หรือการรีดิวซ์สารอินทรีย์ที่มีกำมะถันด้วยไฮโดรเจน
การใช้งาน
การผลิตกำมะถัน สารประกอบอินทรีย์ที่มีกำมะถัน และซัลไฟด์ของโลหะแอลคาไล
ประโยชน์สำคัญของไฮโดรเจนซัลไฟด์ คือการเป็นสารตั้งต้นในการผลิตธาตุกำมะถัน สารออร์กาโนซัลเฟอร์หลายชนิดก็ผลิตจากไฮโดรเจนซัลไฟด์ เช่น มีเทนไทออล อีเทนไทออล และกรดไทโอไกลโคลิก
เมื่อทำปฏิกิริยากับเบสของโลหะแอลคาไล ไฮโดรเจนซัลไฟด์จะเกิดเป็นเกลือไฮโดรซัลไฟด์และซัลไฟด์ตามลำดับ เช่น:
- H2S + NaOH → NaSH + H2O
- NaSH + NaOH → Na2S + H2O
ซึ่ง NaSH และ Na2S มีประโยชน์ในอุตสาหกรรมกระดาษ โดยไปทำลายพันธะในเยื่อเคมีในกระบวนการคราฟท์
ในทางกลับกัน เกลือเหล่านี้สามารถเกิดปฏิกิริยากลับไปเป็นไฮโดรเจนซัลไฟด์ในกรดได้ จึงใช้เป็นแหล่งให้ไฮโดรเจนซัลไฟด์ในการสังเคราะห์สารอินทรีย์บางตัว
อ้างอิง
ข้อมูลเพิ่มเติม
แหล่งข้อมูลอื่น
Wikiwand - on
Seamless Wikipedia browsing. On steroids.