From Wikipedia, the free encyclopedia
வெள்ளி ஆக்சைடானது (Silver(I) oxide) Ag2O என்ற மூலக்கூற்று வாய்ப்பாட்டை உடைய வேதிச் சேர்மம் ஆகும். இது ஒரு நுண்ணிய துகள்களால் ஆன கருமை அல்லது அடர் பழுப்பு நிறமுடைய சேர்மம் ஆகும். இது மற்ற வெள்ளி சேர்மங்களைத் தயாரிக்கப் பயன்படுகிறது.
 | |
 | |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
வெள்ளி(I) ஆக்சைடு | |
| வேறு பெயர்கள்
வெள்ளி துரு, அர்ஜெண்டியஸ் ஆக்சைடு, வெள்ளி மோனாக்சைடு | |
| இனங்காட்டிகள் | |
| 20667-12-3 | |
| ChemSpider | 7970393 |
| EC number | 243-957-1 |
InChI
| |
| யேமல் -3D படிமங்கள் | Image |
| ம.பா.த | silver+oxide |
| பப்கெம் | 9794626 |
| வே.ந.வி.ப எண் | VW4900000 |
| |
| பண்புகள் | |
| Ag2O | |
| வாய்ப்பாட்டு எடை | 231.74 g·mol−1 |
| தோற்றம் | கருப்பு/பழுப்பு கனசதுர படிகங்கள் |
| மணம் | Odorless[1] |
| அடர்த்தி | 7.14 கி/செமீ3 |
| உருகுநிலை | 300 °C (572 °F; 573 K) ≥200 °செ-இல் இருந்து சிதைகிறது |
| 0.013 கி/லி (20 °செ) 0.025 கி/லி (25 °செ)[2] 0.053 கி/லி (80 °செ)[3] | |
கரைதிறன் பெருக்கம் (Ksp) of AgOH |
1.52·10−8 (20 °செ) |
| கரைதிறன் | காடி, ஆல்கலி (காரம்) ஆகியவற்றில் கரையக்கூடியது மதுசாரத்தில்கரைவதில்லை[2] |
| −134.0·10−6 செமீ3/மோல் | |
| கட்டமைப்பு | |
| படிக அமைப்பு | கன சதுரம் |
| புறவெளித் தொகுதி | Pn3m, 224 |
| வெப்பவேதியியல் | |
| Std enthalpy of formation ΔfH |
−31 கியூல்/மோல்[4] |
| நியம மோலார் எந்திரோப்பி S |
122 யூல்/மோல்·கெல்வின்[4] |
| வெப்பக் கொண்மை, C | 65.9 யூல்/மோல்·கெல்வின்[2] |
| தீங்குகள் | |
| GHS pictograms |   [5] [5] |
| GHS signal word | Danger |
| H272, H315, H319, H335[5] | |
| P220, P261, P305+351+338[5] | |
| Lethal dose or concentration (LD, LC): | |
LD50 (Median dose) |
2.82 கி/கிகி (எலிகள், வாய்வழி)[1] |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |

வெள்ளி(I) ஆக்சைடு வெள்ளி நைட்ரேட்டின் நீர்க்கரைசலுடன் கார ஐதராக்சைடின் நீர்க்கரைசலை வினைப்படுத்துவதன் மூலம் தயாரிக்கப்படுகிறது. இந்த வினைக்கு விரும்பத்தகுந்த ஆற்றலியல் உதவுவதால் அதிக அளவிலான வெள்ளி ஐதராக்சைடு தேவைப்படுவதில்லை:
அமெரிக்க காப்புரிமை எண் 20050050990 நுண்மையாக துாளாக்கப்பட்ட கடத்தும் தன்மையுள்ள நிரப்பும் பசையை தயாரிக்க உதவும் வெள்ளி ஆக்சைடின் தயாரிப்பு முறையை விவரிக்கிறது.
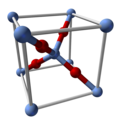
வெள்ளி ஆக்சைடு (Ag2O) நேர்கோட்டு வடிவத்தையும் இரு-அச்சு வடிவத்தில் கொண்டு நான்முகி ஆக்சைடுகளால் இணைக்கப்பட்ட வெள்ளியை மையத்தில் கொண்டுள்ளது. இது தாமிர ஆக்சைடுடன் ஒத்த வடிவத்தைக் கொண்டுள்ளது. இச்சேர்மத்தை சிதைக்கும் கரைப்பான்களில் கரைகிறது. இது Ag(OH)2− ஐ உருவாக்குவதாலும் ஒத்த நீராற்பகுப்பு விளைபொருட்களை உருவாக்குவதாலும் நீரில் சிறிதளவு கரையும் தன்மையுடையது. [சான்று தேவை] இது அமோனியாவில் கரைந்து கரையக்கூடிய வழிப்பொருட்களைத் தருகிறது. [சான்று தேவை] Ag2O இன் களியானது அமிலத்தால் எளிதில் தாக்கப்படுகிறது.:
HX = HF, HCl, HBr, அல்லது HI, HO2CCF3. இது கார குளோரைடுகளுடன் வினைப்பட்டு தொடர்புடைய கார ஐதராக்சைடைக் கரைசலில் விட்டுவிட்டு வெள்ளி குளோரைடு வீழ்படிவைத் தருகிறது.[6][7]
மற்ற வெள்ளி சேர்மங்களைப் போல, வெள்ளி ஆக்சைடானது ஒளிஉணர் தன்மையுடையது. இது 280 °செ வெப்பநிலைக்கு மேல் வெப்பப்படுத்தப்படும் போது சிதைவடைகிறது.[8]
இந்த ஆக்சைடானது வெள்ளி-ஆக்சைடு மின்கலங்களில் வெள்ளி (I,III) ஆக்சைடாக, Ag4O4 பயன்படுத்தப்படுகிறது. கரிம வேதியியலில், வெள்ளி ஆக்சைடானது ஒரு மிதமான ஆக்சிசனேற்றியாக பயன்படுத்தப்படுகிறது. உதாரணமாக, இது ஆல்டிகைடுகளை கார்பாக்சிலிக் அமிலங்களாக ஆக்சிசனேற்றம் செய்கிறது. இந்த வினைகளில் தேவைப்படும் நேரங்களில் வெள்ளி நைட்ரேட்டையும் கார ஐதராக்சைடுகளையும் உடனுக்குடன் வினைபுரியச்செய்து கிடைக்கும் வெள்ளி ஆக்சைடு சிறப்பான முடிவுகளைத் தருகிறது.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.