From Wikipedia, the free encyclopedia
டிரிட்டியம் (Tritium) (/ˈtrɪtiəm//ˈtrɪtiəm/ or /ˈtrɪʃiəm//ˈtrɪʃiəm/; குறியீடு
T
அல்லது 3
H
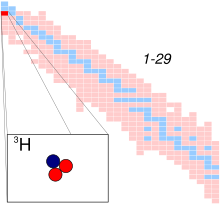
, ஐதரசன்-3 எனவும் அழைக்கப்படுகிறது) ஐதரசனின் கதிரியக்க ஓரிடத்தான் ஆகும். டிரிட்டியத்தின் அணுக்கரு (சில நேரங்களில் டிரிட்டான் எனவும் அழைக்கப்படுகிறது.) ஒரு நேர்மின்னியையும், மற்றும் இரண்டு நொதுமிகளையும் கொண்டுள்ளது, ஐதரசனின் அதிகமாகக் கிடைக்கும் ஓரிடத்தான் புரோட்டியம் ஆகும், இது ஒரு நேர்மின்னியையும், நொதுமியற்றதுமாய் இருக்கிறது. பூமியில் இயற்கையாய் கிடைக்கும் டிரிட்டியம் அரிதாகவே காணப்படுகிறது. அண்டக்கதிர்களால் ஏற்படும் மிக அரிதான அளவிலான வளிமண்டல வாயுக்கள் வினைபுரிவதால் மிகக்குறைந்த அளவிலான டிரிட்டியம் உருவாக்கப்படுகிறது. டிரிட்டியத்தை, அணுக்கரு உலைகளில் இலித்தியம் உலோகம் அல்லது இலித்தியம் தாங்கி சுட்டாங்கல் போன்றவற்றை ஒளிர்விப்பதன் மூலம் உருவாக்க முடியும். டிரிடியம் ஒரு கதிரியக்க உளவுபொருளாகவும், டியூட்ரியத்துடன் இணைந்து கடிகாரங்கள் மற்றும் வாசிப்பிற்கான கருவிகளில் கிளர்மின் ஒளிர்பொருளாகவும், மற்றும் அணுக்கரு இணைவு வினைகளில் எரிபொருளாகவும் ஆற்றல் உற்பத்தி நடைபெறும் இடங்கள் மற்றும் ஆயுதங்களில் எரிபொருளாகவும் பயன்படுகிறது.
 | |
| பொது | |
|---|---|
| குறியீடு | 3H |
| பெயர்கள் | டிரிட்டியம், H-3, டிரிட்டியம் |
| நேர்மின்னிகள் (Z) | 1 |
| நொதுமிகள் (N) | 2 |
| நியூக்லைடு தரவு | |
| இயற்கையில் கிடைக்குமளவு | மிகச்சிறிதளவு |
| அரைவாழ்வுக் காலம் (t1/2) | 12.32 ஆண்டுகள் |
| ஓரிடத்தான் நிறை | 3.0160492 Da |
| சுழற்சி | 1⁄2 |
| மேலதிக ஆற்றல் | 14,949.794 keV |
| பிணை ஆற்றல் | 8,481.821 keV |
| சிதைவு விளைபொருள்கள் | 3He |
| Decay modes | |
| சிதைவு முறை | சிதைவு ஆற்றல் (MeV) |
| Beta emission | 0.018590 |
| Isotopes of நீரியம் நியூக்லைடுகளின் முழுமையான அட்டவணை | |
தேசிய தொழில்நுட்பத் தரத்திற்கான நிறுவனத்தால் வெவ்வேறு சோதனைகள் மூலம் கண்டறியப்பட்ட டிரிட்டியத்திற்கான அரைவாழ்வுக் காலமானது பின்வருமாறு 4,500 ± 8 days (12.32 ± 0.02 years).[1] பீட்டா சிதைவின் மூலமாக பின்வரும் கதிரியக்கச் சமன்பாட்டின்படி இது ஹீலியம்-3 யாக மாறுகிறது. :
| 3 1T | → | 3 2He1+ | + | e− | + | ν e |
இந்த வினையானது 18.6 கிலோ எலத்திரன் வோல்ட் அளவிலான ஆற்றலை வெளியிடுகிறது.
டிரிட்டியமானது இலித்தியம்-6 ஓரிடத்தானை நொதுமி செயலாக்கத்தின் மூலம் அணுக்கரு உலை தொழில்நுட்பத்தைப் பயன்படுத்தி தயாரிக்கலாம். இச்செயல்முறை எந்த ஒரு ஆற்றலைக் கொண்டுள்ள நொதுமியாலும் சாத்தியமாகும். மேலும், இது ஒரு வெப்பம் உமிழ் செயல்முறையாகும். இவ்வினையானது 4.8 எம்.இ.வி அளவு ஆற்றலை வெளியிடுகிறது. ஒப்பீட்டளவில், D-T பிணைவானது 17.6 எம்.இ.வி அளவு ஆற்றலை வெளியிடுகிறது.
| 6 3Li | + | n | → | 4 2He | ( | 2.05 MeV | ) | + | 3 1T ( | 2.75 MeV | ) |
உயர்-ஆற்றல் நொதுமிகள் இலித்தியம்-7 ஓரிடத்தான்களிலிருந்தும் டிரிட்டியத்தைத் தயாரிக்க உதவ முடிம். இந்த வினையானது ஒரு வெப்பம் கொள் வினையாகும். இவ்வினை 2.466 மில்லியன் எலத்திரன் வோல்ட் ஆற்றலை உட்கொள்கிறது. இந்தச் செயல்முறை 1954 ஆம் ஆண்டில் கேஸ்ட்ல் பிரேவோ அணுக்கரு சோதனை நிகழ்த்தப்பட்ட போது எதிர்பாராதவிதமாக கிடைத்த அதிக விளைபொருள் உற்பத்தியிலிருந்து கண்டுபிடிக்கப்பட்டது.[2]
உயர்-ஆற்றல் நொதுமிகள் போரான்-10 ஓரிடத்தானை ஒளிர்வுறச் செய்வதன் மூலமாக எப்போதாவது டிரிட்டியத்தை உருவாக்குகின்றன.[3]
| 10 5B | + | n | → | 2 4 2He | + | 3 1T |
போரான் -10 ஓரிடத்தானின் நொதுமி பிடிப்பு தரும் பொதுவான விளைவானது 7
Li மற்றும் ஒரு ஒற்றை ஆல்பா துகள் உருவாக்கப்படுவதாகும்.[4]
டிரிட்டியம் கனநீரால் கட்டுப்படுத்தப்படும் அணுக்கரு உலைகளில் ஒரு டியூட்ரியமானது நொதுமியை சேர்த்துக் கொள்ளும் போதும் கூட தயாரிக்கப்படுகிறது. இந்த வினையானது மிகக்குறைவான குறுக்குவெட்டுப்பரப்பினால் உட்கவரும் தன்மையைப் பயன்படுத்தி கனநீரை ஒரு நல்ல நொதுமி மட்டுப்படுத்தியாக செயல்படச் செய்கிறது. ஒப்பீட்டளவில் மிகக்குறைவான டிரிட்டியமே உருவாகிறது. இருந்த போதும், பல ஆண்டுகளுக்கு ஒரு முறையாவது டிரிட்டியத்தை மட்டுப்படுத்தியிலிருந்து சுத்தம் செய்து அகற்றுவது சுற்றுப்புறத்தில் அது தப்பிச்செல்லும் அபாயத்தை தவிர்க்கும் நோக்கில் விரும்பத்தக்கதாகும்.[5]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.