
இருகுளோரின் ஏழாக்சைடு
From Wikipedia, the free encyclopedia
இருகுளோரின் ஏழாக்சைடு (dichlorine heptoxide, டைகுளோரின் எப்டாக்சைடு) என்பது Cl2O7 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும். இது பெர்குளோரிக் அமிலத்தின் நீரிலியாகும். பாசுபரசு ஐந்தாக்சைடு முன்னிலையில் பெர்குளோரிக் அமிலத்தை கவனமாகக் காய்ச்சி வடித்து இருகுளோரின் ஏழாக்சைடைத் தயாரிக்கலாம்.:[1]
- 2 HClO4 + P4O10 → Cl2O7 + H2P4O11
விரைவான உண்மைகள் பெயர்கள், இனங்காட்டிகள் ...
 | |
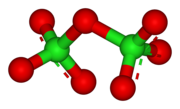 | |
| பெயர்கள் | |
|---|---|
| ஐயூபிஏசி பெயர்
டைகுளோரின் எப்டாக்சைடு | |
| வேறு பெயர்கள்
குளோரின்(VII) ஆக்சைடு; பெர்குளோரிக் நீரிலி; (பெர்குளோரைலாக்சி)குளோரேன் மூவாக்சைடு | |
| இனங்காட்டிகள் | |
| 10294-48-1 | |
| ChEBI | CHEBI:52356 |
| ChemSpider | 109884 |
| யேமல் -3D படிமங்கள் | Image |
| பப்கெம் | 123272 |
| |
| பண்புகள் | |
| Cl2O7 | |
| வாய்ப்பாட்டு எடை | 182.901 கி/மோல் |
| தோற்றம் | நிறமற்ற எண்ணெய் |
| அடர்த்தி | 1900 kg m−3 |
| உருகுநிலை | −91.57 °C (−132.83 °F; 181.58 K) |
| கொதிநிலை | 82 °C (180 °F; 355 K) |
| தீங்குகள் | |
| முதன்மையான தீநிகழ்தகவுகள் | ஆக்சிசனேற்றி, தொடுகையில் வெடிக்கும் [1] |
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |
மூடு
இறுதி விளை பொருள் கலவையில் இருந்து இச்சேர்மத்தை வடித்துப் பிரிக்கலாம்.
குளோரின் மற்றும் ஓசோன்[2] கலந்த கலவையை ஒளியூட்டுவதாலும் இருகுளோரின் ஏழாக்சைடு தயாரிக்க முடியும். பின்னர் இது மெல்ல நீராற்பகுப்பு அடைந்து பெர்குளோரிக் அமிலமாக மீள்கிறது. நீரிலியாக இருக்கும் போது பெர்குளோரிக் அமிலமும் ஒரு நச்சாகவே இருக்கிறது.