Loading AI tools
Från Wikipedia, den fria encyklopedin
Oxoniumjonen, H3O+, ibland även kallad hydroniumjonen eller hydroxoniumjonen (se under Om synonymer) är en positivt laddad jon av vatten (H2O).[1] Oxoniumjoner bildas dels genom vattnets autoprotolys där 2 vattenmolekyler omvandlas till en oxoniumjon och en hydroxidjon
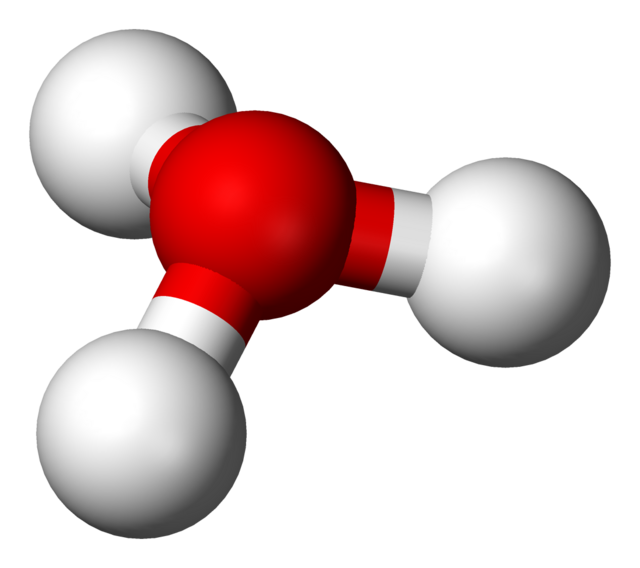
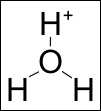
eller när en syra protolyseras i vatten där HAc är den oprotolyserade syran och Ac- syrans anjon.
En vattenlösning med höga halter oxoniumjoner ger en sur lösning. I vattenlösningar råder ett jämviktsförhållande mellan oxoniumjoner och hydroxidjoner, OH−. Vid hög oxoniumjonkoncentration är koncentrationen av hydroxidjoner låg, och tvärtom. Koncentrationerna av de båda jonslagen är även beroende av lösningens temperatur.
I många sammanhang anges oxoniumjonkoncentrationen som pH-värde. Ett lågt pH-värde innebär (vid normalt tryck och temperatur) en hög koncentration av oxoniumjoner, och tvärtom. En lösning med pH = 7 är neutral och håller samma koncentration av oxoniumjoner som av hydroxidjoner (vid 25 °C).
En snabb ändring av balansen mellan oxoniumjonen och hydroxidjonen i en lösning kan ge upphov till stora pH-förändringar. I naturen och i levande organismer skyddar ofta s.k. buffertsystem mot stora och plötsliga förändringar av oxoniumjon-/hydroxidjonkoncentrationerna.
Vid kemiska jämviktsberäkningar gör man vanligen ingen åtskillnad mellan vätejoner och oxoniumjoner, utan man betraktar samtliga som vätejoner, H+ (detta kan man göra beroende på att aktiviteten för vatten sätts till 1).
Det råder viss begreppsförvirring om den mest korrekta termen för H3O+. Organisationen IUPAC (International Union of Pure and Applied Chemistry) har fastslagit termen för oxoniumjon som H3O+. Oxoniumjon är även det begrepp som används i all kemiundervisning i skolan idag.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.