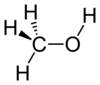
Метанол или метил алкохол (), је први члан хомологог низа засићених монохидроксилних алкохола. Метанол је стекао назив дрвени алкохол јер се некад углавном производио путем деструктивне дестилације дрвета. У данашње време, метанол се углавном индустријски производи путем хидрогенације угљен моноксида.[20] Веома је отрован. Уколико се у мањим количинама унесе у организам доводи до слепила, а у већим до смрти.
| |||
| |||
| Називи | |||
|---|---|---|---|
| Преферисани IUPAC назив
Methanol[1] | |||
| Други називи
Карбинол Колумбијски шпиритус хидроксиметан метил алкохол метил хидрат метил хидроксид метилни алкохол метилол пиролигниски шпиритус дрвени алкохол дрвени шпиритус | |||
| Идентификација | |||
3Д модел () |
|||
| B01170 | |||
| Бајлштајн | 1098229 | ||
| 100.000.599 | |||
| број | 200-659-6 | ||
| Гмелин Референца | 449 | ||
| KEGG[2] | |||
| MeSH | Methanol | ||
| PC1400000 | |||
| UNII | |||
| UN број | 1230 | ||
| Својства | |||
| CH 3OH or CH 4O | |||
| Моларна маса | |||
| Агрегатно стање | Безбојна течност | ||
| Густина | |||
| Тачка топљења | −97,6 °C (−143,7 °F; 175,6 K) | ||
| Тачка кључања | 64,7 °C (148,5 °F; 337,8 K) | ||
| меша се | |||
| −0,69 | |||
| Напон паре | 13,02 (на 20 °C) | ||
| Киселост (pKa) | 15,5[6] | ||
| Конјугована киселина | Метилоксонијум[7] | ||
| Конјугована база | метанолат[8] | ||
| Магнетна сусцептибилност | −21,40·10−6 | ||
| Индекс рефракције () | 1,33141[9] | ||
| Вискозност | 0,545 (на 25 °C)[10] | ||
| Диполни момент | 1,69 | ||
| Опасности[11][12] | |||
| Главне опасности | Умерено токсичан за мале животиње – високо токсичан за велике животиње и људе — може да буде фаталан/леталан или да узрокује слепило и да оштети јетру, бубреге, и срце ако се прогута – Токсични ефекти услед понављајућег прекомерног излатгања имају акумулативни ефекат на ЦНС, а посебно на оптички нерв – Симптоми могу да буду одложени, и да постану озбиљни након 12 до 18 сати, и да се задрже токон неколико дана након излагања[13] | ||
| Безбедност приликом руковања | |||
| ГХС пиктограми |    [14] [14] | ||
| ГХС сигналне речи | Опасност[14] | ||
| H225, H301, H311, H331, H370[14] | |||
| P210, P233, P240, P241, P242, P243, P260, P264, P270, P271, P280, P301+330+331, P310, P302+352[14] | |||
| NFPA 704 | |||
| Тачка паљења | 11 °C (52 °F; 284 K) | ||
| 470 °C (878 °F; 743 K)[16] 385 °C (725 °F; 658 K)[17] | |||
| Експлозивни лимити | 6–36%[18] | ||
| Смртоносна доза или концентрација (): | |||
50 (средња доза) |
5628 (пацов, орално) 7300 (миш, орално) 12880 (пацов, орално) 14200 (зец, орално)[19] | ||
| 64.000 (пацов, 4 )[19] | |||
| 33.082 (мачка, 6 ) 37.594 (миш, 2 )[19] | |||
| Границе изложености здравља у САД (): | |||
| [18] | |||
| [кожа][18] | |||
| 6000 [18] | |||
| Сродна једињења | |||
Сродна |
етанол бутанол | ||
Сродна једињења |
метил-хлорид метоксиметан | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |||
| Референце инфокутије | |||
То је најпростији алкохол, који се састоји од метил групе везане за хидроксилну групу. То је лака, испарљива, безбојна, запаљива течност са особеним задахом сличним етанолу (алкохолу за пиће).[21] Метанол је међутим далеко токсичнији од етанола. На собној температури, он је поларна течност. Са више од 20 милиона тона произведених годишње, он се користи као прекурсорза друге робне хемикалије, укључујући формалдехид, сирћетну киселину, метил терт-бутил етар, као и за низ других специјализованих хемикалија.[20]
Капацитети великих фабрика за производњу метанола се крећу од 200.000 до 310.000 тона годишње. Светска производња метанола је 2015. године износила 70 милиона тона са тенденцијом раста и тадашњим проценама да ће 2020. године износити око 100 милиона тона.
У Србији се метанол производи у Кикинди, фабрика МСК Кикинда (Метанолско-сирћетни комплекс Кикинда).
Мале количине метанола су присутне у нормалним, здравим људима. Једна студија је утврдила присуство од у просеку 4,5 ppm у издахнутом ваздуху испитаника.[22] Средња количина ендогеног метанола код људи од 0,45 /дан може да буде метаболисана из пектина присутног у воћу; један килограм јабука производи до 1,4 метанола.[23]
Метанол се природно производи при анаеробном метаболизму многих сојева бактерија и често је присутан у малим количинама у животној средини. Услед тога, атмосфера садржи мале количине метанолске паре. Атмосферски метанол бива оксидован у ваздуху под дејством сунчеве светлости до угљен-диоксида и воде током дана.
Међузвездана средина
Метанол је присутан у великим количинама у регионима у којима се формирају звезде и користи се у астрономији као маркер таквих региона. Он се детектује помоћу његових спектралних емисионих линија.[24]
Астрономи су 2006. године, користећи низ радио телескопа при Џодрел Банк опсерваторији, открили велики облак метанола у свемиру, широк 463 милиона .[25][26] Године 2016, астрономи су детектовали метил алкохол у диску формирања планета око младе звезде користећи радио телескоп.[27]
Удисањем ваздуха у коме има 3.000 метанола током 8 сати неколико дана доводи до тешког тровања.[28] Смртна доза ингестијом износи 30 до 100 .[28] Метанол се у организму споро оксидује до и те се због тога акумулира. Његови токсични метаболити су формалдехид, млечна и мравља киселина и ацетон чије дејство доводи до појаве специфичне симптоматологије тровања. Акутно тровање има три стадијума: пијанство, латенација (акумулација токсичних метаболита током 12-24 сата) и манифестовање тровања. Овај трећи стадијум карактеришу: запаљење слузокоже дисајних путева, поремећај вида, сметње од стране дигестивног тракта и грчеви мишића. Четвртог дана јављају се цијаноза, периферни колапс, конвулзије, кома, парализа центра за дисање са леталним (смртним) исходом у тежим случајевима.[28] Очна симптоматологија се састоји из: фотофобије, диплопије (дупло виђење), мидријазе, едема папиле и пролазно или трајног слепила.[28]
Метанол има ниску акутну токсичност код људи, али је опасан јер се заједно са етанолом повремено уноси у великим количинама. Мала количкина, као што је 10 mL (0,34 US fl oz) чистог метанола може да узрокује перманентно слепило путем деструкције видног живца. 30 mL (1,0 US fl oz) је потенцијално фатално.[29] Медијана леталне дозе је 100 mL (3,4 US fl oz) (i.e. 1–2 телесне тежине чистог метанола[30]). Референтна доза за метанол је 2 на дан.[31][32] Токсични ефекти почињу неколико сати након узимања, а антидоти често могу да спрече трајно оштећење.[29] Због његове сличности по изгледу и по мирису са етанолом (алкохолом у пићима), тешко је разликовати та два алкохола (као што је исто тако случај са денатурализованим алкохолом, фалсификованим пићима или алкохолним пићима врло ниског квалитета). Међутим, постоје случајеви отпорности на метанол, као што је случај Мајка Малоја који је био жртва неуспелог покушаја убиства метанолом почетком 1930-их.[33]
| Особина | Вредност |
|---|---|
| Број акцептора водоника | 1 |
| Број донора водоника | 1 |
| Број ротационих веза | 0 |
| Партициони коефицијент[34] ( | -0,4 |
| Растворљивост[35] ()) | 0,7 |
| Поларна површина[36] (, Å2) | 20,2 |
У индустрији, метанол се добија из синтетичког гаса, који је претходно добијен из метана. Наиме, метан је лако доступно једињење, будући да чини 70-90% природног гаса. Метан је непогодан за конверзију јер је релативно нереактивно једињење и подлеже реакцијама реформинга, као и хлоровања на високом притиску и температури. Најзначајнији поступак за конверзију метана у друга једињења је преко синтетичког гаса.
Синтетички гас
Синтетички или водени гас представља смешу угљен-моноксида и водоника. Синтетички гас се добија реформингом паре, односно реакцијом метана и водене паре на температури од 900 °C у присуству никла као катализатора. Реакција се изводи у тубуларним реакторима, који су паковани са керамиком преко које је нанет катализатор. Реактор се загрева сагоревањем течног горива или самог гаса. Поред синтетичког гаса као сировина у реакцији реформинга се могу користити и лаке фракције нафте добијене дестилацијом.
У зависности од услова, одвијају се следеће хемијске реакције:
Прва и трећа реакција су, за разлику од друге, ендотермне и потребно је довести енергију да би дошло до реакције. Степен конверзије метана расте са повећањем температуре, повећањем парцијалног притиска водене паре и смањењем укупног притиска.
Метанол
Метанол се добија конверзијом синтетичког гаса, егзотермном реакцијом:
Уколико се синтеза одвија помоћу синтетичког гаса добијеног из метана, онда се неповољан однос између водоника и угљен-моноксида (3:1) може компензовати додатком угљен-диоксида који реагује са водоником:
Равнотежа ових реакција се помера ка метанолу на нижим температурама и повишеном притиску. Као катализатор се раније користила смеша ZnO и Cr2O3 и притом се реакција изводи на температури од 350 °C и притиску од 340 bar. Време задржавања у реактору је врло краатко како би се спречило настајање споредних производа. Степен конверзије при једном проласку кроз катализатор је од 12 до 15%. Нови унапређен поступак производње користи активнији катализатор на бази бакра (CuO-ZnO-Cr2O3 или CuO-ZnO-Al2O3). Овакви катализатори омогућавају извођење реакције на нижим температурама од око 240 °C и нижим притисцима од 50 до 150 bar. Тако настаје метанол високе чистоће од 99,99 %.
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.