Anioni, ki šibko interagirajo s kationi se imenujejo šibko koordinirajoči anioni ali nekoordinirajoči anioni. Pogosto se uporabljajo kot protiioni pozitivno nabitim kovinskim kompleksom, saj se klasični anioni (npr. nitratni NO3-) v odsotnosti močnejših ligandov lahko koordinirajo na kovinski ion. Nekoordinirajoči anioni so med drugim pomembna komponenta superkislin.
This članek potrebuje čiščenje. Pri urejanju upoštevaj pravila slogovnega priročnika. |
Glavna strukturna značilnost nekoordinirajočih anionov je simetrična razporeditev naboja na večje število elektronegativnih atomov. V sintezni koordinacijski kemiji se je sprva uporabljal perkloratni anion ClO4-, vendar se ne uporablja več zaradi potencialne eksplozivnosti produktov. V moderni sintezni koordinacijski kemiji se največ uporabljajo trifluorometansulfonatni (triflatni) CF3SO3- (OTf), tetrafluoridoboratni BF4-, heksafluoridofosfatni PF6- in tetrafenilboratni BPh4- anioni.
- Kloratni ClO3- ion
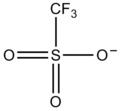
- Trifluorometansulfonatni (triflatni) CF3SO3- ion
- Tetrafluoridoboratni BF4- ion
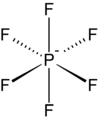
- Heksafluoridofosfatni PF6- ion

Z napredkom v organski kemiji je nastala potreba po še slabše koordinirajočih anionih, saj so raziskave organokovinskih kompleksov napredovale tako daleč, da za nadaljevanje raziskav obstoječe spojine niso več zadostovale. Pri določenih pogojih se je fluoridni ion odcepil od centralnega atoma aniona ali pa deloval kot mostovni ligand in s tem motil preiskovano spojino. Zato so razvili t. i. [BArF4]- komplekse. Ti so sestavljeni iz borovega atoma na katerega so vezani štirje fenilni obroči, substituirani z večjim številom fluoriranih funkcionalnih skupin. Podobne spojine poznamo tudi z aluminijem. Z uvedbo teh velikih anionskih kompleksov so se odprla vrata za raziskave visoko elektrofilnih kationov.[1]
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.