HOMO a LUMO sú druhy molekulových orbitálov. HOMO je skratka pre highest occupied molecular orbital, teda najvyšší obsadený molekulový orbitál, a LUMO je skratka pre lowest unoccupied molecular orbital, teda najnižší neobsadený molekulový orbitál.[1]

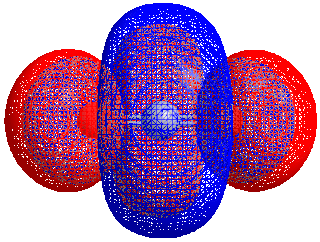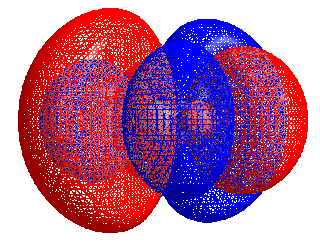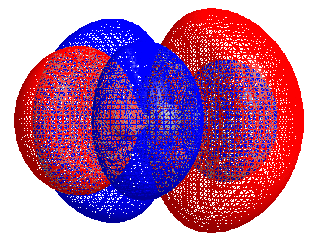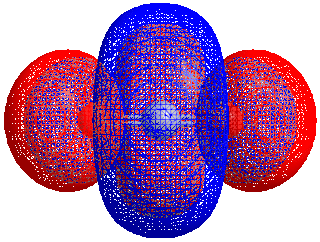

HOMO–LUMO medzera
Energetický rozdiel medzi HOMO a LUMO sa nazýva HOMO–LUMO medzera. Tieto orbitály sa niekedy nazývajú i hraničné orbitály, napríklad v teórii hraničných molekulárnych orbitálov. Energetický rozdiel medzi týmito orbitálmi sa dá použiť na predpoveď sily a stability komplexov prechodných kovov ako i na určenie farieb, ktoré tieto komplexy majú v roztoku.[2]
Polovodiče
HOMO je pre organické polovodiče približne tým, čím je valenčný pás pre anorganické polovodiče a kvantové body. Rovnaká analógia platí pre LUMO a vodivostný pás.[3]
Organokovová chémia
V chémii organokovov je možné použiť rozmer lalokov LUMO na určenie miesta, kde sa budú viazať pí ligandy.[4]
SOMO
SOMO je skratka pre singly occupied molecular orbital, teda molekulový orbitál s jedným elektrónom, napríklad HOMO orbitál radikálu.[5]
Najbližšie orbitály - NHOMO a SLUMO
Ak existujú, tak molekulové orbitály hneď pod HOMO a hneď nad LUMO takisto hrajú úlohu v teórii hraničných orbitálov. Tieto orbitály sa označujú ako NHOMO, teda next-to-highest occupied molecular orbital - druhý najvyšší obsadený molekulový orbitál, a SLUMO, second lowest unoccupied molecular orbital - druhý najnišží neobsadený molekulový orbitál.[6] Tieto orbitály sa niekedy označujú i ako HOMO-1 a LUMO+1.[Pozn. 1]
Poznámky
- Napríklad v článku TSUNEDA, Takao; SINGH, Raman Kumar; CHATTARAJ, Pratim Kumar. Diagrams for comprehensive molecular orbital-based chemical reaction analyses: reactive orbital energy diagrams. Physical Chemistry Chemical Physics, 2018, roč. 20, čís. 20, s. 14211–14222. Dostupné online [cit. 2022-05-17]. ISSN 1463-9076. DOI: 10.1039/C8CP00461G. (po anglicky).
Referencie
Pozri aj
Zdroj
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.
