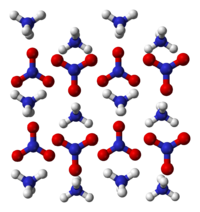
Amonijev nitrat
From Wikipedia, the free encyclopedia
Amonijev nitrat (NH4NO3, amonijeva salitra) amonijeva je sol dušične kiseline. Dolazi u obliku prozirnih kristala ili bijelog praha. Koristi se u poljoprivredi kao dušikom bogato umjetno gnojivo, kao oksidans u eksplozivima, te za postizanje niskih temperatura.
| Amonijev nitrat | |
|---|---|
 | |
 |
|
| IUPAC ime | |
| Identifikacija | |
| CAS registarski broj | 6484-52-2 |
| ChemSpider[1] | 21511 |
| UNII | T8YA51M7Y6 |
| RTECS registarski broj toksičnosti | BR9050000 |
| Jmol-3D slike | Slika 1 |
| Svojstva | |
| Molekulska formula | (NH4)(NO3) |
| Molarna masa | 80.052 |
| Agregatno stanje | bela čvrsta materija |
| Gustina | 1.725 |
| Tačka topljenja |
169.6 ° |
| Tačka ključanja |
aproks. 210 ° razlaže se |
| Rastvorljivost u vodi | 118 150 297 410 576 1024 [2] |
| Struktura | |
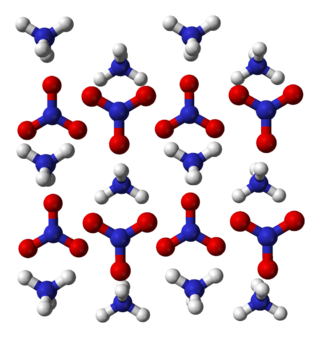
| Kristalna rešetka/struktura | trigonalna |
| Podaci o eksplozivu | |
| Osetljivost na šok | veoma niska |
| Osetljivost na trenje | veoma niska |
| Eksplozivna brzina | 5270 |
| Opasnost | |
| Podaci o bezbednosti prilikom rukovanja (MSDS) | |
| EU-indeks | nije na listi |
| Opasnost u toku rada | Eksploziv |
| NFPA 704 | |
| LD50 | 2085–5300 (oralno kod pacova, miševa)[3] |
| Srodna jedinjenja | |
| Drugi anjoni | Amonijum nitrit |
| Drugi katjoni | Natrijum nitrat Kalijum nitrat Hidroksilamonijum nitrat |
| Srodna jedinjenja | Amonijum perhlorat |
|
(šta je ovo?)
(verifikuj)
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |
| Infobox references | |
Kristalne faze
Kristalno uređenje amonijevog nitrata mijenja se u ovisnosti o tlaku i temperaturi. Određene su slijedeće kristalne faze:
| Sistem | Temperatura (°C) | Faza | Promjena volumena (%) |
|---|---|---|---|
| - | > 169.6 | tekuća | - |
| I | 169.6 do 125.2 | kubična | +2.1 |
| II | 125.2 do 84.2 | tetragonska | -1.3 |
| III | 84.2 do 32.3 | α-rombska | +3.6 |
| IV | 32.3 do −16.8 | β-rombska | −2.9 |
| V | −16.8 | tetragonska | - |
Dobivanje
Procesi od kojih se sastoji industrijska proizvodnja amonijevog nitrata, mada kemijski jednostavni, tehnološki su prilično izazovni. Kiselinsko-bazna reakcija amonijaka s dušičnom kiselinom daje otopinu amonijevog nitrata:[4]
- HNO3(aq) + NH3(g) → NH4NO3(aq)
U industrijskoj proizvodnji ovaj proces se izvodi miješanjem bezvodnog amonijaka i koncentrirane dušične kiseline. Reakcija je burna i vrlo egzotermna. Nakon što je nastala otopina, obično koncentracije od oko 83%, višak vode se otparava i dobiva se otopina amonijevog nitrata koncentracije 95% do 99,9%, ovisno o čistoći. Od dobivene otopine se u tornjevima za raspršivanje rade granule amonijevog nitrata koje su tipičan komercijalni oblik ove kemikalije.
Haberov proces koristi dušik i vodik za proizvodnju amonijaka, dio kojega se može oksidirati u dušičnu kiselinu te s preostalim amonijakom dati amonijev nitrat.
Amonijev nitrat se također može dobiti iz otopina amonijevih i nitratnih soli:
- (NH4)2SO4 + 2 NaNO3 → Na2SO4 + 2 NH4NO3
- Ca(NO3)2 + (NH4)2SO4 → 2 NH4NO3 + CaSO4
Natrijev sulfat se uklanja snižavanjem temperature smjese - budući da je slabije topljiv u vodi od amonijevog nitrata on se taloži i uklanja filtracijom. Kalcijev sulfat je prilično netopljiv, čak i na sobnoj temperaturi.
Reference
Vanjske veze
Wikiwand - on
Seamless Wikipedia browsing. On steroids.