Loading AI tools
химическое соединение Из Википедии, свободной энциклопедии
Окси́д вольфра́ма(VI) (другие используемые названия — триоксид вольфрама, трёхокись вольфрама, вольфрамовый ангидрид, ангидрид вольфрамовой кислоты́) — бинарное химическое соединение кислорода и переходного металла вольфрама.
| Оксид вольфрама(VI) | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Окись вольфрама(VI) |
| Традиционные названия | триоксид вольфрама, трёхокись вольфрама, вольфрамовый ангидрид |
| Хим. формула | WO3 |
| Физические свойства | |
| Молярная масса | 231,8393 г/моль |
| Классификация | |
| Рег. номер CAS | 1314-35-8 |
| PubChem | 14811 |
| Рег. номер EINECS | 215-231-4 |
| SMILES | |
| InChI | |
| RTECS | YO7760000 |
| ChemSpider | 14127 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Обладает кислотными свойствами.
Мелкокристаллический порошок лимонно-жёлтого цвета. Плотность 7,2—7,4 г/см³. Температура плавления 1470 °C, температура кипения 1700 °С.
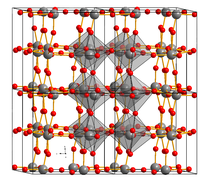
Кристаллическая структура соединения зависит от температуры. Устойчивая моноклинная до −27 °C, триклинная в диапазоне температур от −27 до 20 °C, моноклинная от 20 до 339 °C, ромбическая от 339 до 740 °C, тетрагональная при температуре от 740 до 1470 °C[1].
При температуре выше 800 °C заметно возгоняется, в газовой фазе существует в виде ди-, три- и тетрамеров[1].
В воде и минеральных кислотах (за исключением фтороводородной кислоты) практически не растворяется. До металла может быть восстановлен водородом при температуре 700—900 °C, углеродом при температуре 1000 °C[1] или другими металлами:
Триоксид вольфрама получают термическим разложением гидрата (вольфрамовой кислоты) или паравольфрамата аммония при температуре 500—800 °C[1].
Или из вольфрамата кальция (минерал шеелит) действием соляной кислоты с последующим разложением образующейся вольфрамовой кислоты:
Другой способ получения — окисление металлического вольфрама в атмосфере кислорода или на воздухе при температуре выше 500 °C[1]. Эта реакция происходит при включении потерявшей герметичность лампы накаливания, триоксид вольфрама при этом оседает на внутренних стенках колбы лампы в виде светло-жёлтого налёта:
Триоксид вольфрама применяется для получения карбидов и галогенидов вольфрама, металлического вольфрама.
Из-за насыщенного жёлтого цвета применяется в качестве жёлтого пигмента для придания цвета стеклу и керамике[2].
Для придания огнестойкости тканям[3].
Используется в датчиках газоанализаторов на озон[4].
Используется в производстве сцинтилляторов и люминофоров содержащих вольфраматы бария или стронция.
В последние время триоксид вольфрама нашёл применение в производстве электрохромного оконного стекла. Светопропускание застеклённых таким стеклом окон можно варьировать изменяя управляющее электрическое напряжение, прикладываемое к плёнке электрофотохромного материала[5][6].
Также применяется в качестве катализатора гидрогенизации при крекинга углеводородов[1].
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.