Лимфогранулематоз
злокачественное заболевание лимфоидной ткани Из Википедии, свободной энциклопедии
Лимфома Ходжкина (синонимы: лимфогранулемато́з[8][9], болезнь Ходжкина, злокачественная гранулёма) — злокачественное заболевание лимфоидной ткани, характерным признаком которого является наличие гигантских клеток Рид — Березовского — Штернберга, обнаруживаемых при микроскопическом исследовании поражённых лимфатических узлов.
| Болезнь Ходжкина | |
|---|---|
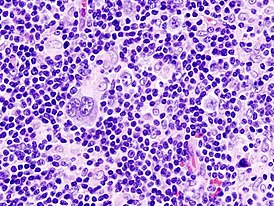 Микропрепарат: биоптат лимфоузла. Характерная клетка Рид — Березовского — Штернберга | |
| МКБ-11 | 2B30.1 |
| МКБ-10 | C81 |
| МКБ-10-КМ | C81.9 и C81 |
| МКБ-9 | 201 |
| МКБ-9-КМ | 201.0[1], 201.2[1], 201.1[1], 201[1] и 201.9[1] |
| МКБ-О | 9650/3, 9667/3 и 965-966 |
| OMIM | 236000, 300221 и 400021 |
| DiseasesDB | 5973 |
| MedlinePlus | 000580 |
| eMedicine | med/1022 |
| MeSH | D006689 |
| Медиафайлы на Викискладе | |
| Лимфогранулематоз | |
|---|---|
 | |
| Названо в честь | Томас Ходжкин |
| Медицинская специальность | гематология |
| Лекарство, используемое для лечения | доксорубицин, блеомицин, винбластин и дакарбазин |
| Генетическая связь | GATA3[вд][2], TCF3[вд][3], CLSTN2[вд][4], EOMES[вд][5], IL13[вд][6] и PVT1[вд][7] |
| МКБ-9-КМ | 201.0[1], 201.2[1], 201.1[1], 201[1] и 201.9[1] |
| Код ICPC 2 | B72 |
| Код NCI Thesaurus | C26956[1], C9357[1] и C6914[1] |
| Медиафайлы на Викискладе | |
История описания
В 1832 году Томас Ходжкин описал семерых больных, у которых наблюдалось увеличение лимфатических узлов и селезёнки, общее истощение и упадок сил. Во всех случаях болезнь имела летальный исход. Спустя 23 года С. Уилкс назвал это состояние болезнью Ходжкина, изучив описанные Ходжкином случаи и добавив к ним 11 собственных наблюдений.
Этиология и эпидемиология
Суммиров вкратце
Перспектива
Эта болезнь принадлежит к большой и достаточно разнородной группе заболеваний, относящихся к злокачественным лимфомам. Основная причина возникновения болезни не совсем ясна, но некоторые эпидемиологические данные, такие как совпадение по месту и времени, спорадические множественные случаи у некровных родственников, говорят об инфекционной природе болезни, а точнее вирусной (вирус Эпштейна — Барр, англ. Epstein-Barr virus, EBV). Ген вируса обнаруживается при специальных исследованиях в 20—60 % биопсий. Эту теорию подтверждает и некоторая связь болезни с инфекционным мононуклеозом. Другими способствующими факторами могут быть генетическая предрасположенность и, возможно, некоторые химические субстанции.
Это заболевание встречается только у человека и чаще поражает представителей европеоидной расы. Лимфогранулематоз может возникнуть в любом возрасте. Однако существует два пика заболеваемости: в возрасте 15—29 лет и старше 55 лет. Мужчины болеют лимфогранулематозом чаще, чем женщины с соотношением 1,4:1.
Частота возникновения заболевания — примерно 1/25 000 человек/год, что составляет около 1 % от показателя для всех злокачественных новообразований в мире и примерно 30 % всех злокачественных лимфом.
Патологическая анатомия
Суммиров вкратце
Перспектива

Обнаружение гигантских клеток Рид-Березовского-Штернберга и их одноядерных предшественников, клеток Ходжкина, в биоптате есть обязательный критерий диагноза лимфогранулематоза. По мнению многих авторов, только эти клетки являются опухолевыми. Все остальные клетки и фиброз есть отражение иммунной реакции организма на опухолевый рост. Главными клетками лимфогранулематозной ткани, как правило, будут мелкие, зрелые Т-лимфоциты фенотипа CD2, CD3, CD4 > CD8, CD5 с различным количеством В-лимфоцитов. В той или иной степени присутствуют гистиоциты, эозинофилы, нейтрофилы, плазматические клетки и фиброз. Соответственно различают четыре основных гистологических типа:
- Лимфогистиоцитарный вариант — примерно 15 % случаев лимфомы Ходжкина. Чаще болеют мужчины моложе 35 лет, обнаруживается в ранних стадиях и имеет хороший прогноз. Преобладают зрелые лимфоциты, клетки Рид-Березовского-Штернберга редки. Вариант низкой злокачественности.
- Вариант с нодулярным склерозом — наиболее частая форма, 40—50 % всех случаев. Встречается обычно у молодых женщин, располагается часто в лимфатических узлах средостения и имеет хороший прогноз. Характеризуется фиброзными тяжами, которые делят лимфоидную ткань на «узлы». Имеет две главные черты: клетки Рид-Березовского-Штернберга и лакунарные клетки. Лакунарные клетки большие по размеру, имеют множество ядер или одно многолопастное ядро, цитоплазма их широкая, светлая, пенистая.
- Смешанноклеточный вариант — примерно 30 % случаев лимфомы Ходжкина. Наиболее частый вариант в развивающихся странах, у детей, пожилых людей. Чаще болеют мужчины, клинически соответствует II—III стадии болезни с типичной общей симптоматикой и склонностью к генерализации процесса. Микроскопическая картина отличается большим полиморфизмом со множеством клеток Рид-Березовского-Штернберга, лимфоцитов, плазмоцитов, эозинофилов, фибробластов.
- Вариант с подавлением лимфоидной ткани — самый редкий, меньше 5 % случаев. Клинически соответствует IV стадии болезни. Чаще встречается у пожилых больных. Полное отсутствие лимфоцитов в биоптате, преобладают клетки Рид-Березовского-Штернберга в виде пластов или фиброзные тяжи или их сочетание.
Симптомы, клиническая картина
Суммиров вкратце
Перспектива
Заболевание обычно начинается с увеличения лимфатических узлов на фоне полного здоровья. В 70—75 % случаев это шейные или надключичные лимфатические узлы, в 15—20 % подмышечные и лимфатические узлы средостения и 10 % это паховые узлы, узлы брюшной полости и т. д. Увеличенные лимфатические узлы плотные, безболезненные, подвижные.
Вследствие того, что часто поражается лимфатическая ткань, расположенная в грудной клетке, первым симптомом заболевания может быть затруднение дыхания или кашель вследствие давления на лёгкие и бронхи увеличенных лимфатических узлов, но чаще всего поражение средостения обнаруживается при случайной обзорной рентгенографии грудной клетки.
Увеличенные лимфатические узлы могут спонтанно уменьшаться и снова увеличиваться, что может привести к затруднению в постановке диагноза.
У небольшой группы больных отмечаются общие симптомы: температура, ночная проливная потливость, потеря веса и аппетита. Обычно это люди старше 50 лет со смешанноклеточным гистологическим вариантом или вариантом с подавлением лимфоидной ткани. Известная лихорадка Пеля — Эбштайна (лихорадка 1—2 недели, сменяемая периодом апирексии), сейчас наблюдается значительно реже. Появление этих симптомов в ранних стадиях утяжеляет прогноз.
У некоторых больных наблюдаются генерализованный кожный зуд и боль в поражённых лимфатических узлах. Последнее особенно характерно после приёма алкогольных напитков.
Поражение органов и систем
- Увеличение лимфатических узлов средостения наблюдается в 45 % случаев I—II стадии. В большинстве случаев не сказывается на клинике и прогнозе, но может вызывать сдавливание соседних органов. О значительном увеличении можно говорить, когда ширина новообразования на рентгенограмме превышает 0,3 (МТИ > 3 Mass Thorac Index) по отношению к ширине грудной клетки.
- Селезёнка — спленомегалия, поражается в 35 % случаев и, как правило, при более поздних стадиях болезни.
- Печень — 5 % в начальных стадиях и 65 % в терминальной.
- Лёгкие — поражение лёгких отмечается в 10—15 % наблюдений, которое в некоторых случаях сопровождается выпотным плевритом.
- Костный мозг — редко в начальных и 25—45 % в IV стадии.
- Почки — чрезвычайно редкое наблюдение, может встречаться при поражении внутрибрюшных лимфатических узлов.
- Нервная система — главным механизмом поражения нервной системы является сдавление корешков спинного мозга в грудном или поясничном отделах уплотнёнными конгломератами увеличенных лимфатических узлов с появлением боли в спине, пояснице.
Инфекции
Из-за нарушения клеточного иммунитета при лимфоме Ходжкина часто развиваются инфекции: вирусные, грибковые, протозойные, которые ещё более утяжеляются химиотерапией и/или лучевой терапией. Среди вирусных инфекций первое место занимает вирус опоясывающего герпеса (Herpes zoster — вирус ветряной оспы). Среди грибковых заболеваний наиболее частыми являются кандидоз и криптококковый менингит. Токсоплазмоз и пневмония, вызванная пневмоцистой (Pneumocystis jiroveci), являются частыми протозойными инфекциями. При лейкопении на фоне химиотерапии могут развиться и банальные бактериальные инфекции.
Стадии заболевания лимфогранулематозом
Суммиров вкратце
Перспектива
В зависимости от степени распространённости заболевания выделяют четыре стадии лимфогранулематоза (энн-арборская классификация):
- 1 стадия — опухоль находится в лимфатических узлах одной области (I) или в одном органе за пределами лимфатических узлов.
- 2 стадия — поражение лимфатических узлов в двух и более областях по одну сторону диафрагмы (вверху, внизу) (II) или органа и лимфатических узлов по одну сторону диафрагмы (IIE).
- 3 стадия — поражение лимфатических узлов по обе стороны диафрагмы (III), сопровождающееся или нет поражением органа (IIIE), или поражение селезёнки (IIIS), или всё вместе.
- Стадия III(1) — опухолевый процесс локализован в верхней части брюшной полости.
- Стадия III(2) — поражение лимфатических узлов, расположенных в полости таза и вдоль аорты.
- 4 стадия — заболевание распространяется помимо лимфатических узлов на внутренние органы: печень, почки, кишечник, костный мозг и др. с их диффузным поражением
- Для уточнения расположения используют буквы E, S и X, значение их приведено ниже.
Расшифровка букв в названии стадии
Каждая стадия подразделяется на категорию А и В соответственно приведённому ниже.
- Буква А — отсутствие симптомов заболевания у пациента
- Буква В — наличие одного или более из следующего:
- Буква Е — опухоль распространяется на органы и ткани, расположенные рядом с поражёнными группами крупных лимфатических узлов.
- Буква S — поражение селезёнки.
- Буква X — объёмное образование большого размера.
Диагноз
Суммиров вкратце
Перспектива

Основным критерием для постановки диагноза служит обнаружение гигантских клеток Рид — Березовского — Штернберга и/или клеток Ходжкина в биоптате, извлечённом из лимфатических узлов. Используются и современные медицинские методы: (ультразвуковое исследование органов брюшной полости, компьютерная рентгеновская или магнитно-резонансная томография органов грудной клетки). При выявлении изменений в лимфатических узлах необходима гистологическая верификация диагноза.
- Обязательные методы
- Хирургическая биопсия
- Подробный анамнез с упором на выявление или нет симптомов группы В
- Полное физикальное обследование с оценкой лимфаденопатии
- Лабораторное исследование с полной гемограммой (гематокрит, эритроциты, СОЭ, лейкоциты-тип, глобулины, проба Кумбса, функциональные пробы печени и т. д.)
- Рентгенография грудной клетки в двух проекциях
- Миелограмма и биопсия костного мозга
- Исследования по показаниям
- Компьютерная томография, ПЭТ/КТ.
- Лапаротомия для определения стадии и спленэктомия
- Торакотомия и биопсия лимфатических узлов средостения
- Сцинтиграфия с галлием
Данные лабораторного исследования
Показатели периферической крови не специфичны для данного заболевания. Отмечаются:
- Повышение СОЭ
- Лимфоцитопения
- Анемия различной степени выраженности
- Аутоиммунная гемолитическая анемия с положительной пробой Кумбса (редко)
- Снижение Fe и TIBC
- Незначительный нейтрофилёз
- Тромбоцитопения
- Эозинофилия, особенно у больных с кожным зудом
Антигены
В диагностике лимфогранулематоза могут быть полезны два антигена.
- CD15, идентифицированный как моноклональное антитело Leu M1 и относящийся к Lewis X кровяному антигену; функционирует как адгезивный рецептор, обнаруживается при всех подтипах лимфогранулематоза, кроме лимфогистиоцитарного варианта.
- Антиген CD30 (Ki-1), который появляется во всех клетках Рид — Березовского — Штернберга.
Лечение
Суммиров вкратце
Перспектива
В настоящее время используются следующие методы лечения:
- Лучевая терапия
- Химиотерапия
- Их комбинация
- Химиотерапия высокими дозами препаратов с последующей пересадкой костного мозга
При I—II стадиях болезни Ходжкина, при отсутствии симптомов В лечение, как правило, включает только облучение в дозе 3600—4400 cGy (1000-cGy еженедельно), с помощью которого достигается до 85 % длительных ремиссий. Лучевая терапия проводится специальными аппаратами. Облучаются определённые группы лимфатических узлов. Действие облучения на другие органы нейтрализуется с помощью специальных защитных свинцовых фильтров.
Для химиотерапии в настоящее время используются различные схемы, в частности BEACOPP (блеомицин, этопозид, доксорубицин (адриамицин), циклофосфамид, винкристин (онковин), прокарбазин, преднизолон) и его вариации BEACOPP-esc (BEACOPP с эскалацией доз ряда компонентов по сравнению со стандартной схемой) и BEACOPP-14 (BEACOPP с сокращением междозового интервала до 14 дней). Используются также более старые схемы — протокол Stanford IV, Stanford V, схемы COPP, ABVD (доксорубицин, блеомицин, винбластин, дакарбазин) циклами по 28 дней в течение, как минимум, 6 месяцев. Недостатком схемы MOPP (мехлоретамин, винкристин (Oncovin), прокарбазин, преднизолон) является более частое развитие лейкоза в отдалённом будущем (через 5—10 лет) по сравнению со схемой COPP. Схема ChlVPP (хлорамбуцил, винбластин, прокарбазин, преднизолон).
Наиболее перспективным и эффективным методом лечения является комбинированная химио-лучевая терапия, которая позволяет получить длительные, 10—20-летние ремиссии более чем у 90 % больных, что равноценно полному излечению.
Как правило, большинство больных с болезнью Ходжкина начинают первый курс лечения в стационаре, а затем, при условии хорошей переносимости лекарств, продолжают получать лечение в амбулаторных условиях.
В 2011 году FDA дало согласие на ускоренное одобрение первого таргетного препарата «Адцетрис» (МНН — брентуксимаб ведотин) для лечения CD30-позитивных лимфом по двум показаниям: 1) лечение лимфомы Ходжкина после 2 линий химиотерапии и аутологичной трансплантации/без трансплантации для лиц, не являющихся кандидатами по медицинским показаниям; 2) лечение системной анапластической крупноклеточной лимфомы после как минимум одной линии химиотерапии.[10] Адцетрис является конъюгатом антитела и цитотоксического агента, который селективно воздействует на опухолевые клетки. В 2016 году препарат зарегистрирован в Российской Федерации и доступен для пациентов по решению врачебной комиссии. [11]
В 2017 году FDA впервые одобрил иммунологический препарат «Кейтруда» (пембролизумаб) для лечения рецидивов лимфомы Ходжкина.[12] Другие препараты: ниволумаб, тислелизумаб[англ.], синтилимаб[англ.], камрелизумаб[англ.].
Прогноз
Суммиров вкратце
Перспектива
В настоящее время терапия лимфомы Ходжкина, а это злокачественное заболевание, осуществляется достаточно успешно (в 70—84 % случаев удаётся достичь 5-летней ремиссии). По данным Национального института рака (США), пациенты, у которых полная ремиссия продолжается более 5 лет после окончания лечения, могут считаться окончательно излеченными. Количество рецидивов колеблется в пределах 30—35 %.
Наиболее часто используются по меньшей мере 3 системы клинических прогностических факторов, предложенных наиболее крупными кооперированными группами: EORTC (European Organization for the Research and Treatment of Cancer), GHSG (German Hodgkin’s lymphoma Study Group) и NCIC/ECOG (National Cancer Institute of Canada и Eastern Cooperative Oncology Group).
| Прогностическая группа | EORTC | GHSG | NCIC/ECOG |
|---|---|---|---|
| Благоприятная | благоприятная — favorable CS* I и II стадии без факторов риска | ранняя — early CS I и II стадии без факторов риска | низкого риска — low risk CS IA с поражением одного лимфатического узла, гистологический вариант только лимфоидное преобладание или нодулярный склероз, размеры лимфатического узла не более 3 см и локализация в верхней трети шеи, СОЭ менее 50 мм/ч, возраст менее 50 лет |
| Промежуточная | неблагоприятная — unfavorable CS I—II стадии с факторами риска A, B, C, D | промежуточная — intermediate CS I—II А стадии с факторами риска A, B, C, D и II В стадия с факторами риска B, C | не специфицирована CS I—II стадии, не входящие в группы низкого и высокого риска |
| Неблагоприятная | распространенная — advanced III и IV стадии | неблагоприятная — unfavorable CS IIB стадия с факторами риска A, D, а также III и IV стадии | высокого риска — high risk CS I и II стадии с массивным поражением средостения или периферических лимфатических узлов или интраабдоминальное поражение, а также III и IV стадии |
| Факторы риска | А. массивное поражение средостения — МТИ > 0,35 B. поражение лимфатических узлов > 4 областей (area) C. СОЭ > 50 при стадии А и СОЭ > 30 при стадии В D. возраст > 50лет | А. массивное поражение средостения — МТИ > 0,35 B. поражение лимфатических узлов > 3 областей C. СОЭ > 50 при стадии А и СОЭ > 30 при стадии В D. экстранодальное поражение (стадия Е) | А.возраст > 40 лет B. гистологический вариант смешанноклеточный или лимфоидное истощение C. СОЭ > 50 D.поражение лимфатических узлов > 4 областей (area) |
В статье есть список источников, но не хватает сносок. |
Примечания
Литература
Ссылки
Wikiwand - on
Seamless Wikipedia browsing. On steroids.
