Cloreto de alumínio
composto químico / De Wikipedia, a enciclopédia encyclopedia
O cloreto de alumínio, ou tricloreto de alumínio, de fórmula química AlCl3, é um sal, preparado pela adição de ácido clorídrico e alumínio metálico, que libera H2 gasoso.
Esta página ou se(c)ção precisa ser formatada para o padrão wiki. (Dezembro de 2009) |
Mais informação Cloreto de alumínio Alerta sobre risco à saúde, Identificadores ...
| Cloreto de alumínio Alerta sobre risco à saúde | |
|---|---|
 | |
 | |
| Nome IUPAC | Aluminium(III) chloride |
| Identificadores | |
| Número CAS | [7446-70-0] (anidro) [10124-27-3] (hexahidrato) |
| Propriedades | |
| Fórmula molecular | AlCl3 |
| Massa molar | 133.34 g mol−1 (anhydrous) 241.432 g mol−1 (hexahydrate) |
| Aparência | Pale yellow solid, hygroscopic. |
| Densidade | 2,44 g·cm−3[1] |
| Ponto de ebulição |
180 °C (Sublimation, 262 °C decompõe-se)[1] |
| Solubilidade em água | 43.9 g/100 ml (0°C) 44.9 g/100 ml (10°C) 45.8 g/100 ml (20°C) 46.6 g/100 ml (30°C) 47.3 g/100 ml (40°C) 48.1 g/100 ml (60°C) 48.6 g/100 ml (80°C) 49 g/100 ml (100°C) [carece de fontes?] 450 g·l−1 (decompõe-se [1]) |
| Pressão de vapor | 1 hPa[1] (20 °C) |
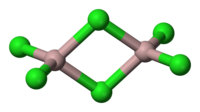
| Estrutura | |
| Estrutura cristalina | 6-coordinate layer lattice |
| Geometria de coordenação |
Octahedral (solid) Tetrahedral (liquid) |
| Forma molecular | Trigonal planar (monomeric vapour) |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
−704 kJ·mol−1[2] |
| Riscos associados | |
| Classificação UE | |
| NFPA 704 | |
| Frases R | R34 |
| Frases S | S1/2, S7/8, S28, S45 |
| LD50 | 3450 mg·kg−1[1] |
| Compostos relacionados | |
| Outros aniões/ânions | Fluoreto de alumínio Brometo de alumínio Iodeto de alumínio Sulfeto de alumínio |
| Outros catiões/cátions | Tricloreto de boro Cloreto de gálio (III) Cloreto de índio (III) Cloreto de tálio (III) Cloreto de magnésio Tetracloreto de silício |
| ácidos de Lewis relacionados | Cloreto de ferro (III) Trifluoreto de boro |
| Compostos relacionados | Tetracloroaluminato de lítio |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Fechar
Ele reage violentamente com água (formando-se cloreto de hidrogênio). É conhecido como sal anidro (sem água),ou como sal hexaidratado, perde água aos 100°C. O cloreto de alumínio pode ser obtido fazendo a passagem do cloro sobre óxido de alumínio aquecido e carbono. O cloreto de alumínio é usado comercialmente como um catalisador no craqueamento do petróleo, é também usado como catalisador em reações orgânicas.
Existe também um sal de cloreto de alumínio (I) (AlCl), mas é muito instável e apenas conhecido em seu estado gasoso.