
Електролитна ќелија
From Wikipedia, the free encyclopedia
Електролитна ќелија е електрохемиска ќелија која предизвикува неспонтана-редокс реакција преку примена на електрична енергија. Тие често се користат при распаѓањето на хемиските соединенија, во процес наречен електролиза - грчкиот збор лиза значи да се растури. Важни примери за електролиза се: разградувањето на водата во водород и кислород, боксит во алуминиум и други хемикалии. Галванизацијата (на пример од бакар, сребро, никел или хром) се изведува со помош на електролитските ќелии.
Оваа статија или заглавие има потреба од викифицирање за да ги исполни стандардите за квалитет на Википедија. Ве молиме помогнете во подобрувањето на оваа статија со соодветни внатрешни врски. |
Оваа статија можеби бара дополнително внимание за да ги исполни стандардите за квалитет на Википедија. Ве молиме подобрете ја оваа статија ако можете. |
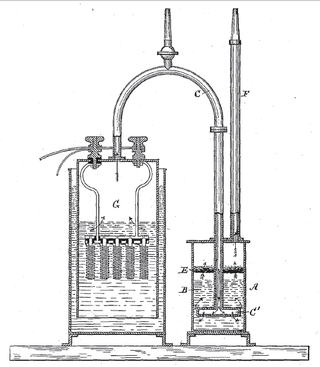
Електролитната ќелија има три компоненти: електролит и две електроди (катодна и анодна). Електролитот обично е раствор на вода или други растворувачи во кои се раствораат јони. Стопените соли, како што е натриум хлоридот, исто така се електролити. Кога се управувани од надворешен напон кој се применува на електродите јоните во електролитот се привлекуваат кон електрода со спротивен полнеж, каде што може да се случат реакциите кои се пренесуваат со полнење (кои исто така се наречени фарадаични или редоксни реакции). Само со надворешен електричен потенцијал (т.е. напон) со точен поларитет и доволна големина електролитната ќелија може да распадне нормално,стабилно или инертно како хемиско соединение во раствор. Обезбедена електрична енергија може да предизвика хемиска реакција која не би се случила спонтано на друг начин.