
Олово(II) јодид
хемиско соединение / From Wikipedia, the free encyclopedia
Олово(II) јодид (or олово јодид) iе хемиско соединение со формула PbI2. На собна температура, тоа е светло жолта кристална цврста материја без мирис, која станува портокалова и црвена кога ќе се загрее.[7] Порано се нарекуваше плумбосен јодид.
 | |
 | |
Други називи Плумбосен јодид | |
| Назнаки | |
|---|---|
| 10101-63-0 | |
| ChemSpider | 23305 |
| EC-број | 233-256-9 |
| 3Д-модел (Jmol) | Слика |
| PubChem | 24931 |
| |
| UNII | OTL90F2GLT |
| ОН-бр. | 2291 3077 |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | свело жолт прашок |
| Мирис | без мирис |
| Густина | 6.16 g/cm3 |
| Точка на топење | |
| Точка на вриење | |
| Производ на растворливост, Ksp | 4.41×10−9 (20 °C) |
| Растворливост | |
| Забранет појас | 2.34 eV (direct)[4][5] |
Магнетна чувствителност (χ) |
−126.5·10−6 cm3/mol[6] |
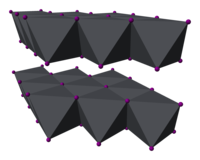
| Структура | |
| Кристална структура | Шестаголна hP6 |
Просторна група |
P63mc, No. 186 |
Константа на решетката |
|
Константа на решетката |
|
| octahedral | |
| Термохемија | |
| Стандардна моларна ентропија S |
174.9 J/(mol·K) |
| Специфичен топлински капацитет, C | 77.4 J/(mol·K) |
| Опасност | |
| GHS-ознаки: | |
Пиктограми |
   |
Сигнални зборови |
Опасност |
Изјави за опасност |
H302, H332, H360, H373, H410 |
Изјави за претпазливост |
P201, P202, P260, P261, P264, P270, P271, P273, P281, P301+P312, P304+P312, P304+P340, P308+P313, P312, P314, P330, P391, P405, P501 |
| NFPA 704 | |
| Температура на запалување | Non-flammable |
| Слични супстанци | |
| Други анјони |
|
| Други катјони | Калај(II) јодид |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Соединението моментално има неколку специјализирани примени, како што е производството на соларни ќелии[8] и детектори за Х-зраци и гама-зраци.[9] Нејговата подготовка е забавна и популарна демонстрација во образованието по хемија, за предавање на теми како што се реакции на таложење и стехиометрија.[10] Се распаѓа од светлина на температури над 125 °C (257 °F), и овој ефект е користен во патентиран фотографски процес.[2][11]
Оловото јодид порано се користел како жолт пигмент во некои бои, со име јодид жолто. Сепак, таа употреба во голема мера е прекината поради неговата токсичност и лошата стабилност.[12]
