хемиско соединение From Wikipedia, the free encyclopedia
Октан — јаглеводород и алкан so хемиската формула C
8H
18 и згусната структурна формула CH
3(CH
2)
6CH
3. Има многу структурни изомери кои се разликуваат по мерата и местото на разгранување на јаглеродната верига. Еден од овие изомери, 2,2,4-триметилпентан (наречен изооктан) се користи како една од стандардните вредности во октанскиот број.
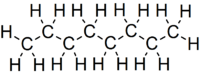 | |
 | |
 | |
| Систематско име | октан[1] |
Други називи n-октан | |
| Назнаки | |
|---|---|
| 111-65-9 | |
| 3DMet | B00281 |
| Бајлштајн | 1696875 |
| ChEBI | CHEBI:17590 |
| ChEMBL | ChEMBL134886 |
| ChemSpider | 349 |
| DrugBank | DB02440 |
| EC-број | 203-892-1 |
Гмелин |
82412 |
| 3Д-модел (Jmol) | Слика |
| KEGG | C01387 |
| MeSH | octane |
| PubChem | 356 |
| RTECS-бр. | RG8400000 |
| |
| UNII | X1RV0B2FJV |
| ОН-бр. | 1262 |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | безбојна течност |
| Мирис | бензински |
| Густина | 0,703 г/см3 |
| Точка на топење | |
| Точка на вриење | |
| 0,007 мг/дм3 (при 20 °C) | |
| log P | 4,783 |
| Парен притисок | 1,47 kPa (при 20,0 °C) |
Хенриева константа (kH) |
29 nmol/(Pa·кг) |
| Конјуг. киселина | октониум |
Магнетна чувствителност (χ) |
−96,63·10−6 см3/mol |
| Показател на прекршување (nD) | 1,398 |
| Вискозност |
|
| Термохемија | |
| Ст. енталпија на образување ΔfH |
−252,1 - −248,5 kJ/mol |
| Ст. енталпија на согорување ΔcH |
−5,53 - −5,33 MJ/mol |
| Стандардна моларна ентропија S |
361,20 J/(K·mol) |
| Специфичен топлински капацитет, C | 255,68 J/(K·mol) |
| Опасност | |
| GHS-ознаки: | |
Пиктограми |
    |
Сигнални зборови |
ОПАСНОСТ |
Изјави за опасност |
H225, H304, H315, H336, H410 |
Изјави за претпазливост |
P210, P261, P273, P301+P310, P331 |
| NFPA 704 | |
| Температура на запалување | 130 °C (266 °F; 403 K) |
| 2,200 °C (3,990 °F; 2,470 K) | |
| Граници на запалливост | 0,96 – 6,5 % |
| Смртоносна доза или концентрација: | |
LDLo (најниска објавена) |
428 мг/кг (глушец, венски)[3] |
| NIOSH (здравствени граници во САД): | |
PEL (дозволива) |
TWA 500 мд (2350 мг/м3) |
REL (препорачана) |
TWA 75 мд (350 мг/м3) C 385 мд (1800 мг/м3) [15-мин.] |
IDLH (непосредна опасност) |
1000 мд |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Ова соединение е состојка на бензинот.[4] Како и сите јаглеводороди со мала молекулска маса, октанот е испарлив и многу запалив.
Зборот „октан“ се користи за октански број, кој е показател за способноста на горивото да го сузбие тропањето кај моторите со разни соодноси на набивање, што е својствено за разгранетите ланчени изомери на октанот, особено за изооктанот. Октанскиот број на бензинот не е непосредно поврзан со моќноста на моторот. Употребата на повисокооктанско гориво отколку предвиденото за моторот не ја зголемува неговата моќ.
Октанскиот број првично е утврден со мешање на горива само од нормален хептан и изооктан (2,2,4-триметилпентан, високоразгранет октан) и давање на противтропачки оцени од нула за нормален хетптан до 100 за чист изооктан. Противтропачката способност е зависна од уделот на изооктан во смесата. Различните изомери на октанот даваат помал или поголем октански број. На пример, n-октан (правиот ланец со 8 јаглеродни атоми без разгранетост) има негативна оценка од -20, а чистиот изооктан се оценува со 100. Некои горива имаат октански број поголем од 100, особено тие што содржат метанол или етанол.
Октанот има 18 структурни изомери (24 броејќи ги стереоизомерите):
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.