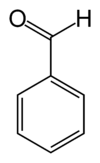
Бензалдехид (C6H5CHO) е органско соединение кој се состои од бензенов прстен со формил супституент. Тој е наједноставниот ароматичен алдехид и еден од индустриски најкорисните.
| |||
Назив според МСЧПХ Бензенкарбалдехид | |||
Други називи Бензенкарбоксалдехид | |||
| Назнаки | |||
|---|---|---|---|
| 100-52-7 | |||
| ChEBI | CHEBI:17169 | ||
| ChEMBL | ChEMBL15972 | ||
| ChemSpider | 235 | ||
| EC-број | 202-860-4 | ||
| 3Д-модел (Jmol) | Слика Слика | ||
| KEGG | D02314 | ||
| PubChem | 240 | ||
| RTECS-бр. | CU437500 | ||
| |||
| UNII | TA269SD04T | ||
| ОН-бр. | 1990 | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Изглед | безбојна течност високо реактивен | ||
| Мирис | како бадем | ||
| Густина | 1.044 g/mL, течност | ||
| Точка на топење | |||
| Точка на вриење | |||
| 6.95 g/L (25 °C)[2] | |||
| log P | 1.64[3] | ||
Магнетна чувствителност (χ) |
-60.78·10−6 cm3/mol | ||
| Показател на прекршување (nD) | 1.5456 | ||
| Вискозност | 1.321 cP (25 °C) | ||
| Термохемија | |||
| Ст. енталпија на образување ΔfH |
−36.8 kJ/mol | ||
| Ст. енталпија на согорување ΔcH |
−3525.1 kJ/mol | ||
| Опасност | |||
| GHS-ознаки: | |||
Пиктограми |
 | ||
Сигнални зборови |
Предупредување | ||
Изјави за опасност |
H302 | ||
Изјави за претпазливост |
P264, P270, P301+P312, P330, P501 | ||
| NFPA 704 | |||
| Температура на запалување | 64 °C (147 °F; 337 K) | ||
| 192 °C (378 °F; 465 K) | |||
| Граници на запалливост | 1.4–8.5% | ||
| Смртоносна доза или концентрација: | |||
LD50 (средна доза) |
1300 mg/kg (стаорец, орално) | ||
| Безбедносен лист | J. T. Baker | ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||
Тоа е безбојна течност со карактеристичен мирис на бадем. Примарната компонента на маслото од горчлив бадем, бензалдехидот може да се извлече од голем број други природни извори.[4] Синтетичкиот бензалдехид е ароматично средство во имитациониот екстракт од бадем, кој се користи за ароматизирање на колачи и други печива.[5]
Бензалдехидот првпат бил изолиран во 1803 година од францускиот фармацевт Мартрес. Неговите експерименти се фокусираа на разјаснување на природата на амигдалин, отровниот материјал кој се наоѓа во горчливите бадеми, плодот на Prunus dulcis.[6] Понатамошната работа на маслото од Пјер Робике и Антоан Бутрон Шарлар, двајца француски хемичари, произвеле бензалдехид.[7] Во 1832 година, Фридрих Волер и Јустус фон Либиг првпат синтетизирале бензалдехид.[8]
Почнувајќи од 1999 година, годишно се произведувале 7000 тони синтетички и 100 тони природен бензалдехид.[9] Хлорирањето во течна фаза и оксидацијата на толуенот се главните начини. Развиени се бројни други методи, како што се делумна оксидација на бензил алкохол, алкална хидролиза на бензал хлорид и карбонилација на бензен.[10]
Значително количество на природен бензалдехид се произведува од цинамалдехид добиен од масло од касија со ретро-алдолна реакција:[9] Цинамалдехидот се загрева во воден/алкохолен раствор помеѓу 90 °C и 150 °C со база (најчесто натриум карбонат или бикарбонат) за 5 до 80 часа,[11] проследено со дестилација на формираниот бензалдехид. Оваа реакција, исто така, дава ацеталдехид. Природниот статус на бензалдехидот добиен на овој начин е контроверзен.[9]
„Спектроскопија на нуклеарна магнетна резонанца специфична за локацијата“, која ги проценува односот на изотопот 1H/2H се користи за да се направи разлика помеѓу природно настанатиот и синтетичкиот бензалдехид.[12]
Бензалдехид и слични хемикалии природно се наоѓаат во многу видови храна. Поголемиот дел од бензалдехидот што луѓето го јадат е од природна растителна храна, како што се бадемите.[13]
Бадемите, кајсиите, јаболката и семките од цреши содржат значителни количини амигдалин. Овој гликозид се распаѓа при ензимска катализа во бензалдехид, цијановодород и два еквиваленти на гликоза.

Бензалдехидот придонесува за мирисот на буковката (Pleurotus ostreatus).[14]
Бензалдехидот може да се оксидира до бензоева киселина; всушност „бензалдехидот лесно се подложува на автооксидација за да формира бензоева киселина при изложување на воздух на собна температура“[15] што предизвикува вообичаена нечистотија во лабораториските примероци. Бидејќи точката на вриење на бензоевата киселина е многу повисока од онаа на бензалдехидот, таа може да се прочисти со дестилација. Бензил алкохолот може да се формира од бензалдехид со помош на хидрогенирање. Од реакцијата на бензалдехид со безводен натриум ацетат и оцетен анхидрид се добива циметна киселина, додека алкохолниот калиум цијанид може да се користи за катализирање на кондензацијата на бензалдехид во бензоин. Бензалдехидот е подложен на диспропорција при третман со концентрирани бази (реакција на Каницаро): една молекула од алдехидот се редуцира до бензил алкохол, а друга молекула истовремено се оксидира до бензоева киселина.
Со диоли, вклучувајќи многу шеќери, бензалдехидот кондензира за да формира бензилиден ацетали.
Бензалдехидот вообичаено се користи за да се даде вкус на бадем на храна и производи со мирис, вклучително и течности за е-цигари. Понекогаш се користи во козметички производи.[16]
Во индустриски услови, бензалдехидот се користи главно како прекурсор на други органски соединенија, почнувајќи од фармацевтски производи до пластични адитиви. Анилинската боја малахит зелена се подготвува од бензалдехид и диметиланилин. Бензалдехидот е исто така прекурсор на одредени акридински бои. Преку кондензации на алдол, бензалдехидот се претвора во деривати на цинамалдехид и стирен. Синтезата на манделична киселина започнува со додавање на цијановодородна киселина во бензалдехид:
Добиениот цијанохидрин се хидролизира до манделична киселина. (Горната шема прикажува само еден од двата формирани енантиомери).
Друга употреба
Бензалдехидот се користи како средство за заштита од пчели.[17] Мала количина раствор на бензалдехид се става на плочка за гас во близина на саќе. Пчелите потоа се оддалечуваат од чешлите за мед за да ги избегнат испарувањата.[18] Пчеларот потоа може да ги отстрани медните рамки од пчелната кошница со помал ризик и за пчелите и за пчеларот.
Како што се користи во храната, козметиката, фармацевтските производи и сапунот, бензалдехидот „генерално се смета за безбеден“ (GRAS) од американската FDA[19] и FEMA.[13] Овој статус беше реафирмиран по прегледот во 2005 година.[13] Во Европската унија е прифатен како арома.[16] Токсиколошките студии покажуваат дека е безбеден и неканцероген во концентрациите што се користат за храна и козметика,[16] а може дури и да има антиканцерогени својства.[16]
За човек тежок 70 кг, смртоносната доза се проценува на 50 мл.[10] Прифатлива дневна доза од 15 mg/ден е идентификувана за бензалдехид од Агенцијата за заштита на животната средина на Соединетите држави.[20] Бензалдехидот не се акумулира во човечките ткива.[16] Се метаболизира, а потоа се излачува во урината.[16]
Wikiwand in your browser!
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.