хемиско соединение From Wikipedia, the free encyclopedia
Арсен трихлорид — неорганско соединение со формулата AsCl3, познат и како арсен хлорид или путер од арсен. Ова отровно масло е безбојно, иако нечистите примероци може да изгледаат жолти. Тој е посредник во производството на органоарсенски соединенија.[4]
 | |
Други називи Арсен(III) хлорид, Арсен трихлорид, Путер од арсен, Ден Валакинов раствор | |
| Назнаки | |
|---|---|
| 7784-34-1 | |
| ChemSpider | 22974 |
| EC-број | 232-059-5 |
| 3Д-модел (Jmol) | Слика |
| PubChem | 24570 |
| RTECS-бр. | CG1750000 |
| |
| UNII | 5XW39M1300 |
| ОН-бр. | 1560 |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | безбојна мрсна течност |
| Густина | 2.163 g/cm3, течност |
| Точка на топење | |
| Точка на вриење | |
| Хидролизира | |
| Растворливост | растворливо во алкохол, диетил етер, HCl, HBr, хлороформ, CCl4[1] |
Магнетна чувствителност (χ) |
-79.9·10−6 cm3/mol |
| Показател на прекршување (nD) | 1.6006 |
| Вискозност | 9.77 x 10−6 Pa s |
| Опасност | |
| Безбедност при работа: | |
Главни опасности |
Многу токсичен, канцероген, корозивен, се распаѓа при контакт со вода и се ослободува HCl |
| GHS-ознаки: | |
Пиктограми |
    |
Сигнални зборови |
Опасност |
Изјави за опасност |
H301, H310, H314, H331, H350, H410 |
Изјави за претпазливост |
P201, P202, P260, P261, P262, P264, P270, P271, P273, P280, P281, P301+P310, P301+P330+P331, P302+P350, P303+P361+P353, P304+P340, P305+P351+P338, P308+P313, P310, P311, P321, P322, P330, P361, P363, P391, P403+P233, P405, P501 |
| NFPA 704 | |
| Смртоносна доза или концентрација: | |
LD50 (средна доза) |
48 mg/kg |
LCLo (најниска објавена) |
100 mg/m3 (мачка, 1 час) 200 mg/m3 мачка, 20 мин) 338 ppm (стаорец, 10 мин)[2] |
| NIOSH (здравствени граници во САД): | |
PEL (дозволива) |
[1910.1018] TWA 0.010 mg/m3[3] |
REL (препорачана) |
Ca C 0.002 mg/m3 [15-минути][3] |
IDLH (непосредна опасност) |
Ca [5 mg/m3 (as As)][3] |
| Слични супстанци | |
| Други анјони | Арсен триоксид, Арсен трифлуорид |
| Други катјони | Антимон трихлорид |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
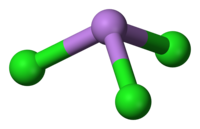
AsCl3 е пирамидална молекула со C3v симетрија. As-Cl врската е 2,161 Å, а аголот Cl-As-Cl е 98° 25'±30.[5][6] AsCl3 има четири нормални начини на вибрации: ν1(A1) 416, ν2(A1) 192, ν3 393, и ν4(E) 152 cm−1.[7]
Оваа безбојна течност се подготвува со третман на арсен(III) оксид со хлороводород проследено со дестилација:
Може да се подготви и со хлорирање на арсен на 80–85 °C, но овој метод бара елементарен арсен.[4]
Арсен трихлорид може да се подготви и со реакција на арсен оксид и сулфур монохлорид. Овој метод бара едноставна апаратура и продолжува ефикасно:[8]
Конвенционален лабораториски метод е рефлуксирање на арсен(III) оксид со тионил хлорид:[9]
Со хидролиза се добива арсенова киселина и хлороводородна киселина:
Иако AsCl3 iе помалку чувствителен на влага отколку PCl3, сè уште испарува на влажен воздух.[10]
AsCl3 подложи на редистрибуција при третман со As2O3 за да се добие неорганскиот полимер AsOCl. Со извори на хлориди, AsCl3, формира соли кои го содржат анјонот [AsCl4]−. Реакцијата со калиум бромид и калиум јодид дава арсен трибромид и арсен тријодид, соодветно.
AsCl3 е корисен во органоарсенската хемија, на пример трифениларзин е дериват од AsCl3:[11]
Отровните гасови наречени Lewisites се подготвуваат со додавање на арсен трихлорид во ацетилен:
Неорганските соединенија на арсен се многу токсични,[12] и AsCl3 особено поради неговата испарливост и растворливост (во вода).
Класифициран е како исклучително опасна супстанција во Соединетите Држави како што е дефинирано во Дел 302 од Законот за планирање вонредни состојби и Заедницата за правото на знаење (42 U.S.C. 11002) и е предмет на строги барања за известување од страна на капацитетите што произведуваат, складираат, или да го користите во значителни количини.[13]
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.