Loading AI tools
결핵균이 일으키는 감염병 위키백과, 무료 백과사전
결핵(結核, 영어: tuberculosis, TB)은 여러 종류의 미코박테륨, 특히 결핵균에 감염되어 발병하는 흔하면서도 치명적일 수 있는 전염병이다.[8] 옛말로 가슴앓이(consumption), 백사병(white death), 노체(勞瘵)라고도 했다. 결핵균은 1882년 미생물학자인 로베르트 코흐에 의해 발견되었다. 1950년대 항결핵제 개발 전까지 치료가 어려운 질병이었다. 항결핵제 이전의 치료방법은 그저 영양, 안정, 맑은 공기와 햇볕 쬐기가 치료법의 전부였으며, 수술요법으로는 감염부위를 폐쇄시키는 수술이었다.
 | |
|---|---|
| 다른 이름 | Tuberculosis, Phthisis, phthisis pulmonalis, consumption |
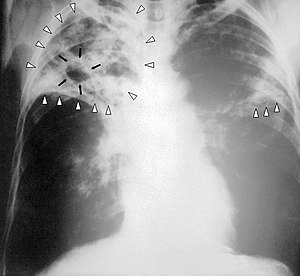 | |
| 결핵이 상당히 진행된 환자의 흉부 X-레이 사진 | |
| 진료과 | 감염병, 기도학 |
| 증상 | 만성 기침, 발열, 객혈, 체중 감소[1] |
| 병인 | 결핵균[1] |
| 위험 인자 | 흡연, 후천면역결핍증후군[1] |
| 진단 방식 | CXR, 배양, 결핵 피부반응 검사[1] |
| 유사 질병 | 폐렴, 히스토플라스마증, 유육종증, 콕시디오이데스진균증[2] |
| 예방 | 고위험군 검사, 감염자 치료, BCG 백신 접종[3][4][5] |
| 치료 | 항생물질[1] |
| 빈도 | 인구 중 25% (잠복결핵감염, latent TB)[6] |
| 사망 | 1,600,000 (2017)[7] |
결핵균은 수천 년 동안 인류에게 질병을 일으켜 왔다. 이 질환은 인체의 어느 곳에나 발생할 수 있는 전염성인 동시에 감염성인 급성질환이며 만성질환이다. 심지어는 사망에 이르게 할 수도 있는 무서운 질환이다. 결핵은 폐에 잘 걸리는데 약 85%정도가 폐에 발생하며, 혈류나 임파관을 따라 몸의 어느 기관에나 전파되어 영향을 줄 수 있다. 결핵은 환자의 기침, 콧물, 가래로부터 공기를 통해 전염된다.[9] 대부분의 감염자들은 활동성 결핵이 나타나기 전까지는 증상이 없으며, 그 중 1/10 정도가 발병한다. 이때 치료를 하지 않으면 그 중 절반 이상이 병으로 죽게 된다.
전형적인 증상은 피가 섞인 가래를 동반한 기침, 오한, 식은땀, 체중 감소이다. 다른 기관에의 감염은 다양한 증상을 초래한다. 진단은 X-레이, 투베르쿨린 반응, 체외 인터페론 감마(Interferon-gamma) 검사, 혈액 검사, 현미경 검사, 체액 배양, 중합효소 연쇄반응법(PCR)을 이용한 검사 등의 방법에 의한다.
결핵의 치료는 상당히 어렵고 길며, 치료 과정에 여러 항생제가 투입된다. 필요한 경우, 폐의 공기로부터의 접촉을 차단하거나 관리하기도 한다. 다제내성 결핵에 있어서 항생제에 대한 내성의 문제가 커지고 있다. 예방은 격리와 백신(보통은 BCG) 접종에 의존한다.
세계 인구의 1/3이 결핵균에 감염되었다고 추정된다.[10][11] 매초 1명 꼴로 새로운 환자가 발생한다. 매년 결핵을 앓는 사람들의 비율은 전 세계적으로 조금씩 줄고 있으나, 인구 증가로 새로운 환자의 수는 여전히 증가하고 있다.[12] 2007년에는 개발도상국을 중심으로 약 1,370만의 만성 질환자가 있으며, 930만의 새로운 환자가 발생하고, 180만이 사망한다고 추정되었다.[13]
결핵은 선진국에서도 생각보다 많은 사람들이 걸리고 있는데, 이는 이들의 면역계가 면역억제제와 지속적인 남용, 또는 AIDS에 위협받기 때문이다. 결핵의 분포는 전 세계적으로 균등하지 않다. 아시아와 아프리카에서는 약 80%의 인구가 투베르쿨린 검사에서 양성 반응을 나타내는 반면, 미국에서는 5~10%만이 양성 반응을 보인다.[8]
공기를 통해 감염되는 경우가 많아 폐에서의 증상 발현이 많지만, 중추신경(수막염), 임파조직, 혈류(속립 결핵), 비뇨생식기, 뼈, 관절 등에도 감염하여, 증상을 나타내는 기관도 전신에 이른다. 폐에 감염되는 결핵을 폐결핵(pulmonary tuberculosis), 다른 기관에 감염되는 결핵을 폐외결핵(extrapulmonary tuberculosis)이라고 한다. 결핵균은 다양한 기관에서 세포내 기생하며, 면역 시스템은 이를 숙주세포와 함께 공격하므로, 광범위한 조직이 파괴되어 방치하면 위중한 상태가 되어 높은 빈도로 사망에 이른다. 폐결핵에서의 심한 폐출혈과 이에 따른 객혈, 그로 인한 질식사가 이러한 병의 증상을 나타낸다.
폐 감염시 증상은 흉통, 객혈, 3주 이상 오래 지속되는 기침으로, 객담은 누렇고 끈적이는 점액성이고 호흡 곤란이나 늑막통을 동반하기도 한다. 전체적인 증상으로는 고열, 오한, 식은땀, 식욕 감퇴, 체중 감소가 있고, 얼굴이 창백해지며, 쉽게 피곤해지는 경향이 있다.[12]
나머지 부위는 감염 부위가 폐로부터 옮겨가, 다른 종류의 결핵을 발생시킨다.[17] 이는 종종 면역이 억제된 사람이나 어린이에게서 잘 일어난다. 발병 부위는 흉막염의 경우 흉막, 수막염의 경우 중추 신경계, 연주창의 경우 림프계, 비뇨 생식기 결핵의 경우 비뇨생식기계, 척추에 발생하는 포트 병의 경우 뼈와 관절이 된다.
특히 심각한 형태는 산재된 경우로, 속립 결핵이라 부른다. 폐 외부의 결핵은 폐결핵을 동반할 수도 있다.[18]
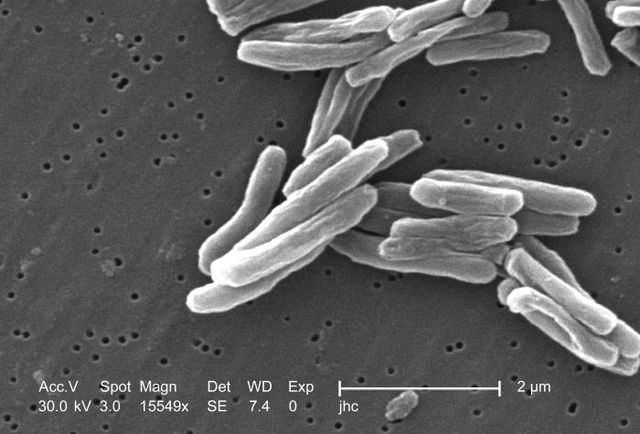

결핵의 주요 원인은 결핵균으로, 작은, 호기성의 운동 능력이 없는 간균이다. 내부가 고지방질로 되어 있어서 특이한 성질을 갖는다.[19] 결핵균은 매 16내지 20시간 마다 분열을 일으키는데, 이는 보통 1시간 내에 분열하는 다른 박테리아에 비해 매우 늦은 속도이다.[20] 결핵균은 세포벽은 있으나 인지질의 외막이 부족하여 그람 양성 박테리아로 분류된다. 어쨌거나, 결핵균은 세포벽이 지방질이 높고 미콜산을 함유하고 있어서 그람 염색에서 매우 약한 그람 양성 반응을 보이거나, 염색 상태를 유지하지 못한다.[21] 결핵은 약한 살균제에 죽지 않으며, 건조한 상태(내성포자)로 수 주를 지낼 수 있다. 사실상 박테리아는 숙주의 세포 조직에서만 성장할 수 있지만, 결핵균은 체외에서도 배양이 가능하다.[22]
가래 샘플에 대한 조직학적인 착색을 이용하여, 현미경으로 결핵을 식별할 수 있다. 결핵은 산성 용액으로 처리한 후에도 분명한 착색을 유지하여, 항산균(AFB)으로 분류된다.[8][21] 가장 흔한 항산성 착색 기술인 질-닐슨 염색(Ziehl-Neelsen stain)은 항산균을 파란색 배경에 분명하게 눈에 띄는 선홍색으로 물들인다. 항산균을 보이게 하는 다른 방법으로는 오라민-로다민 염색(auramine-rhodamine stain)과 형광현미경이 쓰인다.
결핵균군은 4가지의 결핵을 유발하는 항산균이 있는데, 이들은 M. bovis(우결핵균), M. africanum, M. canetti, M. microti 등이다.[23] M. africanum은 널리 퍼지지는 않았지만, 일부 아프리카에서는 결핵을 유발하는 주요 원인이다.[24][25] 우결핵균(M. bovis)은 한때 결핵의 주요 병원균이었으나, 저온 살균법의 도입으로 선진국의 공중 보건 문제로부터 제거되었다.[8][26] M. canetti는 드물며, 아프리카에 한정된 것으로 보이는데, 몇몇 경우는 아프리카 이주민에게서 발생하기도 한다.[27] M. microti는 주로 면역이 결핍된 사람에게서 발생한다.[28]
알려져 있는 또 다른 병원성 항산균으로는 'Mycobacterium leprae', 'Mycobacterium avium', 'M. kansasii' 등이 있다. 마지막 두 종류의 균은 결핵균이 아니지만, 결핵과 유사한 폐의 질환을 일으킨다.[29]
규폐증 환자는 결핵이 발병할 위험성이 30배 정도 크다.[30] 이산화규소(실리카)의 먼지 입자들이 호흡기를 자극하여 식작용과 같은 면역 반응을 일으키며, 결과적으로는 림프액이 많이 고이게 한다.[31] 이러한 대식세포의 봉쇄와 간섭이 결핵의 위험성을 증가시킨다.[32] 만성 신장 부전증을 앓는 사람이나 혈액을 투석중인 사람 또한 일반의 10 ~ 25배 정도 위험이 높아진다. 당뇨병을 앓는 사람은 결핵이 발병할 확률이 2 ~ 4배 높아지며, 인슐린에 의존하거나 당뇨병이 조절되지 않는 경우에는 더 높아질 수 있다. 결핵의 발병과 관련이 있는 또 다른 임상적 상태로는 위절제술로 체중이 감소하거나 영양분이 흡수되기 어려운 경우, 공회장(空回腸)의 우회, 신장 또는 심장 이식, 머리나 목의 암, 또는 다른 종양 (예를 들면, 폐암, 백혈병, 림프종 등) 등이 있다.[33]
규폐증이 결핵의 위험을 증가시키므로, 다양한 실내·외의 대기 오염원의 질병에 대한 보다 많은 연구가 필요하다. 실내에서 이산화규소가 발생하는 원인으로는 페인트, 콘크리트, 시멘트를 들 수 있다. 결정 실리카는 콘크리트, 석조물, 사암, 바위, 페인트, 기타 연마제에서 볼 수 있다. 이러한 재질들을 절단, 파괴, 파쇄, 천공, 연마하면 미세한 실리카 먼지를 발생시킬 수 있다. 또한, 흙, 회반죽, 지붕 판자에 있을 수도 있다. 먼지가 묻은 옷을 집이나 차 안에서 입는 것은, 실리카 먼지를 옮기는 행위가 될 수 있다.[34]
저체중 또한 결핵의 위험성과 관련이 있다. 체질량 지수(BMI)가 18.5 미만인 경우, 위험은 2 ~ 3배 높아진다. 반면, 체질량의 증가는 위험성을 줄인다.[35][36]
결핵은 활동성 결핵 환자가 기침을 하거나, 콧물을 흘리거나, 대화, 가래를 뱉을 때에 발생하는 지름 0.5에서 5 µm의 미세한 방울을 매개로 전염된다. 한 번의 재채기는 4만개까지의 작은 방울을 발생시킬 수 있다.[37] 각각의 방울들은 질병을 전파할 수 있는데, 이는 결핵은 10개 미만의 세균을 들여마셔도 감염될 수 있을 만큼 적은 양으로 전파가 가능하기 때문이다.[38][39]
지속적으로 잦은, 또는 긴밀한 접촉이 있는 사람들은 특히 감염될 위험이 높아 감염율이 22%에 이른다. 결핵이 활성화되었으나 치료받지 않은 환자는 매년 10 ~ 15명의 다른 사람들을 감염시킬 수 있다.[12] 또 다른 위험군으로 결핵이 만연한 지역에 거주하는 이들, 비위생적인 바늘로 약물을 주사하는 이들, 의료 지원이 열악하거나 소득이 낮은 이들, 위험성이 큰 인종·민족적 소수 집단, 고위험군의 성인에 노출된 어린이들, HIV/AIDS 등으로 면역이 결핍된 환자들, 면역억제제를 복용하는 사람들, 이러한 고위험군의 고객들의 시중을 드는 의료 서비스 종사자들을 들 수 있다.[40]
전염은 결핵이 활성화 된 환자에게서만 발생한다.[8] 한 사람으로부터 다른 사람으로의 전염될 가능성은 보균자가 내뱉는 전염성 방울의 숫자, 통풍의 유효성, 노출 기간, 결핵균의 독성에 좌우된다.[18] 연쇄적인 전파는, 병이 활동 중인 환자를 격리하고 효과적인 항결핵 치료를 받게 하여 막을 수 있다. 이러한 치료가 2주간 진행되면, 내성이 없는 활성화 된 결핵은 더 이상 전염되지 않게 된다.
결핵은 결핵에 감염된 고기를 먹음으로써 전염될 수도 있다. 'Mycobacterium bovis'는 소에 결핵을 일으킨다.
결핵균에 감염된 약 90%는 증상이 없이 잠복 중이며, 10%만이 평생 동안 결핵으로 진행될 가능성이 있다.[8]
결핵의 감염은 미코박테리아가 폐포에 도달하는 데에서 시작하는데, 세균은 침입하여 폐포대식세포(alveolar macrophages)의 엔도솜 안에서 증식한다.[8][41] 폐 안의 주요 감염부는 'Ghon focus'(초기 감염부)라 부르는데, 일반적으로 하부엽의 상부나 상부엽의 하부에 위치한다.[8] 세균은 증식을 허용하지 않는 수지상 세포에 의해 처리되는데, 이 세포들은 세균을 일부 (종격) 림프절로 옮길 수 있다. 이들은 혈류를 타고 결핵이 증식할 수 있는 폐의 다른 부분의 조직이나 기관 (특히, 상부엽의 윗부분), 주변의 림프절, 신장, 뇌, 뼈로 확산된다.[8][42] 신체의 모든 부분이 질병의 영향을 받을 수 있으나, 심장, 골격근, 췌장, 갑상선에는 영향을 주는 경우가 드물다.[43]
결핵은 육아종의 염증 상태의 하나로 분류되기도 한다. 대식세포들, T 임파구, B 임파구와 섬유아세포들은 모여 육아종을 형성하는 세포에 속하며, 감염된 대식세포를 둘러싼 임파구도 그러하다. 육아종은 미코박테리아의 전염을 막을 뿐 아니라, 면역계 세포의 소통을 위한 국소(局所) 환경을 제공한다. 육아종 내에서는, T 임파구가 감마 인터페론과 같은 사이토킨(cytokine)을 분비하는데, 이는 대식세포를 활성화하여 감염된 세균을 파괴하게 한다.[44] 세포 장애성 T세포(Cytotoxic T cell)는 또한 퍼포린(perforin)과 granulysin을 분비하여 감염된 세포들을 직접 죽일 수 있다.[41]
중요한 것은, 세균은 항상 육아종과 함께 제거되는 것은 아니며, 휴면기가 되어 잠복하게 될 수 있다.[8] 결핵 육아종의 또 다른 특징은, 결절 안에서 세포가 괴사를 일으켜 비정상적으로 죽게 된다는 것이다. 맨눈으로는 부드러운 흰 치즈의 질감처럼 보이는데, 이를 건락괴사(caseous necrosis)라 한다.[45]
결핵균이 손상된 조직으로부터 혈류에 진입하게 되면 이들은 신체에 전파되며, 많은 감염원을 만들어내는데, 이들은 모두 조직 안의 작고 흰 결절처럼 보인다. 이러한 심각한 형태의 결핵은 어린이나 고령자에서 가장 많이 발견되며, 속립 결핵이라 불린다. 속립 결핵이 있는 환자는 치료하지 않으면 사망률이 거의 100%에 가까우나, 조기에 치료되면 사망률은 10% 정도로 줄어든다.[46]
많은 환자들에서 감염은 차고 이지러진다. 조직 파괴와 괴사는 치료와 섬유 형성으로 균형을 이룬다.[45] 병에 걸린 조직은 흉터와 치즈처럼 흰 괴저성 물질로 채워진 공동으로 대체된다. 병세가 활발할 때에는, 이러한 공동 중 어떤 것들은 기관지와 연결되어 기침할 때 나오기도 한다. 여기에는 살아있는 세균이 포함되며, 전염을 일으킬 수 있다. 적절한 항생제를 사용하면 세균을 죽여 치료할 수 있다. 치료하게 되면, 감염되었던 영역들은 흉터로 대체된다.[45]
치료받지 않으면, 결핵의 감염은 대엽성 폐렴으로 진행할 수 있다.[47]

결핵은 임상 표본에서 원인이 되는 신체 기관을 확인하는 것(예를 들면, 고름이나 가래)으로부터 확정적으로 진단한다. 불가능하다면, X-레이 스캔과/또는 투베르쿨린 피부 검사(망투 검사)가 사용될 수 있다.
결핵 진단의 주요 문제는 느리게 자라는 생물체를 실험실에서 배양하기 어렵다는 것이다. (피나 가래 배양균에서는 4 ~ 12주 정도 걸릴 수 있다.) 결핵균의 완전한 의학 평가는 의학 이력, 신체 검사, 흉부 X-레이, 미생물학적인 도말표본검사, 배양이 포함되어야 한다. 또한, 투베르쿨린 피부 검사와 혈청 검사가 포함되어야 한다.[18]
결핵은 난치병은 아니지만, 치료에는 오랜 기간이 필요하다. 보통 3개월 이내에 병세가 호전되지만, 치료는 1년 가까이 계속되어야 하며, 약의 복용을 중단하게 되면 결핵균이 내성이 생기게 되어 치료가 어려워질 수 있다.[48]
결핵의 치료에는 세균을 죽이기 위해 항생제를 사용한다. 효과적인 결핵의 치료는 쉽지 않은데, 미코박테리아 세포벽은 구조와 화학적 구성이 특이하여, 여러 항생제를 무력화하며, 약의 진입을 방해한다.[49][50][51][52] 가장 흔히 쓰이는 항생제는 리팜피신과 이소니아지드이다. 다른 세균들은 단기간 항생제를 사용하는 것과는 달리, 결핵은 6개월 ~ 2년의 훨씬 긴 치료 기간을 필요로 하는데, 이는 미코박테리아를 박멸하기 위해서이다.[18] 잠복기의 결핵 치료는 통상 한 가지 항생제를 사용하는데, 활동성인 결핵은 여러 항생제의 조합으로 치료한다. 이는, 세균이 내성을 갖게 될 위험성을 줄이기 위한 것이다.[53] 잠복기의 치료는, 이후의 삶의 기간에 결핵이 활성화되는 것을 방지하기 위한 것이다.
약에 내성이 있는 결핵은 일반적인 결핵과 동일한 형태로 전염된다. 결핵은, 치료가 충분하지 않거나, 제대로 복용하지 않거나, 질 낮은 약을 사용하면 내성을 얻게 된다.[53] 내성이 있는 결핵은 여러 개발도상국의 공중 보건에 문제가 되는데, 치료 기간이 길어지고, 더 비싼 약이 필요하기 때문이다. 가장 효과적인 1차 약제인 리팜피신과 이소니아지드에 내성을 가진 경우, 다제내성 결핵(MDR-TB)이라 한다. 광범위 약제내성 결핵(XTR-TB)는 여기에 6종의 2차 약제 중 3개 이상에 내성을 가진 경우를 말한다.[54]

결핵 예방과 통제는 두 가지 방법을 병행한다. 첫 번째는, 결핵 환자와 그 접촉자들을 확인하고 치료하는 것이다. 감염의 확인은 종종 결핵 고위험군의 검사와 관련된다. 두 번째 방법은, 어린이에 백신을 접종하여 결핵으로부터 보호하는 것이다. 성인에는 신뢰할 만한 백신이 없다. 어쨌거나, 다른 미코박테리아의 종류가 많은 적도 지역에서는 결핵이 아닌 미코박테리아에 대한 노출로 어느 정도 결핵에 대한 방어가 된다.[55]
세계 보건 기구(WHO)는 1993년 결핵을 전 세계적인 보건 비상사태(global health emergency)로 선포하였고, 결핵을 퇴치하기 위한 동업자 관계는 2006년부터 2015년까지 1400만 명의 생명을 구조하기 위한 '결핵 퇴치를 위한 세계적인 계획(Global Plan to Stop Tuberculosis)을 전개했다.[56] 사람만이 결핵균(Mycobacterium tuberculosis)을 보균하므로, 박멸은 가능할 지도 모른다. 이러한 목표는 효과적인 백신이 크게 도움이 될 것이다.[57]
많은 나라에서는 BCG(Bacillus Calmette-Guérin) 백신을 결핵 통제 프로그램의 일부로, 특히 어린이들에게 사용한다. WHO에 의하면, 이는 세계적으로 가장 자주 쓰이는 백신으로, 1993년에는 172개국의 85%의 어린이들이 면역을 얻었다.[58] 미국에서는 BCG 접종을 실시하고 있지 않는데, 미국내의 결핵은 흔하지 않다.[59] BCG는 결핵의 첫 번째 백신이었다. 1905년 이후로 앨버트 칼메트와 카미유 게랭은 프랑스의 Institut Pasteur de Lille과 파스퇴르 연구소에서 BCG를 개선하였고, 1921년에 처음으로 인체를 대상으로 시도하였다.[60] 어쨌거나, 제조 과정의 결점에 인한 죽음은 BCG에 대한 대중의 저항을 불러일으켰고, 제2차 세계대전 후에야 대량 접종이 가능하게 되었다.[61] 어린이들이 결핵이 심각한 형태(예를 들면 결핵성 뇌막염)가 되는 것을 막아주는 BCG의 방어 효능은 80%를 넘는다. 폐결핵을 막아주는 성인에 대한 방어 효능은 0에서 80%까지 가변적이다.[62]
단점은, 투베르쿨린 반응을 양성화시켜 결핵의 진단이 늦어지게 한다는 것이다. 결핵균의 빈도가 낮은 지역에서는 BCG의 단점이 커진다고 여겨진다. BCG를 중지한 스웨덴, 옛 동독, 체코슬로바키아 등에서는 중지 후 어린이 결핵이 증가하였다.
남아프리카에서는, 결핵이 널리 퍼진 나라에서 BCG를 3살 미만의 모든 어린이들에게 투여한다. 어쨌거나, BCG는 미코박테리아가 비교적 유행하지 않는 지역에서는 효과가 줄어든다. 예를 들면, 미국 내에서는 특정 조건을 만족시키지 않는 사람들에는 BCG 백신 접종을 권고하지 않는다.[18]
결핵을 막기 위한 다수의 새로운 백신이, 특히 'Aeras'와 'TBVI(TuBerculosis Vaccine Initiative)'에서 개발 중에 있다. 첫 번째 유전자 재조합형의 결핵 백신인 rBCG30이 미국 내에서 NIAID(National Institute of Allergy and Infectious Diseases)의 후원으로 임상 시험에 들어갔다.[63]
결핵은 대한민국의 법정전염병으로, 1960년에 환자 수 80만으로 조사되었고, 이후 전체 인구에 대한 환자 수는 감소했으나 인구 증가로 1980년대 중반까지 환자 수 80만이 유지되었다. 이후 1990년에 72만, 1995년 62만, 1996년 43만으로 환자 수가 크게 줄어들었고, 2010년에는 17만 정도로 파악되었다. 다만 감염자수는 이보다 훨씬 많을 것으로 추정된다. 환자는 연간 35,000여명씩 발생하고 있으며, 이중 2천여명이 사망하고 있다고 보고된 바 있다.[64] 약제의 남용으로 다제내성 결핵 환자가 늘어나는 추세이다.[65] 2009년에는 사람들이 가장 많이 걸리는 전염병으로 보도되었다.[66]
2010년대 초반 기준 북한에는 약 12만여명의 결핵 환자가 있을 것으로 추정되고 있다.[67] 2010년 3월 기준으로, 북한의 결핵 환자 발생 수는 남한의 3.9배에 이르는 것으로 보고되었다.[68]
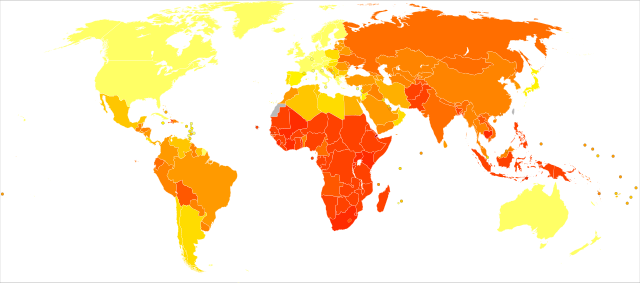


세계 인구의 약 1/3이 결핵균에 감염되어 왔으며, 매초 1명의 비율로 새로 감염된다.[12]
어쨌거나, 결핵균에 감염됐다고 해서 모두 결핵에 걸리는 것은 아니며, 많은 경우 감염의 증상이 없다. 2007년에는 약 1,370만 명이 활동적인 결핵에 걸렸으며, 930만이 새로 발병하였고, 180만이 결핵으로 죽었다. 연간 발생률은 아프리카의 10만 명당 363명에서 아메리카의 10만 명당 32명까지 차이가 있다.[13] 결핵은 가임 연령의 여성에 있어서는 가장 위험한 질병이며, HIV/AIDS 환자에 있어서는 죽음에 이르는 주요 원인이다.[72]
HIV 감염의 증가와 TB 통제 프로그램의 방치로 결핵이 활동을 재기하게 되었다.[73] 항생물질에 대한 내성을 갖는 변종 세균의 출현 또한 이러한 신종 유행의 한 원인이 되는데, 2000년에서 2004년 사이에 20%의 결핵이 표준 치료에 내성이 있었으며, 2%는 2차 약제들에 내성이 있었다.[54] 새로운 결핵이 발병하는 정도는 인접한 국가간에도 크게 달라지는데, 이는 의료 서비스 체계의 차이 때문이다.[74]
2007년, 결핵의 발생률이 가장 높은 곳은 10만 명당 1,200명이 발생한 스와질란드였다. 인도에서는 2백만 명이 발생하여 발생 수가 가장 많았다.[13] 선진국에서 결핵은 비교적 흔치 않으며, 주로 도시에서 발생한다. 영국에서는 10만 명당 15명이 발생하며, 서유럽에서 가장 높은 발병률은 10만 명 중 30명인 포루투갈과 스페인이다. 중국에서는 10만 명당 98명, 브라질에서는 10만 명당 48명이 발생한다. 미국에서는 2007년 10만명 당 4명이 발병하였다.[70] 캐나다에서는 일부 지방에서 여전히 유행하고 있다.[75]
결핵의 발생 정도는 나이에 따라 다르다. 아프리카에서 결핵은 주로 청소년들과 청년들에 영향을 준다.[76]
사람이 결핵에 걸리기 쉽게 하는 몇 가지 알려진 인자가 있다. 전 세계적으로 가장 중요한 인자는 HIV이다. 사하라 사막 이남에서는 결핵이 HIV와 함께 감염되는 것이 특별한 문제가 되는데, 이는 해당 지역에서 HIV의 발생 빈도가 높기 때문이다.[77][78] 하루 20개비 이상의 흡연 또한 결핵의 발병 위험을 2 ~ 4배 늘린다.[79][80] 진성 당뇨병 또한 개발도상국에서 증가하고 있는 중요한 위험 요소 중 하나이다.[81] 결핵 발병의 위험을 높이는 다른 질병으로는 호지킨 림프종, 말기 간염, 급성 폐 질환, 영양실조, 알코올 중독 등이 있다.[8]
식습관 또한 위험도를 바꿀 수 있다. 예를 들면, 런던의 인도 아대륙으로부터의 이주민 중에 채식주의자 힌두교 아시아인들은 결핵에 걸릴 위험성이 매일 고기와 생선을 먹는 이슬람교 신자들보다 8.5배 높았다.[82] 인과관계는 자료를 통해 입증되지 않았으나,[83] 이러한 위험의 증가는 미량 영양소 결핍에 의한 것일 수 있다. 결핍된 영양소는 철일 수도, 비타민 B12나 비타민 D일 수도 있다.[82] 심층적인 연구에서는 비타민 D 부족과 결핵에 걸릴 위험성 증가와의 관련성에 대한 더 많은 증거가 제공되었다.[84][85] 세계적으로, 일부 개발도상국에서 흔한 심각한 영양 실조는 면역계에 손상을 주어 활동적인 결핵이 발생할 위험을 크게 증가시킨다.[86][87] 인구 과밀과 함께, 부족한 영양은 결핵과 부가 강한 관련성을 갖는 원인일 수 있다.[88][89]
죄수들(특히 빈곤 국가)은 과밀한 수용과 부족한 영양 상태와 공공 의료 서비스로 HIV/AIDS와 결핵과 같은 감염병에 걸리기 쉽다. 1990년대 초에는 동유럽의 여러 나라에서 죄수들의 결핵 발생이 보고되었다. 죄수들간의 결핵의 확산은 일반인에 비해 훨씬 높다. - 일부 국가에서는 40배까지 높았다.[90][91]
결핵은 고대로부터 인간 세계에 존재해 왔다. 모호하지 않은 가장 오래된 결핵균(Mycobacterium tuberculosis)은 약 17,000년 전의 북아메리카 들소의 뼈에서 발견되었다.[92] 결핵이 소에서 유래하여 인간에게 옮긴 것인지, 또는 공통의 조상으로부터 파생되어 다른 종으로 전염된 것인지는 현재까지는 명확하지 않다.[93] 어쨌거나, 결핵균(M. tuberculosis)이 우결핵균(M. bovis)의 직계 후손이 아닌 것은 명확하며, 비교적 최근에 진화한 것으로 보인다.[94]
동지중해 신석기 정착지 인골에서 선사시대(BC 7000)에 사람이 결핵에 걸린 증거가 있으며,[95] 결핵성 부식이 미라의 등뼈에서 발견되었다.[96] 'Phthisis'(소모성 질환)는 결핵에 대한 그리스 말이었다. 기원전 460년경, 히포크라테스가 'Phthisis'를 당시 가장 널리 퍼진, 피를 토하고 열이 나는, 거의 대부분의 경우 치명적인 질병으로 확인하였다.[97] 남아메리카에서 가장 이른 결핵의 증거는 파라카스 문화(약 B.C.750 ~ A.D.100)와 관계가 있다.[98][99] 북아메리카의 선사시대의 유골들은 이 병이 흔하여 선사시대 후기 사회의 거의 모든 구성원이 결핵에 노출되었음을 보여준다.[100]
19세기 낭만주의가 퍼지면서 사람들은 결핵을 천재성의 상징이라고 여겼다. 창백한 피부, 붉은 뺨 그리고 피 묻은 손수건을 예술적 열정의 표시라고 생각했다. 1800년대 초까지 결핵으로 유럽 인구의 1/4이 죽었다. 원인을 잘 알지 못하던 시절의 일본에서는 상사병이라고도 불렀다. 1882년 코흐에 의해 결핵균이 알려지자 결핵은 낭만의 상징이 아니라 지구상에서 가장 무서운 균으로 바뀌었다.
결핵에 대한 연구는 《의학전범》(The Canon of Medicine 또는 '회회약방')을 저술한 이븐 시나의 1020년대로 거슬러 올라간다. 그는 폐결핵을 감염병으로 인식한 최초의 의사였으며, 당뇨병과의 관련성을 주목한 것도 최초였다.[101] 이븐 세나는 고대 그리스로부터 감염병은 공기의 오염으로부터 비롯된다는 이론을 채택하였다.[102] 그는 결핵의 전파를 막기 위해 격리하는 방법을 발전시켰다.[103] 대 플리니우스가 저술한 《박물지》에서와 같이, 고대의 치료는 환자의 영양에 중점을 두었다.[104]
1689년 의사 리처드 모턴에 의해 폐결핵이 혹('tubercles')과 관련이 있음이 규명되었으나,[105][106] 결핵은 그 증세가 다양하여 1820년대까지는 하나의 병으로 인식되지 않았고, 1839년이 되어서야 J. L. Schönlein에 의해 'tuberculosis'로 명명되었다.[107] 첫 번째 결핵 요양원이 헤르만 브레머에 의해 1854년 독일 Görbersdorf(현재는 폴란드 Sokołowsko)에서 문을 열었다.[108]

결핵을 발생시키는 간균인 '결핵균(Mycobacterium tuberculosis)'은 1882년 3월 24일 로베르트 코흐가 발견하였다. 그는 이 발견으로 1905년 노벨 생리학·의학상을 받았다.[109] 코흐는 소와 사람의 결핵이 유사하다고 생각하지 않았기에, 감염된 우유를 감염원으로 인식하는 데 시간이 걸렸다. 이는 후에 저온 살균 공정에서 제거되게 된다. 1890년 코흐는 결핵에 대한 치료로서 결핵균의 글리세린 추출물을 발표하면서 이를 '투베르쿨린(tuberculin)'이라 불렀다. 투베르쿨린은 효과가 없었으나, 후일 증상을 보이기 전의 결핵 검사에 채택되었다.[110]
결핵에 대한 성공적인 백신은 1906년 알베르 칼메트와 카미유 게랭이 약화된 소의 결핵으로부터 개발한 것이 최초이다. 이는 'BCG'(Bacillus Calmette-Guérin, 칼메트와 게랭의 간균)로 불렸고, 1921년 프랑스에서 처음으로 사람에 사용되었으나,[60] 제2차 세계대전 후에야 미국, 영국, 독일 등에 널리 채택되었다.[61]
결핵(Tuberculosis 또는 consumption)은 19세기와 20세기초 도시 빈민의 고질적인 질병으로서의 우려를 확산시켰다.[111] 1815년에는 영국에서 네 명 중 한 명이 결핵으로 죽었으며, 프랑스에서는 1918년까지 여섯 명 중 한 명이 결핵이 원인이었다. 20세기에 약 1억 명이 결핵으로 죽었다.[112] 1880년대에 전염성임이 규명된 후, 영국에서 결핵은 신고대상질병이 되었다. 공공 장소에서는 침을 뱉지 않는 캠페인이 있었고, 감염된 빈민은 감옥과 유사한 요양원에 들어가도록 압력을 받았다. 중상류층을 위한 요양원은 보살핌과 치료가 제공되었다.[108] 요양원에서의 신선한 공기와 노력이 도움이 된다고 주장되었건 간에, 최상의 조건에서도 요양원에 들어간 사람들 중 50%는 5년내로 사망하였다.[108]

크리스마스 실의 홍보는 1904년 결핵 프로그램을 위한 모금을 위해 덴마크에서 시작되었다. 이는 1907년 ~ 1908년에는 미국폐협회(당시 명칭은 National Tuberculosis Association)에 도움을 주기 위해 미국과 캐나다로 확장되었다.
미국에서는 결핵에 대한 우려가 확산되어 타구(唾具) 외에는 공공 장소에서 침뱉기를 금지하는 운동에 역할을 하였다.
유럽에서는 결핵으로 인한 사망자가 1850년 10만 명 중 500명에서 1950년 10만 명 중 50명으로 줄어들었다. 공중 위생의 향상은 항생제가 등장하기 전에도 결핵을 줄이고 있었다. 하지만, 결핵은 여전히 공중 위생의 큰 적으로, 1913년 영국의 의학 연구 협의회가 구성되었을 때, 첫 과제가 결핵의 연구였다.[113]
1946년 항생제 스트렙토마이신이 개발되고 나서야 유효한 치료가 가능해졌다. 그 전에는 요양원 외에 가능한 유일한 치료는 외과 수술이었으며, 기흉이나 충전법(充塡法) 기술과 함께 기관지경술과 흡입이 사용되었는데, 이득이 적어 1950년대까지 대부분 중지되었으나,[114] 다제내성 결핵의 출현으로 수술을 이들 감염의 치료의 일부로 다시 도입하게 되었다. 여기에서, 외과적으로 감염된 혹을 제거하는 것은 폐내의 세균의 수를 줄이고, 남은 세균들이 혈류내의 약제에 더 노출되게 할 것이어서 화학요법의 효과를 늘릴 것으로 여겨지고 있다.[115]
결핵이 완전히 사라질 것이라는 기대가 있었으나, 1980년대에 약제 내성을 갖는 변종이 대두하였다. 예를 들자면, 영국내 결핵의 발생은 1913년 약 117,000명에서 1987년 5,000명으로 떨어졌으나, 다시 증가하여 2000년에는 6,300명, 2005년에는 7,600명에 달하였다.[116] 미국 뉴욕 시는 공중 보건 설비의 제거와 HIV의 등장으로 1980년대 후반에 결핵이 다시 증가하였다.[117] 치료를 마치지 못하는 환자 수가 많아 뉴욕 시는 2만 명이 넘는 다제내성 결핵 환자에 대응해야 했다.
결핵의 재기로 세계 보건 기구(WHO)에서는 1993년 세계적인 보건 비상사태를 선포하기에 이르렀다.[118] 매년, 전 세계적으로 거의 50만 명이 새로 다제내성 결핵에 걸린다.[119]
일제강점기 초기의 조선 내 결핵 환자는 비교적 적었다. 1925년에는 약 11,900 명 정도로 파악되었고,[120] 그 중 조선인은 8,238명이었으며, 목축업 상업 교통 업자가 가장 많았다. 당해 조선인 결핵 환자는 3,100명이 사망하였다. 조선에 나병 환자에 비해 결핵 환자가 적다는 점이 주목받기도 했다.[121]
1920년대 후반에 조선 내 결핵 환자가 매년 3천 명씩 증가한다고 보도되었고,[122] 1927년에는 셔우드 홀이 결핵 환자를 위한 첫 요양원인 '해주구세요양원'을 건립하였다.[123]
1930년대에 들어서자 결핵 환자는 함경도에서만도 36,100명에 이르렀고,[124] 1932년 겨울에는 조선 최초로 크리스마스 실이 판매되었다.[125] 1936년에는 조선 내 결핵환자가 45만으로 발표되었고,[126] 조선총독부 경무국 위생과에서는 조선의 결핵예방법령을 실시하고 결핵예방협회를 설치하여 전조선적인 폐결핵 예방 운동을 계획하였다.[127] 6월 6 ~ 8일에는 '결핵예방주간'으로 지정하여 상담소 개설, 객담 검사, 강연회 등 여러 행사를 개최하였다.[128]
1930년대 후반에는 농촌에서도 결핵 환자가 증가하고 있음이 보도되었다.[129]
결핵은 포유류에 의해 전파될 수 있다. 고양이나 개와 같은 길들여진 종은 일반적으로 결핵과는 무관하나, 야생 동물들은 전파할 수도 있다.
소결핵균은 소의 결핵을 유발한다. 소와 사슴의 무리에서 소결핵을 박멸하기 위한 노력이 뉴질랜드에서 진행 중이다.
Seamless Wikipedia browsing. On steroids.
Every time you click a link to Wikipedia, Wiktionary or Wikiquote in your browser's search results, it will show the modern Wikiwand interface.
Wikiwand extension is a five stars, simple, with minimum permission required to keep your browsing private, safe and transparent.